
����Ŀ����ͼװ���У�������ʵ������ʼʱ����С�Թ��еĵ����ڵ�Һ���½���һ��ʱ����ڵ�Һ��������Ը���U���е�Һ�档�����йؽ��Ͳ���������
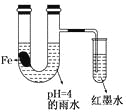
A. ����Ƭ��������̼����ǿ���Ŀ���ʴ��
B. ��ˮ���Խ�ǿ������Ƭ��ʼ�������ⸯʴ
C. ������īˮҺ�����ʱ��������Ӧʽ��O2��2H2O��4e��==4OH��
D. ���ŷ�Ӧ�Ľ��У�U������ˮ����������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�����ʵ�����ӷ���ʽ����ȷ����( )
A.��ʯī�缫��ⱥ��ʳ��ˮ��2Cl- + 2H2O![]() 2OH-+ H2��+ Cl2��
2OH-+ H2��+ Cl2��
B.��Na2CO3��Һ������¯ˮ���е�CaSO4��CaSO4(s)+CO32-![]() CaCO3(s) + SO42-
CaCO3(s) + SO42-
C.����������ϡ���ᷴӦ��Fe+NO3��+4H+= Fe3++NO��+2H2O
D.��Ba(OH)2��Һ����μ���NaHSO4��Һ��Ba2+ǡ�ó�����ȫ��Ba2����OH����H����SO42-= BaSO4����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ա�
(1)�� 25�桢101kPa ʱ��C(s)��H2(g)��CH3COOH(l)��ȼ���ȷֱ�Ϊ 393.5kJ/mol��285.8kJ/mol��870.3kJ/mol���� 2C(s)+2H2(g)+O2(g)= CH3COOH(l)�ġ�H=___________��
(2)�¶�Ϊ T ʱ���� 2 L ���ܱ������м��� 2.0 mol SO2 �� 1.0 mol O2 ������Ӧ���ﵽƽ��ʱ����������ѹǿ��Ϊ��ʼʱ�� 0.7 �����÷�Ӧ��ƽ�ⳣ��Ϊ_____��
(3)��һ����� pH��12 �� Ba(OH)2 ��Һ�У���μ���һ�����ʵ���Ũ�ȵ� NaHSO4 ��Һ�� ����Һ�е� Ba2��ǡ����ȫ����ʱ����Һ pH��11������Ӧ����Һ��������� Ba(OH)2 ��Һ�� NaHSO4 ��Һ�����֮�ͣ��� Ba(OH)2 ��Һ�� NaHSO4 ��Һ____
(4)������ͼ��ʾ�ĵ��װ�ã��ɽ������е� NO��SO2 ת��Ϊ����泥��Ӷ�ʵ�ַ����Ļ� �������á�ͨ�� NO �ĵ缫��ӦʽΪ_____����ͨ��� NO ���Ϊ 4.48 L(�����)������������һ�缫ͨ�� SO2 �����ʵ���ӦΪ_________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ը���������(��Ҫ�ɷ�ΪAl2O3��Fe2O3��SiO2������FeS2�ͽ���������)Ϊԭ�ϣ�����Al(OH)3�����Fe3O4�IJ��ֹ���������ͼ��

��1�����չ��̾������SO2����������SO2���Լ�������______��
��2������1%CaO�Ͳ�����CaO�Ŀ�۱��գ�����ȥ�������¶ȱ仯������ͼ��ʾ��

��֪���������������εķֽ��¶ȶ�����600��
��ȥ����=(1![]() )��100%
)��100%
��500�決��(������CaO�Ŀ��)ʱ��ȥ������Ԫ����Ҫ��Դ��______��
��700�決��ʱ������1%CaO�Ŀ����ȥ���ʱȲ�����CaO�Ŀ����ȥ���ʵ͵���Ҫԭ����______��
��3������AlO2-����Һ��ͨ�����CO2���õ�Al(OH)3��ɫ�����������÷�Ӧ�����ӷ���ʽΪ______��
��4��FeS2��������Fe2O3��ȱ�������±�������Fe3O4��SO2��������1molFeS2��ȫ���뷴Ӧ���ɵ�Fe3O4�����ʵ���Ϊ______mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼʵ��װ�ý������ʵ�飬�ܵó���Ӧʵ����۵��ǣ� ��
a | b | c | ʵ����� |
| |
A | Ũ���� | CaCO3 | C6H5ONa��Һ | ���ԣ�̼����� | |
B | Br2�ı���Һ | ��м | AgNO3��Һ | ����Һ�巢��ȡ����Ӧ | |
C | Ũ���� | ����KMnO4��Һ | �⻯����Һ | �����ԣ�Cl2��I2 | |
D | ����ʳ��ˮ | ��ʯ | ����KMnO4��Һ | ��Ȳ���л�ԭ�� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ�Ļ�����Ʒ���ǵ��ʹ�ҵ�����������ԭ�ϡ�
��1��д��ʵ������ȡ�����Ļ�ѧ����ʽ_____��
��2����ҵ�Ϻϳɰ��ķ�ӦN2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
�����������仯��ͼ��ʾ��
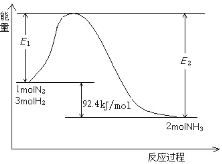
�ٸ÷�Ӧ��_____��Ӧ��������������������������
���ڷ�Ӧ��ϵ�м��������E2��_____��������������������С��������������
����Ҫ����NH3���ʣ��ɲ�ȡ�Ĵ�ʩ��_____��������ĸ��
a.�����¶� b.����ѹǿ c.���Ϸ����NH3
��3��������ͼ��ʾװ��̽��NH3�ܷ�NO2������
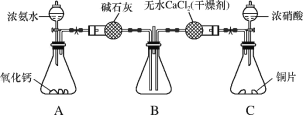
��Cװ������ȡNO2��Ӧ�����ӷ���ʽ��_____��
��ijͬѧ��ΪNH3�ܱ�NO2��������ȫ�����������ʣ�Ԥ�ڹ۲쵽Bװ���к���ɫ��ʧ���±�Ϊ��ͬʱ���¹۲쵽������
ʱ�� | 1���� | 2���� | 3���� |
���� | ����ɫδ��ʧ | ����ɫδ��ʧ | ����ɫδ��ʧ |
�����û�дﵽԤ��������ܵ�ԭ����д������_____��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������������ȷ����
��3lg�������1.5NA��P-P��
��1L0.1mol��L-1��Na2CO3��Һ�����������ӵ�����ĿΪ0.1NA
�۱�״���£�22.4LHF �к���NA������
�ܵ�⾫��ͭʱ����ת��NA�����ӣ��������ܽ�32gͭ
�ݽ�2.24L(��״��)Cl2����ˮ��ת�Ƶĵ�����Ϊ0.1NA
�����£�����0.2molH2SO4��Ũ����������ͭ��Ӧ������SO2���ӵ���ĿС��0.1NA
��142gNa2SO4 ��Na2HPO4�Ĺ����������������������ӵ�����ĿΪ3NA
��NA��Fe(OH)3�������ӵ�����Ϊ107g
A.2��B.3��C.4��D.5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�����õ��NaB(OH)4��Һ�Ʊ�H3BO3�Ĺ���ԭ������ͼ�� ����˵������ȷ����
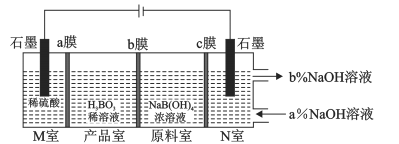
A.bĤΪ�����ӽ���Ĥ
B.N����,���ںͳ���NaOH��Һ��Ũ��:a%<b%
C.���Ӵ����ʯī�缫����,�Ⱥ�a��b��cĤ�����ұ�ʯī�缫
D.������ÿ����1molH3BO3,�����ҹ�����33.6L����(��״��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ļ�ѧʽΪ![]() ���ṹʽΪ
���ṹʽΪ![]() ��������±�����ƣ������й�������ȷ���ǣ� ��
��������±�����ƣ������й�������ȷ���ǣ� ��
A.���������м��м��Լ������зǼ��Լ�
B.����������![]() ���ļ�������
���ļ�������![]() ���ļ���
���ļ���
C.�����������2��![]() ����4��
����4��![]() ��
��
D.�������ܺ�����������Һ������Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com