
【题目】为了测定草酸晶体(H2C2O4·xH2O)中的 x 值,进行如下实验
(1)称取 Wg 草酸晶体,配成 100.00mL 溶液
(2)取 25.00mL 所配溶液于锥形瓶内,加入适量稀 H2SO4 后,用浓度为 amol/L 的 KMnO4 溶液滴定至 KMnO4不再褪色为止,所发生的反应为: 2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2 ↑+2MnSO4+8H2O。 试回答:
①实验中,需要的仪器有(填序号)_____,还缺少的仪器有____________(填名称)
A、托盘天平(带砝码、镊子) B、滴定管 C、100mL 的量筒 D、100mL 的容量瓶
E、烧杯 F、漏斗 G、锥形瓶 H、玻璃棒 I、药匙 J、烧瓶
②实验中,标准 KMnO4 溶液应装在_____式滴定管中,因为__________________
③若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴至终点,则所测得的 x 的值会_____(填偏大、偏小、无影响)。
④在滴定过程中若用去 amol/L 的 KMnO4 溶液 VmL,则所配制的草酸溶液的物质的量浓度为____________mol/L,由此,x=_____。
⑤若滴定终点读数时俯视刻度,则计算的 x 值会_____(填偏大、偏小、无影响)。
【答案】 A、B、D、E、G、H、I 胶头滴管、铁架台带滴定管夹 酸 KMnO4溶液有腐蚀性,会腐蚀橡胶 无影响 0.1aV ![]() -5 偏大
-5 偏大
【解析】(2)①为了配制准确浓度的草酸溶液,所需要的实验仪器主要有天平(含砝码)、烧杯、药匙、100mL容量瓶、胶头滴管、玻璃棒等;用高锰酸钾溶液进行滴定测草酸的物质的量,所需要的实验仪器主要有烧杯、酸式滴定管、铁架台(带滴定管夹)、锥形瓶等,故需要的仪器有:ABDEGHI,还缺少的仪器有:胶头滴管、铁架台带滴定管夹,故答案为:ABDEGHI;胶头滴管、铁架台带滴定管夹;
②高锰酸钾具有强氧化性,会腐蚀橡胶管,应装在酸式滴定管中,故答案为:酸;KMnO4溶液有腐蚀性,会腐蚀橡胶;
③滴定时为减小实验误差,应用少量蒸馏水将锥形瓶内壁冲洗,使草酸完全反应,所以用少量蒸馏水将锥形瓶内壁冲洗一下,对实验结果无影响,故答案为:无影响;
④2KMnO4 ~ 5H2C2O4
2mol 5mol
aV×10-3mol0.025L×cmol/L
解得:c=0.1aVmolL-1
H2C2O4xH2O~H2C2O4 ~xH2O
1mol 18xg
0.1aV×0.1 W-0.1aV×0.1×90
解得x=![]() -5,故答案为:0.1aV;
-5,故答案为:0.1aV; ![]() -5;
-5;
⑤滴定终点时俯视滴定管刻度,会导致测量体积偏小,测定草酸质量偏小,则x值会偏大,故答案为:偏大。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】除去下列物质中的杂质选用的试剂和方法最合理的是
物质 | 杂质 | 试剂 | 方法 | |
A | 甲烷 | 乙烯 | 酸性高锰酸钾溶液 | 洗气 |
B | 氯化亚铁溶液 | 氯化铁 | 过量铁粉 | 过滤 |
C | 二氧化硅 | 氧化铝 | 氢氧化钠溶液 | 过滤 |
D | 乙酸乙酯 | 乙酸 | 饱和碳酸钠溶液 | 蒸馏 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是一种检验某气体化学性质的实验装置,图中B为开关。如先打开B,在A处通入干燥氯气,C中干燥红色布条颜色无变化;当关闭B时,C处干燥红色布条颜色褪去。则D瓶中盛有的不可能是
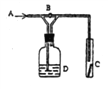
A. 饱和NaCl溶液 B. 浓H2SO4
C. 浓Na2SO4溶液 D. H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 大气污染问题日益引起全民关注.
(1)PM2.5是指大气中直径小于或等于2.5μm(1μm=103nm)的颗粒物.下列说法不正确的是______(填字母序号)。
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1~2.5μm的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(2)某地科研工作者用五年时间研究出利用石灰乳除工业燃煤尾气中的硫(SO2、SO3)和氮(NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4和Ca(NO2)2

硫酸型酸雨的形成过程是大气中的SO2溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为___________、__________.
CaSO4可以调节水泥的硬化时间.尾气中2molSO2被石灰乳逐渐吸收最终生成了1molCaSO4,该过程中转移的电子数目为___________。
③Ca(NO2)2可制成混凝土防冻剂、钢筋阻锈剂等。尾气中NO、NO2与石灰乳反应生成Ca(NO2)2的化学方程式_________________.
(3)人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如下:

在阳极区发生的反应包括___________和H++HCO3-=H2O+CO2↑。
简述CO32-在阴极区再生的原理___________。
③再生装置中产生的CO2和H2在一定条件下反应生成甲醇,工业上利用该反应合成甲醇。
已知:25℃,101KPa下:
H2(g)+![]() O2(g)═H2O(g)△H1=-242kJ/mol
O2(g)═H2O(g)△H1=-242kJ/mol
CH3OH(g)+![]() O2(g)═CO2(g)+2H2O(g)△H2=-676kJ/mol
O2(g)═CO2(g)+2H2O(g)△H2=-676kJ/mol
写出CO2和H2生成气态甲醇等产物的热化学方程式____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定条件下N2与H2反应生成NH3,请回答:
①若反应物的总能量为E1,生成物的总能量为E2,且E1>E2,则该反应为________(填“吸热”或“放热”)反应。
②已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为________________。
(2) N2H4和H2O2混合可作火箭推进剂,已知:16 g液态N2H4和足量氧气反应生成N2(g)和H2O(l),放出310.6 kJ的热量;2H2O2(l)===O2(g)+2H2O(l) ΔH=-196.4 kJ·mol-1。反应N2H4(g)+O2(g)===N2(g)+2H2O(l)的ΔH=____________kJ·mol-1。N2H4和H2O2反应生成N2(g)和H2O(l)的热化学方程式为_______________________________________。
(3)实验室用50 mL 0.50 mol·L-1盐酸与50 mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有两处明显的错误,其中一处是缺少一种玻璃仪器,该仪器的名称为____________;实验室提供了0.50 mol·L-1和0.55 mol·L-1两种浓度的NaOH溶液,应选择_____________mol·L-1的NaOH溶液进行实验。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列数据是对应物质的熔点

据此做出的下列判断中错误的是( )
A. 铝的化合物的晶体中有的是离子晶体
B. 表中只有BCl3和干冰是分子晶体
C. 同族元素的氧化物可形成不同类型的晶体
D. 不同族元素的氧化物可形成相同类型的晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y均为主族元素,I为电离能,单位是kJ/mol。根据下表所列数据判断错误的( )
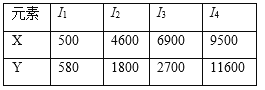
A. 元素X的常见化合价是+1价
B. 元素Y是ⅢA族的元素
C. 元素X与氯形成化合物时,化学式可能是XCl
D. 若元素Y处于第3周期,它可与冷水剧烈反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生活密切相关,下列有关物质的用途和原理分析正确的是
选项 | 物质的用途 | 原理和分析 |
A | 漂白粉可用于食品漂白 | 漂白粉能使食品中的色素褪色 |
B | Al(OH)3可中和胃酸 | Al(OH)3能与胃液中的酸发生中和反应 |
C | Na2O2常作供氧剂 | Na2O2在常温下能分解放出O2 |
D | 明矾可作净水剂 | 明矾溶于水后能消毒杀菌 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com