
【题目】反应①Fe(s)+CO2(g)=FeO(s)+CO(g);△H1=akJmol-1
反应②CO(g)+![]() O2(g)=CO2(g);△H2=bkJmol-1
O2(g)=CO2(g);△H2=bkJmol-1
测得在不同温度下,在密闭容器中进行的反应①的平衡常数K值随温度的变化如下:
温度/℃ | 500 | 700 | 900 |
K | 1.00 | 1.46 | 2.51 |
(1)反应①的化学平衡常数表达式为___,a___0(填“>”、“<”或“=”)。在500℃2L密闭容器中进行反应①,Fe和CO2的起始物质的量均为4mol,10min后达到平衡状态,平衡时CO2的转化率为___,用CO表示的化学反应速率为___。
(2)700℃反应①到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有___(填序号)。
A.缩小反应容器体积
B.通入CO2
C.升高温度到900℃
D.使用合适的催化剂
(3)由反应①和②可求得反应2Fe(s)+O2(g)=2FeO(s)△H3中的△H3=___(用含a、b的代数式表示)。
【答案】K=![]() > 50% 0.1mol·L-1·min-1 BC 2(a+b)kJ·mol-1
> 50% 0.1mol·L-1·min-1 BC 2(a+b)kJ·mol-1
【解析】
根据平衡常数公式及三段式计算,平衡常数增大,反应吸热;根据勒夏特列原理原理分析;根据盖斯定律进行计算。
(1)反应①的化学平衡常数表达式为K=![]() ,根据表格可知,温度升高,平衡常数增大,即平衡正向移动,反应正反应为吸热反应,a>0。在500℃2L密闭容器中进行反应①,平衡常数K=1,Fe和CO2的起始物质的量均为4mol,,10min后达到平衡状态,列三段式:
,根据表格可知,温度升高,平衡常数增大,即平衡正向移动,反应正反应为吸热反应,a>0。在500℃2L密闭容器中进行反应①,平衡常数K=1,Fe和CO2的起始物质的量均为4mol,,10min后达到平衡状态,列三段式:
Fe(s)+CO2(g)=FeO(s)+CO(g)
反应前 4mol 0
变化量 xmol xmol
平衡时 (4-x)mol xmol
K=![]() ,即x=2
,即x=2
平衡时CO2的转化率为50%,用CO表示的化学反应速率为![]() 。
。
(2)700℃反应①到平衡,要使该平衡向右移动,其它条件不变时,
A.缩小反应容器体积,反应前后气体体积不变,平衡不移动,A错误 ;
B.通入CO2增大反应物浓度,平衡正向移动,B正确;
C.升高温度到900℃,正反应吸热,平衡正向移动,C正确;
D.使用合适的催化剂,不改变平衡,D错误;
答案为BC。
(3)根据盖斯定律,反应①和②可求得反应2Fe(s)+O2(g)=2FeO(s)△H3中的△H3=2△H1+△H2=2(a+b)kJ·mol-1。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图是模拟侯氏制碱法的部分装置。下列操作正确的是![]()
![]()
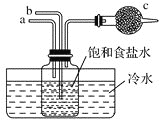
A.b通入![]() ,然后a通入
,然后a通入![]() ,c中放碱石灰
,c中放碱石灰
B.a通入![]() ,然后b通入
,然后b通入![]() ,广口瓶中析出
,广口瓶中析出![]()
C.a通入![]() ,然后b通入
,然后b通入![]() ,c中放蘸稀硫酸的脱脂棉
,c中放蘸稀硫酸的脱脂棉
D.b通入![]() ,然后a通入
,然后a通入![]() ,c中放蘸NaOH溶液的脱脂棉
,c中放蘸NaOH溶液的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】减排是各个国家都在努力为之的事,![]() 和
和![]() 的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将
的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将![]() 、
、![]() 转化为重要的化工原料。
转化为重要的化工原料。
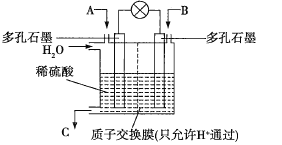
(1)若A为![]() ,B为
,B为![]() ,C为
,C为![]() ,电池总反应方程式为
,电池总反应方程式为![]() ,则正极的电极反应式为________。
,则正极的电极反应式为________。
(2)若A为![]() ,B为
,B为![]() ,C为
,C为![]() ,则负极的电极反应式为_________,电池的总反应方程式为___________。
,则负极的电极反应式为_________,电池的总反应方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 W、X、Y、Z 的原子序数依次增大,W、X 原子的最外层电子数之比为 4:3,Z 原子比 X 原子的核外电子数多 4。下列说法正确的是
A.W、Y、Z 的电负性大小顺序一定是 Z>Y>W
B.W、X、Y、Z 的原子半径大小顺序可能是 W>X>Y>Z
C.Y、Z 形成的分子空间构型可能是正四面体
D.WY2 分子中![]() 键与π键的数目之比是 2:1
键与π键的数目之比是 2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A.![]() 氦
氦![]() 含有的中子数为
含有的中子数为![]()
B.在![]() 与
与![]() 的混合物中,离子总数为
的混合物中,离子总数为![]()
C.一定条件下,丁烷催化裂化生成![]() 乙烯时,消耗丁烷的数目为
乙烯时,消耗丁烷的数目为![]()
D.已知![]() 溶液呈中性,则
溶液呈中性,则![]() 的
的![]() 溶液中含
溶液中含![]() 数目为
数目为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家。磷酸铁锂锂离子电池充电时阳极反应式为,![]() ,放电工作示意图如图。下列叙述不正确的是
,放电工作示意图如图。下列叙述不正确的是
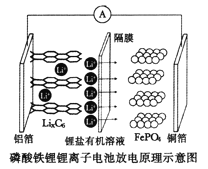
A.放电时,Li+通过隔膜移向正极
B.放电时,电子由铝箔沿导线流向铜箔
C.放电时正极反应为:![]()
D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,C、Fe、P元素化合价均不发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:
CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:
①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④B.①④⑥C.②③⑤D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将3molSO2和1 molO2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+ O2(g)![]() 2SO3(g) △H=-197kJ/ mol,当达到平衡状态时,下列说法中正确的是
2SO3(g) △H=-197kJ/ mol,当达到平衡状态时,下列说法中正确的是
A.SO2与O2的转化率可能相等
B.容器中一定存在n(SO2)>1mol且n(SO3)<2mol
C.放出的热量为197kJ
D.当O2的转化率为50%时SO2和SO3 的物质的量一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某红色固体粉末可能是Cu、Cu2O、Fe2O3中的一种或几种。为探究其组成,称取a g该固体粉末样品,用过量的稀硫酸充分反应后(已知:Cu2O+2H+=Cu2++Cu+H2O),称得固体质量为b g。则下列推断不合理的是
A. 反应后溶液中大量存在的阳离子最多有3种
B. 向反应后的溶液中加入一定量的NaNO3,可能使b g固体完全溶解
C. 若b=![]() a,则红色固体粉末一定为纯净物
a,则红色固体粉末一定为纯净物
D. b的取值范围:0<b≤a
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com