
短周期元素的A、B、C在元素周期表中的位置如图所示,已知A、C两种元素的原子核外电子数之和等于B的质子数,B原子核内质子数和中子数相等。据此填空:
| A | C | |
| B |
(1)A的氢化物分子式为 ,
(2)B在周期表中位于第 周期族;
(3)C的单质分子式为 ,C的单质溶于水所得溶液叫 。
科目:高中化学 来源: 题型:
有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
| 实验 装置 |
|
|
|
|
| 部分实 验现象 | a极质量减小,b极质量增大 | b极有气体产生,c极无变化 | d极溶解,c极有气体产生 | 电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>d B.b>c>d>a C.d>a>b>c D.a>b>d>c
查看答案和解析>>
科目:高中化学 来源: 题型:
已知HI为无色气体,在一定条件下,对于可逆反应H2(g)+I2(g) 2HI(g),下列叙述中能表明该反应已达到化学平衡状态的是( )
2HI(g),下列叙述中能表明该反应已达到化学平衡状态的是( )
A.HI的生成速率与H2的生成速率相等 B.H2的生成速率与I2的生成速率相等
C.混合物的颜色不再发生变化 D.H2、I2、HI的分子数之比为1∶1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列金属冶炼的反应原理中正确的是( )
A.2AlCl3(熔融)  2Al+3Cl2↑ B.MgO+H2
2Al+3Cl2↑ B.MgO+H2  Mg+H2O
Mg+H2O
C.ZnO+CO  Zn+CO2 D.2CuO
Zn+CO2 D.2CuO  2Cu+O2↑
2Cu+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、漂白粉等一系列物质(见下图)。下列说法正确的是( )

A.CO、SO2、SO3均是酸性氧化物 B.除去与水反应,图示转化反应均为氧化还原反应
C.工业上利用Cl2和澄清石灰水反应来制取漂白粉
D.用CO合成CH3OH进而合成HCHO的两步反应,原子利用率均为100%
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物在生产和生活中有着广泛的应用。
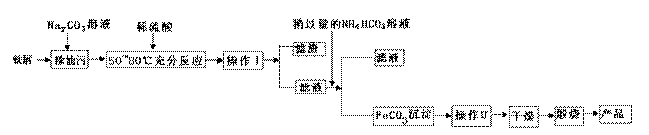
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:回答下列问题:
①操作Ⅰ、Ⅱ的名称分别是____ 、____。
②写出在空气中煅烧FeCO3的化学方程式 ;
③.煅烧如果不充分,产品中将有Fe2+ 存在,试设计实验检验产品中有无Fe2+ 。
(2)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定。
a. 称取2.850g绿矾(FeSO4·7H2O)产品,配成250mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①写出酸性KMnO4溶液与FeSO4 溶液反应的离子方程式
②计算上述样品中FeSO4·7H2O的质量分数为 [ 已知M(FeSO4·7H2O)=278g/mol]
③滴定达到终点时锥形瓶中溶液颜色变化为
④下列操作会导致样品中FeSO4·7H2O的质量分数的测定结果偏高的有_____________。
a.未干燥锥形瓶
b.盛装标准液的滴定管没有用标准液润洗
c. 滴定结束时仰视刻度线读数
d.量取待测液的滴定管没有润洗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com