
����Ŀ��Ԫ�ظ�(Cr)����Ȼ����Ҫ��+3�ۺ�+6�۴��ڡ���ش��������⣺
(1)���ø�����(FeOCr2O3)ұ����ȡ�������Ĺ���������ͼ��ʾ��
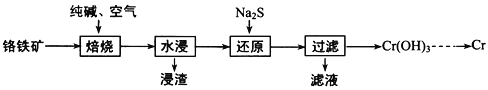
��Ϊ�ӿ챺�����ʺ����ԭ�ϵ������ʣ��ɲ�ȡ�Ĵ�ʩ֮һ��__________________ ��
����ˮ����Ҫ��ý���Һ�IJ�����_________������Һ����Ҫ�ɷ�ΪNa2CrO4��������Һ���м����ữ���Ȼ�����Һ�а�ɫ�������ɣ��� ����ԭ�������з�����Ӧ�����ӷ���ʽΪ___________________________________________________��
(2)��֪ Cr3+��ȫ����ʱ��ҺpHΪ5��(Cr3+Ũ�Ƚ���10-5molL-1����Ϊ��ȫ����)��Cr(OH)3���ܶȻ����� Ksp��_______________��
(3)��ʯī�缫��������(Na2CrO4)��Һ�������ظ�����(Na2Cr2O7)��ʵ��װ����ͼ��ʾ(��֪��2CrO42-+2H+![]() Cr2O72-+ H2O)��
Cr2O72-+ H2O)��
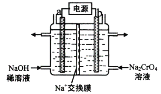
�ٵ缫b���ӵ�Դ��______��(����������������) �� b �������ĵ缫��Ӧ��______________��
�ڵ��һ��ʱ������������Һ��Na+���ʵ�����a mol��Ϊb mol���������������ظ����Ƶ����ʵ�����_______________mol ��
���𰸡���������� ���� 8CrO42��+3S2-+20H2O=8Cr(OH)3��+3SO42-+16OH- 1��10-32 �� 2H2O-4e-=O2��+4H+ (a-b)/2
��������
(1)�������̣�������(FeOCr2O3)���봿�ͨ��������գ��õ�Na2CrO4�����ˣ���Һ����Na2CrO4������Na2S��ԭ�õ�Cr(OH)3����ӦΪ��8CrO42-+3S2-+20H2O=8Cr(OH)3��+3SO42-+16OH-������Cr(OH)3�ɵõ�Cr2O3�����û�ԭ����ԭ�õ�Cr���ݴ˷������
(2)��֪Cr3+��ȫ����ʱ��ҺpHΪ5�����ʱc(OH-)=1��10-9mol/L��c(Cr3+)=1��10-5mol/L��Cr(OH)3���ܶȻ�����Ksp=c(Cr3+)c3(OH-)���ݴ˼��㣻
(3)��b���õ�Na2Cr2O7����b�з�Ӧ2CrO42-+2H+![]() Cr2O72-+H2O����b�ĵ缫��ӦΪˮ�ŵ����������������ӣ��ݴ˷�����𣻢ڸ��ݵ���غ�������㡣
Cr2O72-+H2O����b�ĵ缫��ӦΪˮ�ŵ����������������ӣ��ݴ˷�����𣻢ڸ��ݵ���غ�������㡣
(1)��Ӱ�컯ѧ��Ӧ���ʵ����أ����ʵı������С�������Խ��Ӧ����Խ�죬Ϊ�ӿ챺�����ʺ����ԭ�ϵ������ʣ���ȡ�Ĵ�ʩ�����н����������ȣ��ʴ�Ϊ����������飻
����ˮ����Ҫ��ý���Һ����Ҫ���˳���������ȡ�IJ����ǹ��ˣ�����Һ����Ҫ�ɷ�ΪNa2CrO4��������Һ���м����ữ���Ȼ�����Һ�а�ɫ�������ɣ�˵�������Na2S��������SO42-��CrԪ����+6�۽�Ϊ+3�ۣ�SԪ����-2������+6�ۣ�����ԭ���غ�͵�ʧ�����غ㣬��Ӧ�ķ���ʽΪ��8CrO42��+3S2-+20H2O=8Cr(OH)3��+3SO42-+16OH-���ʴ�Ϊ�����ˣ�8CrO42��+3S2-+20H2O=8Cr(OH)3��+3SO42-+16OH-��
(2)pHΪ5��c(OH-)=10-9��c(Cr3+)=1��10-5mol/L����Ksp��c(Cr3+)c3(OH-)=10-5��(10-9)3=1��10-32���ʴ�Ϊ��1��10-32��
(3)�ٸ���ͼʾ����b�����ڵ缫�ҵõ�Na2Cr2O7������2CrO42-+2H+![]() Cr2O72��+ H2O����������b��c(H+)������b���缫��ӦʽΪ2H2O-4e-=O2��+4H+�����a��������b���������缫b���ӵ�Դ���������ʴ�Ϊ������2H2O-4e-=O2��+4H+��
Cr2O72��+ H2O����������b��c(H+)������b���缫��ӦʽΪ2H2O-4e-=O2��+4H+�����a��������b���������缫b���ӵ�Դ���������ʴ�Ϊ������2H2O-4e-=O2��+4H+��
�ڵ��һ��ʱ������������Һ��Na+���ʵ�����a mol��Ϊb mol������Һ���ƶ��ĵ��Ϊ(a-b)mol���������·��ת�Ƶĵ���Ϊ(a-b)mol�������ĵ缫��ӦΪ��2H2O-4e-=O2+4H+�����������ɵ�������Ϊ(a-b)mol������2CrO42-+2H+Cr2O72-+H2O�������������ظ����Ƶ����ʵ�����![]() mol���ʴ�Ϊ��
mol���ʴ�Ϊ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ��������£�����ѡ����ʾ�����ʼ�ת������ʵ������
A.CH4![]() H2
H2![]() H2OB.N2
H2OB.N2![]() NH3
NH3![]() NH4Cl
NH4Cl
C.Cu![]() NO2
NO2![]() HNO3D.CH2=CH2
HNO3D.CH2=CH2![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��W��X��Y��Z��ԭ����������������������Ԫ���γɵ�һ������Һ������FeCl3��Һ����Ѫ��ɫ��������Һ��NaOH�ڼ��������»�����һ����ʹʪ��ĺ�ɫʯ����ֽ���������塣����˵����ȷ���ǣ� ��
A.W��X�γɵĻ������ڳ����¾�Ϊ��̬
B.XԪ�ؿ����γɶ��־��й㷺��;�ĵ���
C.X��Z������������Ӧˮ���ﶼ��ǿ��
D.Y�ļ�������Z�ļ����Ӿ�����ͬ�ĵ��Ӳ�ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���X��Y��M�ת����ϵ���¡������й�˵������ȷ����

A. ����̼����������X��Y
B. Y������ԭ����ͬһƽ����
C. X��Y��M���ܷ����ӳɡ�������ȡ����Ӧ
D. X���ϵĶ��ȴ��ﹲ��11��(������˳���칹)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(Ni)���仯����㷺Ӧ����������ء���ƺʹ���������
��1��ij���ط�ӦΪ2NiO(OH)+Cd+2H2O![]() Cd(OH)2+2Ni(OH)2�������س��ʱ����������������__(�ѧʽ)���ŵ�ʱ������73gCd(OH)2�������·��ת�Ƶĵ�������___��
Cd(OH)2+2Ni(OH)2�������س��ʱ����������������__(�ѧʽ)���ŵ�ʱ������73gCd(OH)2�������·��ת�Ƶĵ�������___��
��2�������ʻ���ӦΪ��Ni(s)+4CO(g)![]() Ni(CO)4(g) ��H��
Ni(CO)4(g) ��H��
��һ���¶��£���һ�����Ĵ�����CO���뵽1L�ĺ����ܱ������з�Ӧ��5s����Ni(CO)4�����ʵ���Ϊ1.5mol����0~5s��ƽ����Ӧ����v(CO)=__mol��L��s-1��
�ڸ÷�Ӧ��ƽ�ⳣ��K���¶����߶���С����÷�Ӧ����H__0(����>������<")��
��3��NiSO4��6H2O������һ����ɫ������ˮ�ľ��壬�㷺Ӧ���ڻ�ѧ������������صȣ����ɵ�Ʒ���(�������⣬������Cu��Zn��Fe��Ԫ��)Ϊԭ����ȡ����ȡ�������£�
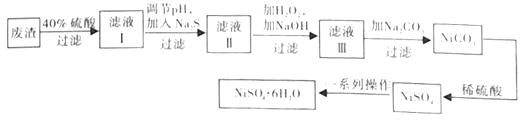
����ʵ�����У�����98%��Ũ����(�ܶ�1.84g��mL-1)����40%��ϡ���ᣬ��Ҫ�IJ����������������⣬����__��
������Һ���м���Na2S��Ŀ����_��(��֪��Ksp[FeS]=6.3��10-18��Ksp[CuS]=1.3��10-36��Ksp[ZnS]=1.3��10-24��Ksp[NiS]=1.1��10-21)
����Һ������������������Ҫ��__��
��NiSO4��ǿ����Һ����NaClO���������Ƶü������ӵ�ص缫����NiOOH���÷�Ӧ�����ӷ���ʽΪ__��
�����Ʊ�NiSO4��6H2O����ʱ��������ˮ�Ҵ���������ˮ��ϴ�Ӽ���ԭ����__(д��һ������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ���� 2 L ���ܱ������У�X��Y��Z(��Ϊ����)�����ʵ�����ʱ��ı仯������ͼ��ʾ����ش��������⣺

(1)��ͼ���������ݽ��з������÷�Ӧ�Ļ�ѧ����ʽΪ__________��
(2)��Ӧ�ӿ�ʼ��2 min���� Z ��Ũ�ȱ仯��ʾ��ƽ����Ӧ���� v(Z)��___________��
(3)_____minʱ�� ��Ӧ�ﵽƽ�⣬�����ڻ�������ƽ����Է�����������ʼʱ_____(��������������С��������������ͬ)�����������ܶ�______��
(4)�ı����д�ʩ�ܼӿ췴Ӧ���ʵ���_____(����ţ���ͬ)��
A.��ѹʱ����He B.����ʱ����He C.����ʱ����X D.����������� E.�����¶� F.ѡ���Ч�Ĵ���
(5)��������Ϊ�жϷ�Ӧ�ﵽƽ������ݵ���_____��
A.��ϵѹǿ���� B. 2v(Z)����3v(X)�� C.������������������� D.X ��ת����Ϊ 30%
(6)�� a mol X �� b mol Y �Ļ������ͨ�� 2 L ���ܱ������в�����������Ӧ����Ӧ��ijʱ�̸����ʵ����ʵ���ǡ�����㣺n(X)��n(Y)��n(Z)����ԭ��������� a��b��_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʹ���Թؽڲ��ķ����������������йء������£��������ƣ� NaUr��������Һ���ã�ȡ�ϲ���Һ�μ����ᣬ��Һ�������Ũ��c��HUr����pH�Ĺ�ϵ��ͼ��ʾ����֪Ksp��NaUr��=4.9��10-5 mol2��L-2��Ka��HUr��=2.0��10-6 mol��L-1������˵����ȷ����

A.�ϲ���Һ�У�c��![]() ��= 7.0��10-2 mol��L-1
��= 7.0��10-2 mol��L-1
B.M��N�ı仯�����У�c(Na+)��c(Ur-)��ֵ����С
C.��c(HUr)=c(Ur-)ʱ��c(Cl-)��c(Ur-)
D.��pH=7ʱ��2c(Na+)��c(Ur-)+c(Cl-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ż�����˫��[2.2.1]����Ľṹ��ʽ��ͼ��ʾ�����й��ڸû������˵���������
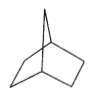
A. �뻷��ϩ��Ϊͬ���칹��
B. ���ȴ���ṹ��9��
C. ����̼ԭ�Ӳ��ܴ���ͬһƽ��
D. 1mol˫��[2.2.1]������ȫȼ��������Ҫ10 molO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������CO2����ͨ��NaOH��Ca(OH)2��NaAlO2�Ļ����Һ�У������ɳ��������ʵ�����ͨ��CO2������Ĺ�ϵ�ɱ�ʾΪ(�� )
A.  B.
B. 
C.  D.
D. 
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com