
【题目】一定条件下,碳钢腐蚀与溶液pH的关系如下:
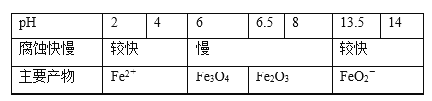
下列说法不正确的是( )
A.在pH<4溶液中,碳钢主要发生析氢腐蚀
B.在pH>6溶液中,碳钢主要发生吸氧腐蚀
C.在pH>14溶液中,碳钢腐蚀的正极反应为O2+4H++4e-=2H2O
D.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减缓
【答案】C
【解析】
A.当pH<4溶液中,酸性较强,碳钢主要发生析氢腐蚀,负极电极反应式为:Fe-2e-=Fe2+,正极上电极反应式为:2H++2e-=H2↑,故A正确;
B.当pH>6溶液中,溶液的酸性较弱,碳钢主要发生吸氧腐蚀,负极电极反应式为:Fe-2e-=Fe2+,正极上电极反应式为:O2+2H2O+4e-=4OH-,故B正确;
C.在pH>14溶液中,溶液显强碱性,碳钢主要发生吸氧腐蚀,碳钢腐蚀的正极反应O2+2H2O+4e-=4OH-,故C错误;
D.在煮沸除氧气后的碱性溶液中,碳钢主要发生吸氧腐蚀,正极上氧气浓度减小,生成氢氧根离子速率减小,所以碳钢腐蚀速率会减缓,故D正确;
故选C。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】酸雨的形成是一种复杂的大气化学和光学化学过程,在清洁空气、污染空气中形成硫酸型酸雨的过程如下:

下列有关说法错误的是( )
A. 光照能引发酸雨的形成
B. 所涉及的变化均为氧化还原反应
C. 污染空气能加快酸雨的形成
D. 优化能源结构能有效遏制酸雨污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向密闭容器中充入1.0 mol CO和2.0 mol H2O(g)发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g)。当反应达平衡时,CO的体积分数为α。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达平衡时CO的体积分数小于α的是
CO2(g)+H2(g)。当反应达平衡时,CO的体积分数为α。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达平衡时CO的体积分数小于α的是
A.0.5 mol CO+2.0 mol H2O(g)+1.0 mol CO2+1.0 mol H2
B.1.0 mol CO+2.0 mol H2O(g)+0.5 mol He
C.1.0 mol CO+1.0 mol H2O(g)+1.0 mol CO2+1.0 mol H2
D.0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应在一定条件下进行,反应类型不正确的是( )
A.CH3CH2OH+HO-NO2 → H2O+CH3CH2ONO2 (取代反应)
B.2CH2=CH2+O2 → 2CH3CHO(氧化反应)
C.nCH2=CHCH3 →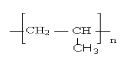 (加聚反应)
(加聚反应)
D.![]() →
→![]() (消去反应)
(消去反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W(C16H14O2)用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下:

已知:
请回答下列问题
(1)F的化学名称是______,⑤的反应类型是______。
(2)E中含有的官能团是_____(写名称),E在一定条件下聚合生成高分子化合物,该高分子化合物的结构简式为______。
(3)E + F→W反应的化学方程式为_____。
(4)与A含有相同官能团且含有苯环的同分异构体还有____种(不含立体异构),其中核磁共振氢谱为六组峰,且峰面积之比为1∶1∶2∶2∶2∶2∶2的结构简式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S2O3是一种弱酸,实验室欲用0.01 mol·L-1的Na2S2O3溶液滴定I2溶液,发生的反应为I2+2Na2S2O3===2NaI+Na2S4O6,下列说法合理的是( )
A.该滴定可用甲基橙作指示剂
B.Na2S2O3是该反应的还原剂
C.该滴定可选用如图所示装置

D.该反应中每消耗2 mol Na2S2O3,电子转移数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 和
和![]() 可以相互转化
可以相互转化![]()
![]() 。现将一定量
。现将一定量![]() 和
和![]() 的混合气体通入体积为1L的恒温恒容的密闭容器中,反应物浓度随时间变化关系如图。下列说法不正确的是
的混合气体通入体积为1L的恒温恒容的密闭容器中,反应物浓度随时间变化关系如图。下列说法不正确的是
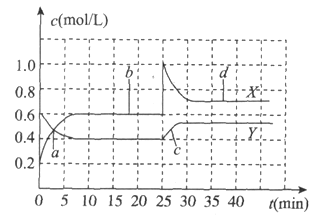
A. 反应进行至25min时,曲线发生变化的原因是加入0.4mol![]()
B. a、b、c、d四个点中,表示化学反应处于平衡状态的点是b和d
C. 图中共有两条曲线X和Y,其中曲线X表示![]() 浓度随时间的变化
浓度随时间的变化
D. 若要达到与d相同的状态,在25min时还可以采取的措施是适当缩小容器体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向2.0L恒容密闭容器中充入2molSO2和1molO2,发生反应为:2SO2(g)+O2(g) ![]() 2SO3(g)。经过一段时间后达到平衡,反应过程中测定的部分数据见下表:下列说法正确的是( )
2SO3(g)。经过一段时间后达到平衡,反应过程中测定的部分数据见下表:下列说法正确的是( )
t/s | 0 | 2 | 4 | 6 | 8 |
n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
A.反应在前2 s的平均速率υ(O2)=0.4 mol·L1·s1
B.保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C.相同温度下,起始时向容器中充入4 mol SO3,达平衡时,SO3的转化率大于10%
D.保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2) 增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com