
【题目】摩尔盐[(NH4)2Fe(SO4)2·6H2O]是分析化学中的重要试剂。摩尔盐隔绝空气加热可完全分解生成红棕色固体和其他产物。某学习小组欲探究其分解产物。
I.甲组同学设计了如下实验装置。

(1)实验中,装置B中观察到的现象是____________________。
(2)碱石灰的主要作用是__________________。
(3)装置D中观察到酚酞溶液变红色,由此可知摩尔盐分解的产物中有_____________(写化学式)。
(4)设计实验验证装置A中固体残留物不含FeO:___________________(简要说明实验操作、现象和结论)。
Ⅱ.乙组同学认为摩尔盐受热分解的产物中还含有SO2、SO3和N2。为进行验证,用甲组实验中的装置A和下列所示装置进行实验。

(5)乙组同学的实验装置中,依次连接的合理顺序为A、__________。装置G中盐酸的作用是_________________。
(6)实验中,准确称量摩尔盐7.8400 g,充分加热反应后,测得装置A中固体残留物的质量为1.6000 g,装置G中生成白色沉淀的质量为3.4950 g,装置H中收集到112 mL N2(标准状况下),写出摩尔盐受热分解的化学方程式:___________________。(分解产物被充分吸收,不考虑其损失)
【答案】(1)白色固体变为蓝色
(2)碱石灰能吸收酸性气体(3)NH3
(4)取少量A中残留物与试管中,加入适量稀硫酸,充分振荡使其完全溶解,在所得溶液中滴加高锰酸钾溶液,并振荡,无明显现象,则残留物中不含有FeO;
(5)G、E、F、H;吸收氨气、并排除二氧化硫的干扰
(6)![]()
【解析】
试题分析:(1)硫酸亚铁铵晶体的化学式为:(NH4)2Fe(SO4)26H2O,在500℃时隔绝空气加热完全分解,有水生成,所以装置B中观察到的现象是白色固体变为蓝色;(2)碱石灰能吸收酸性气体;(3)装置D中观察到酚酞溶液变红色,说明溶液呈碱性,由此可知摩尔盐分解的产物中有NH3;(4)根据亚铁离子的还原性,可以用高锰酸钾溶液检验,方法为:取少量A中残留物与试管中,加入适量稀硫酸,充分振荡使其完全溶解,在所得溶液中滴加高锰酸钾溶液,并振荡,若高锰酸钾溶液褪色,则残留物中含有FeO;若高锰酸钾溶液不褪色,则残留物中不含FeO;三氧化硫和氯化钡溶液反应生成硫酸钡沉淀,二氧化硫与氯化钡溶液不反应,二氧化硫能使品红溶液褪色,用品红检验二氧化硫;用氢氧化钠吸收二氧化硫,用排水法收集氮气,所以依次连接的合理顺序为A、G、E、F、H;装置G中盐酸的作用是吸收氨气、并排除二氧化硫生成沉淀;(6)实验中,准确称量摩尔盐7.8400 g,充分加热反应后,测得装置A中固体残留物的质量为1.6000 g,装置G中生成白色沉淀的质量为3.4950 g,装置H中收集到112 mL N2(标准状况下),7.8400 g摩尔盐的物质的量![]() =0.02mol;根据氮元素守恒,H中收集到0.005mol N2,则生成氨气的物质的量是0.01mol;G中生成白色沉淀的质量为3.4950 g,所以生成SO3的物质的量是0.015mol,根据硫元素守恒,生成二氧化硫的物质的量是0.04mol-0.015mol=0.025mol;根据电子守恒,生成0.025mol二氧化硫,生成0.005mol N2,生成氧化铁0.01mol;摩尔盐受热分解的化学方程式:
=0.02mol;根据氮元素守恒,H中收集到0.005mol N2,则生成氨气的物质的量是0.01mol;G中生成白色沉淀的质量为3.4950 g,所以生成SO3的物质的量是0.015mol,根据硫元素守恒,生成二氧化硫的物质的量是0.04mol-0.015mol=0.025mol;根据电子守恒,生成0.025mol二氧化硫,生成0.005mol N2,生成氧化铁0.01mol;摩尔盐受热分解的化学方程式:![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关于细胞内化合物的叙述,错误的是
A. 蛋白质的盘曲折叠被解开时,功能发生改变
B. 脂质中只有磷脂参与构成细胞膜
C. 落叶中的纤维素经微生物分解可产生葡萄糖
D. 种子萌发过程中自由水的比例升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照物质的树状分类和交叉分类,HNO3应属于( )
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥强氧化性酸 ⑦一元酸
⑧化合物
A.①②③④⑤⑥⑦⑧ B.①④⑥⑦⑧
C.①⑧ D.①④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海藻中提取碘的流程如下:
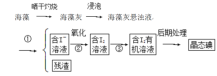
(1)写出提取碘的过程中有关实验操作的名称:①______;③________。
(2)提取碘的过程中可供选择的有机溶剂是
A.汽油、酒精
B.四氯化碳、汽油
C.醋酸、酒精
(3)为完成以上①、③两步操作,实验室里有烧杯、玻璃棒、铁架台、烧瓶、导管、酒精灯,尚缺少的玻璃仪器是____________________________________。
(4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出下图所示的实验装置中的错误之处:① ,② ,③ ,④ 。
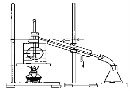
(5)为便于控制蒸馏时的温度,操作时使用水浴加热,最后晶体碘在________里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如下图所示,下列说法不合理的是

A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液退色
B.装置C的作用是吸收SO2尾气,防止污染空气
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀
D.为了验证A中发生了氧化还原反应,加入KMnO4溶液,紫红色退去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器(W)中,进行如下两个可逆反应:
①A(g)+2B(g) ![]() 3C(g)+D(s) △H1>0 ②xM(g)+N(g)
3C(g)+D(s) △H1>0 ②xM(g)+N(g) ![]() 3Q(g) △H2。反应①中各物质与反应②中各物质均不发生反应。在某容器里只进行反应②,M的转化率与温度、压强的关系如图所示。下列对W容器中进行的反应推断合理的是
3Q(g) △H2。反应①中各物质与反应②中各物质均不发生反应。在某容器里只进行反应②,M的转化率与温度、压强的关系如图所示。下列对W容器中进行的反应推断合理的是
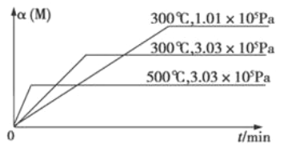
A.反应①一定是自发反应,反应②一定是非自发反应
B.若容器内温度保持不变,则 v正(B): v逆(C)=2:3
C.若恒压条件下,充入N,则C的物质的量减小
D.升高温度,两个反应的平衡常数都减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于组成细胞的化合物的叙述正确的是
A. 蛋白质分子中的N主要存在于氨基中
B. 糖原的最终代谢产物是葡萄糖
C. 组成ATP、DNA、RNA的元素种类完全相同
D. 脂肪分子中含H比糖类多,是主要的能源物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)CH4可用于设计燃料电池,甲烷燃料电池的工作原理如图(左)所示:原电池工作过程中OH-的作用是_______________;负极电极反应式为:_____________。若电路中转移电子数为0.8NA,左侧溶液中pH________(填“增大”,“减小”,”不变”)(忽略溶液体积的变化),右侧的OH-物质的量变化量为_________。
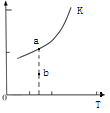
(2)CH4与H2O在隔绝空气、高温和催化剂条件下反应:
CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH=m kJ·mol—1
CO(g)+3H2(g) ΔH=m kJ·mol—1
则反应的平衡常数表达式K=______________,K的大小与温度(T)的关系如上图(右)中曲线所示,则m__________0(填“>”“=”或“<”);改变某一条件,使状态从a点到达b点,若保持温度不变,反应再次达到平衡时,则CH4的转化率___________(填“增大”、“减小”、“不变”或“不确定”),反应的焓变(△H)将_______________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com