
����Ŀ��������ⷨ���Ѱ۲����ķ�Һ[���д���FeSO4��H2SO4������Fe2(SO4)3��TiOSO4]����������Ͳ�Ѫ�������������������������£�
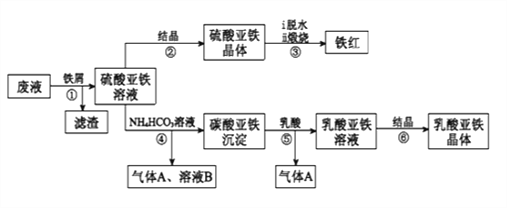
��֪��TiOSO4������ˮ����ˮ�п��Ե���ΪTiO2+��SO42-��TiOSO4ˮ���TiO2xH2O����Ϊ���淴Ӧ������ṹ��ʽΪCH3CH(OH)COOH��
��ش�
��1���������з�������������Һ�������IJ�����________________________��
��2��������м��Ŀ��һ�ǻ�ԭ����Fe2(SO4)3������ʹ����TiOSO4ת��ΪTiO2xH2O��������ƽ���ƶ���ԭ�����͵õ�������ԭ��___________________________��
��3�����������ڿ�������������������������÷�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ_________________��
��4�������ӷ���ʽ���Ͳ������м������ܵõ�����������ԭ��_________________��
��5�������������ӷ���ʽ��_________________________________________��
��6��Ϊ�ⶨ�����������þ�����FeSO4��7H2O������������ȡ������Ʒa g������ϡ�������100.00 mL��Һ��ȡ��20.00 mL��Һ����KMnO4��Һ�ζ���������KMnO4����Ӧ����������0.1000 molL-1 KMnO4��Һ20.00 mL�����þ�����FeSO4��7H2O����������Ϊ______________����a��ʾ����
���𰸡� ���� TiOSO4+(x+1)H2O![]() TiO2 xH2O��+H2SO4��TiO2++(x+1)H2O
TiO2 xH2O��+H2SO4��TiO2++(x+1)H2O![]() TiO2 xH2O��+2H+����м��H2SO4��Ӧ��c(H+)���ͣ�ʹƽ�������ƶ���TiOSO4ת��ΪTiO2xH2O���� 1: 4 FeCO3+2CH3CH(OH)COOH== Fe2++2CH3CH(OH)COO-+H2O+CO2�� Fe2++2HCO3-==FeCO3��+H2O+CO2�� 13.9/a
TiO2 xH2O��+2H+����м��H2SO4��Ӧ��c(H+)���ͣ�ʹƽ�������ƶ���TiOSO4ת��ΪTiO2xH2O���� 1: 4 FeCO3+2CH3CH(OH)COOH== Fe2++2CH3CH(OH)COO-+H2O+CO2�� Fe2++2HCO3-==FeCO3��+H2O+CO2�� 13.9/a
����������Һ�к��д���FeSO4��H2SO4������Fe2(SO4)3��TiOSO4������м��Fe��H2SO4������Fe2(SO4)3��Ӧ����FeSO4��TiOSO4ˮ������TiO2xH2O�����ˣ�����ΪTiO2xH2O��Fe����ҺΪFeSO4��FeSO4��Һͨ������Ũ������ȴ�ᾧ������ϴ�ӵõ������������壬��ˮ�����յõ���������FeSO4��Һ�м�̼����泥�����̼����������������狀Ͷ�����̼��̼�����������������ܽ���������������Һ�Ͷ�����̼������������Һͨ������Ũ������ȴ�ᾧ������ϴ�ӵõ������������塣
(1)��������������Һ�������IJ����ǹ��ˣ��ʴ�Ϊ�����ˣ�
(2)TiOSO4ˮ������TiO2xH2O�Ļ�ѧ����ʽΪ��TiOSO4+(x+1)H2O![]() TiO2xH2O��+H2SO4����м��H2SO4��Ӧ��c(H+)���ͣ�ʹƽ�������ƶ���TiOSO4ת��ΪTiO2xH2O�������ʴ�Ϊ��TiOSO4+(x+1)H2O
TiO2xH2O��+H2SO4����м��H2SO4��Ӧ��c(H+)���ͣ�ʹƽ�������ƶ���TiOSO4ת��ΪTiO2xH2O�������ʴ�Ϊ��TiOSO4+(x+1)H2O![]() TiO2xH2O��+H2SO4����м��H2SO4��Ӧ��c(H+)���ͣ�ʹƽ�������ƶ���TiOSO4ת��ΪTiO2xH2O������
TiO2xH2O��+H2SO4����м��H2SO4��Ӧ��c(H+)���ͣ�ʹƽ�������ƶ���TiOSO4ת��ΪTiO2xH2O������
(3)���������ڿ��������������������������ķ���ʽΪ��4FeSO4+O2![]() 2Fe2O3+4SO3���÷�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ1: 4���ʴ�Ϊ��1: 4��
2Fe2O3+4SO3���÷�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ1: 4���ʴ�Ϊ��1: 4��
(4)����У�̼�����������ᷴӦ����������������Ӧ�����ӷ���ʽΪFeCO3+2CH3CH(OH)COOH== Fe2++2CH3CH(OH)COO-+H2O+CO2�����ʴ�Ϊ��FeCO3+2CH3CH(OH)COOH== Fe2++2CH3CH(OH)COO-+H2O+CO2����
(5)����ܵ����ӷ���ʽ��Fe2++2HCO3-�TFeCO3��+H2O+CO2�����ʴ�Ϊ��Fe2++2HCO3-�TFeCO3��+H2O+CO2����
(6)�������ӻᱻ�����������Ϊ���������ӣ���������ԭΪ+2�۵������ӣ����ݵ����غ㣬��5FeSO47H2O��KMnO4����������0.1000molL-1 KMnO4��Һ20.00mL�����Ծ�����FeSO47H2O����������=![]() ��100%=
��100%=![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��


 ��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ᴿ��������ȷ���ǣ� ��
A.��ȥKNO3�е�NaCl����----�ᾧ.
B.��ȥʳ���е���ɳ-----����
C.��ȥKCl�е�K2CO3-----����������
D.��ȥCaCO3�е�CaO-----����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о������仯��������ʾ��м�Ϊ��Ҫ�����塣
��1�� NOx���γ����꣬д��NO2ת��ΪHNO3�Ļ�ѧ����ʽ��_____________________________
��2���ں�Cu+���ӵ�ø�Ļ�У�������� (NO2-)���ӿ�ת��ΪNO��д��Cu+�������������������ˮ��Һ�з�Ӧ�����ӷ���ʽ ��
��3����38.4 gͭ��150mLһ��Ũ�ȵ����ᷴӦ��ͭ��ȫ�ܽ⣬������NO��NO2��������ڱ�״���µ����Ϊ11.2L����ش�
�� NO2�����Ϊ____________L��
����ͭ������պ÷�Ӧ��ȫ����ԭ������Һ��Ũ��Ϊ____________molL-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��M��W��ԭ��������С�������е����ֶ���������Ԫ�أ�����X��Z��M��W����Ԫ�ص�ԭ������֮��Ϊ32����Ԫ�����ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ�Yԭ�ӵ�����������������Ӳ�����2����Z��M�������ڣ�M��Wλ��ͬ���塣�ش��������⣺
(1)Y�����ڱ��е�λ����________, W�������ӷ�����_____��
(2) Z�ĵ��ʵĽṹʽΪ________����״���£��Թ����ռ���Z�ļ��⻯�������ˮ�У��������ʲ����Թ�����ɢ����һ��ʱ����Թ�����Һ�����ʵ����ʵ���Ũ��Ϊ_______��
(3����X��Z��M����Ԫ����ɵĻ��������ᡢ��εĻ�ѧʽ�ֱ�Ϊ________������һ������
(4��д������ʱY�ĵ�����W������������ˮ�����Ũ��Һ������Ӧ�Ļ�ѧ����ʽ��____________��
(5�����������X��Z��M��W��Fe����Ԫ����ɣ���Ħ������Ϊ392g��mol-1, 1 mol���к���6 mol�ᾧˮ���Ի������������ʵ�飺
a��ȡ��ˮ��Һ���������������ŨNaOH��Һ�����ȣ�������ɫ��״��������ɫ���д̼�����ζ�����壻��ɫ��״����Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ��
b����ȡ��ˮ��Һ���������������BaCl2��Һ��������ɫ�������ټ����ᣬ��ɫ�������ܽ⡣
�� �Ļ�ѧʽΪ________��
�� ��֪100 mL 1 mol��L-1�ļ���Һ����20 mL 1 mol��L-1������KMnO4��Һǡ�÷�Ӧ��д����Ӧ�����ӷ���ʽ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ����,�۲쵽������ָ��ƫת,M�����,N����ϸ,����PΪ�������Һ���ɴ��ж�M��N��P�����������ʿ�����( )

A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ��������ˮϡ��1 mol/L�Ĵ�����Һ��0.01 mol/L��������Һ��ϡ�ͣ����и�����ʼ�ձ����������( )
A.![]()
B.![]()
C.![]()
D.![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���25 ��ʱijЩ����ĵ���ƽ�ⳣ����
��ѧʽ | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka��1.8��10��5 | Ka��3.0��10��8 | Ka1��4.1��10��7 | Ka1��5.9��10��2 |
��1��H2C2O4�뺬�����ʵ�����KOH����Һ��Ӧ��������Һ�����ԣ�����Һ�и�����Ũ���ɴ�С��˳��Ϊ��
��2����0.1 mol��L��1 CH3COOH��Һ�еμ�NaOH��Һ��c��CH3COOH����c��CH3COO������5��9����ʱ��ҺpH����
��3����̼������Һ�еμ�������ˮ�����ӷ���ʽΪ��
��4����0.1mol��L��1CH3COOH��Һ��0.1mol��L��1NaOH��Һ�������ϣ����Ի�Ϻ���Һ����ı仯������û����Һ��pH��8����c��Na+��-c��CH3COO����=mol��L��1���ȷ����������
��5����CH3COOH��Һ�����ʯ��Ӧ�������ı����44.8L����ȫ��ͨ�뵽2L 1.5mol/L��NaOH��Һ�г�ַ�Ӧ������Һ���������ӵ����ʵ���Ũ���ɴ�С��˳��Ϊ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ��Ӧ2H2��g��+O2��g���T2H2O��g���������仯ʾ��ͼ������˵����ȷ���ǣ�������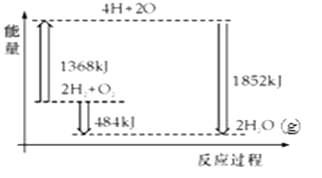
A.H2��g����O2��g����Ӧ����H2O��g �����������ȷ�Ӧ
B.2mol H2��1mol O2ת��Ϊ4mol H��2mol Oԭ�ӵĹ����зų�����
C.2mol H2��g����1mol O2��g����Ӧ����2mol H2O��g�������ų�484kJ����
D.4mol H��2mol O����2mol H2O��g�������ų�484kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������ȷ���ǣ� ��
A.����������ʹNaCl����Һ������ʱ��Ӧ���ȱ߽���ֱ����Һ����
B.��10mL��Ͳ��ȡ8.58mL����ˮ
C.����ƿ����ʱ�۲�Һ��ʱ���ӣ���ʹ��õ���ҺŨ��ƫ��
D.�þƾ���ȡ��ˮ�е�I2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com