
| A、①②⑥⑦ | B、③⑤⑦⑧ |
| C、①③⑦⑧ | D、③⑤⑥⑦ |
| 1 |
| 2 |


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
| A、为了使婴儿对食品有浓厚兴趣,我们可以在婴儿食品中多加着色剂 |
| B、为保证人体所需足够蛋白质我们要多吃肉,少吃蔬菜和水果 |
| C、食盐加碘是防止人体缺碘而加的营养强化剂,能预防地方性甲状腺肿 |
| D、为了使火腿肠颜色更鲜红,可多加一些亚硝酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时溶液中一定大量共存:Na+、Ca2+、Cl-、SO42- |
| B、能与铝反应放出氢气的溶液中一定共存:Mg2+、Cu2+、SO42-、NO3- |
| C、弱碱性溶液中可能大量共存:Na+、K+、Cl?、HCO3? |
| D、0.1mol/LFeCl3溶液中可能大量共存:Fe2+、NH4+、SCN-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5a=2b |
| B、2a=5b |
| C、3a=2b |
| D、2a=3b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配制一定物质的量浓度的溶液时,容量瓶必须洁净、干燥,不漏水 |
| B、实验室里需要480mL2.0moI?L-1氢氧化钠溶液,配制溶液时先称量氢氧化钠固体38.4g,然后再按照溶解、冷却、洗涤、定容、摇匀的步骤进行操作 |
| C、25℃时,用惰性电极电解某浓度的NaOH溶液,一小段时间后,NaOH溶液的浓度可能增大,也可能不变 |
| D、K2CO3在酒精灯上灼烧时能直接观察到紫色火焰 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素X、Y、Z、W在周期表中的位置如图所示,其中W的氧化物是形成酸雨的主要物质之一.
短周期元素X、Y、Z、W在周期表中的位置如图所示,其中W的氧化物是形成酸雨的主要物质之一.| X | |||
| Z | W | Y |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0℃H2+F2═2HF |
| B、40℃H2+Cl2═2HCl |
| C、200℃H2+Br2(g)═2HBr |
| D、300℃H2+I2(g)═2HI |
查看答案和解析>>
科目:高中化学 来源: 题型:
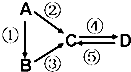 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S2- |
| B、S |
| C、SO32- |
| D、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com