
【题目】化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其他成分遇到盐酸时无气体产生.
(1)摩擦剂中氢氧化铝的定性检验.
取适量牙膏样品,加水充分搅拌、过滤.
往滤渣中加入过量NaOH溶液,过滤,滤液中通入过量二氧化碳,请写出通入过量二氧化碳反应的离子方程式是 .
(2)牙膏样品中碳酸钙的定量测定.
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.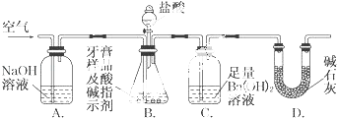
依据实验过程回答下列问题:
(i)实验过程中需持续缓缓通入空气.其作用除了可搅拌B、C中的反应物外,还有
(ii)C中反应生成BaCO3的化学方程式是
(iii)下列各项措施中,不能提高测定准确度的是(填标号).
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A~B之间增添盛有浓硫酸的洗气装置
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(iv)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g.则样品中碳酸钙的质量分数为
(v)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,就可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是 .
【答案】
(1)AlO2﹣+CO2+2H2O=Al(OH)3↓+HCO3﹣;OH﹣+CO2=HCO3﹣
(2)把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收;CO2+Ba(OH)2═BaCO3↓+H2O;cd;25%;B中的水蒸气、氯化氢气体等进入装置C中
【解析】解:(1)氢氧化铝与NaOH溶液反应生成偏铝酸钠与水,反应离子方程式为Al(OH)3+OH﹣═AlO2﹣+2H2O.
往所得滤液中先通入过量二氧化碳,发生反应AlO2﹣+CO2+2H2O=Al(OH)3↓+HCO3﹣ , OH﹣+CO2=HCO3﹣ . 所以答案是:AlO2﹣+CO2+2H2O=Al(OH)3↓+HCO3﹣ , OH﹣+CO2=HCO3﹣ . (2)(i)装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏小,持续缓缓通入空气的作用为:把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收.所以答案是:把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收.(ii)二氧化碳与氢氧化钡反应生成碳酸钡与水,反应方程式为CO2+Ba(OH)2═BaCO3↓+H2O.
所以答案是:CO2+Ba(OH)2═BaCO3↓+H2O.(iii)a、在加入盐酸之前,应排净装置内的CO2气体,防止影响碳酸钡质量的测定,可以提高测定准确度,故a不符合;
b、滴加盐酸过快CO2 , CO2来不及被吸收,就排出装置C,滴加盐酸不宜过快,使二氧化碳吸收完全,可以提高测定准确度,故b不符合;
c、在AB之间增添盛有浓硫酸的洗气装置,吸收水分,不影响CO2 , 不能提高提高测定准确度,故c符合;
d、在BC之间增添盛有饱和碳酸氢钠溶液的洗气装置,可以吸收CO2中的HCl,生成二氧化碳,使二氧化碳增加,影响CO2 , 不能提高测定准确度,故d符合.
故选:cd.(iv)BaCO3质量为3.94g,则n(BaCO3)= ![]() =0.02mol,则n(CaCO3)=0.02mol,质量为0.02mol×100g/mol=2g,所以样品中碳酸钙的质量分数为
=0.02mol,则n(CaCO3)=0.02mol,质量为0.02mol×100g/mol=2g,所以样品中碳酸钙的质量分数为 ![]() ×100%=25%.
×100%=25%.
所以答案是:25%.(v)B中的水蒸气、氯化氢气体等进入装置C中,导致测定二氧化碳的质量偏大,测定的碳酸钙的质量偏大,碳酸钙的质量分数偏高.
所以答案是:B中的水蒸气、氯化氢气体等进入装置C中.


科目:高中化学 来源: 题型:
【题目】在0.5L某NaCl溶液中含有0.5molNa+ , 对该溶液的说法不正确的是( )
A.配制100mL该溶液需用5.85g NaCl
B.该溶液的物质的量浓度为1molL ﹣1
C.该溶液中含有58.5g NaCl
D.量取100mL该溶液,其中Na+的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸( ![]() =1.84g/mL﹣1)配制成浓度为3.68mol/L﹣1的稀硫酸500mL.请按要求填空:
=1.84g/mL﹣1)配制成浓度为3.68mol/L﹣1的稀硫酸500mL.请按要求填空:
(1)所需浓硫酸的体积为mL
(2)请将下列操作按正确的序号填在横线上:
A用量筒量取浓硫酸 B反复颠倒摇匀 C用胶头滴管加水至刻度线 D洗净烧杯内壁和玻璃棒,并将洗液转至容量瓶 E稀释浓硫酸 F将溶液转入容量瓶 G向容量瓶中加入适量蒸馏水至距离刻度线1~2cm处
其操作正确顺序为 .
(3)使用容量瓶前需要先进行操作的是 ,
(4)若实验中出现下列现象对所配溶液有什么影响?(填偏高、偏低、无影响)
①浓硫酸溶解后未冷却至室温即进行定容 ,
②定容时俯视刻度线 ,
③配制前容量瓶内有水 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适当的数据填写在空格中:
(1)0.5molNaOH的质量是g,10gNaOH的物质的量是mol.
(2)在标准状况下0.5molH2的体积为L,在标况下5.6LH2的物质的量为mol.
(3)将58.5gNaCl溶于水配制成500mL溶液,此溶液中溶质的物质的量浓度为;取此溶液100mL,其中Na+的物质的量浓度为 , Na+的物质的量是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组要用0.50molL-1NaOH溶液和0.50molL-1硫酸溶液完成中和热的测定。
(l)实验桌上备有烧杯(大、小各一个)、泡沫塑料、泡沫塑料板、胶头滴管、硫酸、NaOH溶液,尚缺少的玻璃仪器是____________________________.
(2)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如下表.
①请填写如表中的空白:
试验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差 平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | _________ |
2 | 27.0 | 27.4 | 27.2 | 34.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50molL-1 NaOH溶液和0.50molL-1 硫酸的密度都是1gcm-3,中和后生成溶液的比热容c=4.18Jg-1℃-1.则中和热△H=______(取小数点后一位).
③上述实验结果数值与57.3相比有偏差,产生偏差的原因可能是(填字母)______.
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中.
(3)已知:含1mol CH3COOH的醋酸溶液与NaOH(aq)反应的ΔH=-12.1 kJ·mol-1;含1molHCl的盐酸与NaOH(aq)反应的ΔH=-55.6 kJ·mol-1。则CH3COOH在水溶液中电离的ΔH等于______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列有机反应类型的认识中,错误的是
A. ![]() ;取代反应
;取代反应
B. CH2=CH2 + Br2![]() CH2Br-CH2Br;加成反应
CH2Br-CH2Br;加成反应
C. 2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O;取代反应
2CH3CHO+2H2O;取代反应
D. CH3COOH + CH3CH2OH ![]() CH3COOCH2CH3+H2O;取代反应
CH3COOCH2CH3+H2O;取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同周期的X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是:HZO4![]() H2YO4
H2YO4 ![]() H3XO4,下列判断正确的是 ( )
H3XO4,下列判断正确的是 ( )
①阴离子的还原性按X、Y、Z顺序减弱
②单质的氧化性按X、Y、Z顺序增强
③元素的原子半径按X、Y、Z顺序减小
④气态氢化物的稳定性按X、Y、Z顺序减弱
①②A. ②③ B. ①②③ C. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①﹣⑨在表中的位置,用化学用语回答下列问题:
族 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)写出⑧的原子结构示意图 .
(2)④、⑤、⑥的原子半径由大到小的顺序为(用元素符号回答).
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(用化学式回答).
(4)②与④形成的原子个数比为1:2化合物的电子式为 .
(5)⑥的单质与①、④、⑤三种元素形成化合物的水溶液反应的离子方程式为: .
(6)②的最高价氧化物的熔沸点低于⑦的最高价氧化物的熔沸点,原因是 .
(7)⑤元素与⑨元素形成的化合物中,化学键类型为 , 高温灼烧该化合物时,火焰呈色.
(8)在②、③、⑦、⑧单质中,符合下列转化关系的是:(填元素符号).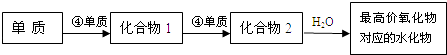
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com