
【题目】氯化亚铜(CuCl)广泛用于有机合成、气体吸收、冶金、医药化工等行业.
(1)工业上氯化亚铜可由下列反应制备:2CuSO4+Na2SO3+2NaCl+Na2CO3→2CuCl↓+3Na2SO4+CO2↑.制备过程中需要20%的CuSO4溶液,配制100g 该CuSO4溶液需要胆矾g,需要水g.
(2)实验室可用如下方法制备少量CuCl:取10mL 0.2mol/L CuCl2溶液,加入0.128g铜屑和36.5%的浓盐酸(密度为1.2g/mL)3mL,在密闭容器中加热,充分反应后,得到无色溶液A;将溶液A全部倾入水中,可得到白色的氯化亚铜沉淀.已知溶液A中只含氢离子和两种阴离子(不考虑水的电离),其中,n(H+)=0.036mol、n(Cl﹣)=0.032mol.请通过分析和计算,确定溶液A中另一阴离子的化学式和物质的量.
(3)由CO2、O2、CO、N2组成的混合气体1.008L,测得其密度为1.429g/L,将该气体依次通过足量的30%KOH溶液、氯化亚铜氨溶液(可完全吸收O2和CO)(假定每一步反应都能进行完全),使上述液体分别增加0.44g、0.44g(体积和密度均在标准状况下测定).该混合气体的摩尔质量是g/mol;混合气体中n(CO2):n(CO和N2)= .
(4)列式计算:①混合气体中CO的质量是多少?
②最后剩余气体的体积是多少?
【答案】
(1)31.25;68.75
(2)解:溶液A中只含氢离子,说明铜元素形成了络合离子,为[CuCl2]﹣,溶液呈电中性,遵循电荷守恒,n(H+)=n(Cl﹣)+n[CuCl2]﹣,n[CuCl2]﹣=4×10﹣3mol,故答案为:①[CuCl2]﹣或[Cu2Cl4]2﹣;4×10﹣3mol或2×10﹣3mol(化学式须与物质的量匹配)
(3)32;1:3
(4)①解:m=nM=28g/mol×0.01mol=0.28g,答:质量为0.28g
②解:剩余气体为氮气,体积是0.02mol×22.4L/mol,答:体积为0.448L
【解析】解:(1)20% 的CuSO4溶液含硫酸铜20g,胆矾的质量为 ![]() =31.25g,水的质量为100g﹣31.25g=68.75g,所以答案是:31.25;68.75;(3)①摩尔质量等于密度乘以气体摩尔体积,1.429g/L×22.4L/mol=32g/mol,混合气体的质量为1.429g/L×1.008L=1.4404g,1.4404g﹣0.44﹣0.44=0.5604g,n(N2)=
=31.25g,水的质量为100g﹣31.25g=68.75g,所以答案是:31.25;68.75;(3)①摩尔质量等于密度乘以气体摩尔体积,1.429g/L×22.4L/mol=32g/mol,混合气体的质量为1.429g/L×1.008L=1.4404g,1.4404g﹣0.44﹣0.44=0.5604g,n(N2)= ![]() =0.02mol, KOH溶液可吸收二氧化碳,n(CO2)=
=0.02mol, KOH溶液可吸收二氧化碳,n(CO2)= ![]() =0.01mol,混合气体的物质的量为
=0.01mol,混合气体的物质的量为 ![]() =0.045mol,n(O2和CO)=0.045mol﹣0.01mol﹣0.02mol=0.015mol,
=0.045mol,n(O2和CO)=0.045mol﹣0.01mol﹣0.02mol=0.015mol,
设CO的物质的量为x,氧气的物质的量为y.
x+y=0.015mol
28x+32y=0.44g
解得x=0.01mol,y=0.005mol
n(CO和N2)=0.01mol+0.02mol=0.03mol
n(CO2):n(CO和N2)=1:3,所以答案是:32;1:3;


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】在下面的装置中,A是实验室制备Cl2的发生装置,圆底烧瓶中盛放的是二氧化锰,C、D为气体净化装置;E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶:烧杯G为尾气吸收装置。试回答:
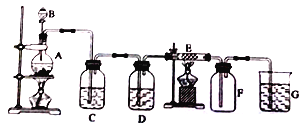
(1)C装置中试剂为______。
(2)E中的现象为______。
(3)写出在A、G中发生反应的离子方程式:A: ___________。G: ________________。
(4)KMnO4的氧化性比MnO2强得多,实验室也可以用KMnO4固体和浓盐酸反应制取氯气,反应方程式如下:2 KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①考试用“单线桥”标出电子转移的方向和数目: __________。
②该反应中被氧化和未被氧化的HCl的物质的量之比是________,如果将20mL、12mol/L的浓盐酸与足量KMnO4充分反应,实际能收集到氯气在标准状况下的体积为_______。
A.≥1.68L B.>1.68L C.≤1.68L D.<1.68L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组在某温度下测定溶液的pH时发现,0.01mol/L的NaOH溶液中,c(H+)c(OH﹣)=10﹣12(mol/L)2 , 则该小组在该温度下测得0.1mol/LNaOH溶液和0.1mol/LHCl溶液pH应为( )
A.13、1
B.13、2
C.11、1
D.10、2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量浓度的NaCl、MgCl2两种溶液的体积比为3∶2,则两种溶液中Cl-的物质的量浓度之比为( )
A. 1∶2B. 3∶4C. 1∶ 1D. 3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 物质的量即微粒的数量
B. 1 mol任何物质都含有6.02×1023个原子
C. 28g CO的体积为22.4L
D. 在同温同体积时,气体物质的物质的量越大,则压强越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时KW=1.0×10﹣14 试计算:
(1)计算室温条件下0.1mol/LHCl溶液中由水电离的氢离子浓度.
(2)计算室温条件下0.01mol/LNaOH溶液的pH.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时0.1molL﹣1 HA溶液的pH=3,0.1molL﹣1 BOH溶液中c(OH﹣):c(H+)=1012 , 将两溶液等体积混合,以下判断正确的是( )
A.c(H+)+c(HA)=c(OH﹣)
B.c(OH﹣)<c(H+)<c(B+)<c(A﹣)
C.c(H+)+c(B+)<c(A﹣)+c(OH﹣)
D.c(A﹣)=c(B+)>c(H+)=c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚酰胺66是含有肽键的高分子化合物,常用于生产帐篷、渔网等.可用以下方法合成:已知:A与E互为同分异构体,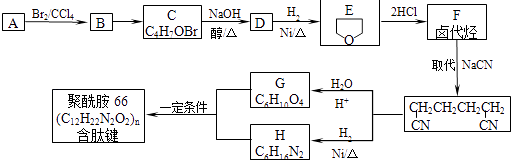
完成下列填空:
(1)A→B的反应类型 , A中含氧官能团的名称 .
(2)B的结构简式 , D可能的结构简式 .
(3)F与氢氧化钠的乙醇溶液共热得到烃I,I的名称 . 比I多一个碳原子的同系物,与等物质的量溴反应生成二溴代物的结构简式正确的是 . a. ![]()
b. ![]()
c. 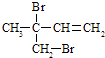
d. 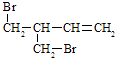
(4)G和H反应生成聚酰胺66的化学方程式: .
(5)同时满足下列条件的G的同分异构体的结构简式为 . ①含一种官能团 ②能发生银镜反应 ③含甲基且有三种化学环境不同的氢原子.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com