
【题目】已知液氨的性质与水相似,25 ℃时,NH3+NH3![]() NH4++ NH2-, NH4+的平衡浓度为1×10-15 mol·L-1,则下列说法中正确的是( )
NH4++ NH2-, NH4+的平衡浓度为1×10-15 mol·L-1,则下列说法中正确的是( )
A.在液氨中加入NaNH2可使液氨的离子积变大
B.在液氨中加入NH4Cl可使液氨的离子积减小
C.在此温度下液氨的离子积为1×10-30
D.在液氨中放入金属钠,可生成NaNH2
科目:高中化学 来源: 题型:
【题目】下列说话正确的是( )
A.构成单质分子的粒子一定含共价键
B.非金属元素组成的化合物一定不是离子化合物
C.第ⅠA族和第ⅦA族原子化合时一定形成离子键
D.共价化合物中一定不含离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲用已知物质的量浓度为0.100 0 mol·L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化,如何判断滴定终点: 。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 (填序号)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
(3)若第一次滴定开始和结束时,酸式滴定管中的液面如下图所示。则起始读数为V1= mL,终点读数V2= mL。
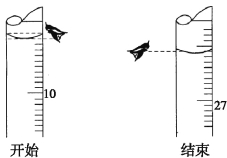
(4)再结合下表数据,计算被测氢氧化钠溶液的物质的量浓度是 mol·L-1。
滴定次数 | 待测溶液体积/mL | 标准酸体积 | |
滴定前的刻度/mL | 滴定后的刻度/mL | ||
第一次 | 10.00 | V1 | V2 |
第二次 | 10.00 | 4.10 | 21.10 |
第三次 | 10.00 | 0.40 | 17.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)在一定条件下,CH4可与NOx反应除去NOx,已知下列热化学方程式:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ·mol-1
②N2(g)+2O2(g)![]() 2NO2(g) △H=+67.0kJ·mol-1
2NO2(g) △H=+67.0kJ·mol-1
③H2O(g)=H2O(l) △H=-41.0kJ·mol-1
则CH4(g)+2NO2(g)![]() CO2(g)+2H2O(g)+N2(g) △H=_________kJ·mol-1;
CO2(g)+2H2O(g)+N2(g) △H=_________kJ·mol-1;
(2)哈伯因证实N2、H2在固体催化剂(Fe)表面吸附和解吸以合成氨的过程而获诺贝尔奖。若用![]() 分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示:
分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示:

①吸附后,能量状态最低的是 (填字母序号)。
②由上述原理,在铁表面进行NH3的分解实验,发现分解速率与浓度关系如图。
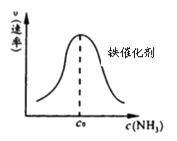
从吸附和解吸过程分析,c0前速率增加的原因可能是 ;c0后速率降低的原因可能是 。
Ⅱ.用石墨作电极电解下列溶液:
①稀H2SO4②K2SO4溶液 ③NaCl溶液 ④CuSO4溶液 ⑤KOH溶液
(1)阴极、阳极都有气体产生,其中溶液pH变大的是______________。(填序号)
(2)已知400mL 0.5 mol·L-1 CuSO4溶液,电解一段时间后,两极产生的气体体积相同,其阳极的电极反应式是_________________,两极共产生气体______________ mol,如要将溶液恢复原浓度,需要加入的物质为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
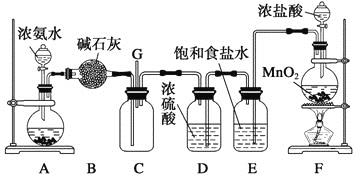
(1)装置A中的烧瓶内固体不可以选用___________________(选填序号)。
A.生石灰 B.碱石灰 C.五氧化二磷 D.烧碱
(2)装置F中发生反应的化学方程式是_____________________________________________。
(3)B装置的作用__________________;E装置的作用__________________________。
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:__________________________________________。当有a mol氯气参加反应时,转移的电子总数为b个,则阿伏加德罗数常数为_____________mol-1 (用含a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖原[(C6H10O5)n]是一种相对分子质量比淀粉更大的多糖,主要存在于肝脏中,所以又叫动物淀粉和肝糖。下列关于糖原的叙述正确的是( )
A. 糖原与淀粉、纤维素互为同分异构体 B. 糖原、淀粉、纤维素属于同系物
C. 糖原水解的最终产物是葡萄糖 D. 糖原具有还原性,能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,按要求填空(填元素符号或化学式):
族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ | ⑾ |
(1)写出元素①单质的电子式
(2)这些元素形成的气态氢化物中,最稳定的是
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是
(4)③的最高价氧化物的水化物与⑤的最高价氧化物的水化物反应的离子方程式为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com