
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | Fe2+具有还原性 | |
| ② | 在FeCl2溶液中加入锌片 | (不写) | Zn+Fe2+═Zn2++Fe | |
| ③ | 在FeCl3溶液中加入足量铁粉 | Fe+2Fe3+═3Fe2+ | Fe3+具有氧化性 | |
| ④ | (不写) | Fe3+具有氧化性 |
分析 (1)实验探究铁离子的氧化性、亚铁离子的还原性及相互转化;
①在FeCl2溶液中滴入适量氯水,生成氯化铁,Fe元素的化合价升高;
②在FeCl2溶液中加入锌片,由浅绿色变化为无色,铁元素化合价降低生成铁单质;
③在FeCl3溶液中加入足量铁粉,反应生成氯化亚铁,溶液盐酸棕黄色变化为浅绿色,FeCl3中Fe元素的化合价降低;
④证明铁离子具有氧化性,利用铁离子在硫氰酸钾溶液中生成血红色溶液,再加入铜片或铜粉后红色褪去;
(2)元素化合价可以升高也可以降低的既有氧化性,又有还原性;
(3)可加入还原性Fe粉保存亚铁盐;
(4)亚铁盐被氧化生成铁盐,铁离子遇KSCN溶液变为红色;
(5)FeCl2溶液中滴加NaOH生成Fe(OH)3,后被空气中氧气氧化为Fe(OH)3.
解答 解:(1)由实验过程及结论可知,实验目的是探究铁及其化合物的氧化性和还原性,
①在FeCl2溶液中滴入适量氯水,生成氯化铁,离子反应为:Cl2+2Fe2+=2Cl-+2Fe3+,Fe元素的化合价升高,则Fe2+具有还原性;
②在FeCl2溶液中加入锌片,由浅绿色变化为无色,铁元素化合价降低生成铁单质,Zn+Fe2+=Zn2++Fe,证明亚铁离子具有氧化性;
③在FeCl3溶液中加入足量铁粉,反应生成氯化亚铁,溶液颜色由棕黄色变化为浅绿色,反应的离子方程式为:2Fe3++Fe=3Fe2+,FeCl3中Fe元素的化合价降低,Fe3+具有氧化性;则得到实验结论为Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性,
④证明铁离子具有氧化性,可以利用铁离子在硫氰酸钾溶液中生成血红色溶液,再加入铜片或铜粉后红色褪去,说明铁离子具有氧化性氧化铜为铜离子,本身被还原为亚铁离子,反应的离子方程式为:2Fe3++Cu=2Fe2++Cu2+;
故答案为:探究铁及其化合物的氧化性和还原性;
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | Cl2+2Fe2+=2Cl-+2Fe3+ | |||
| ② | / | Fe2+具有氧化性 | ||
| ③ | 溶液颜色由棕黄色变化为浅绿色 | |||
| ④ | 在FeCl3溶液中加入硫氰酸钾溶液,然后加足量Cu | / | / |
点评 本题考查性质实验方案的设计,把握发生的氧化还原反应原理及反应中元素的化合价变化为解答的关键,侧重分析能力、实验能力及归纳能力的考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 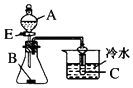 图中若A为醋酸,B为贝壳,C为苯酚钠溶液,则可验证醋酸的酸性大于碳酸,但不能验证碳酸的酸性大于苯酚 | |
| B. | 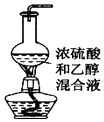 图用于实验室制乙烯 | |
| C. |  图用于实验室制乙炔并验证乙炔可以发生氧化反应 | |
| D. | 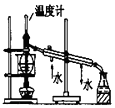 图用于实验室中分馏石油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0g重水(D2O)中含有的中子数为NA | |
| B. | 标准状况下22.4L的四氯化碳,含有四氯化碳分子数为NA | |
| C. | 23g金属钠变为钠离子时失去的电子数为NA | |
| D. | 常温常压下,48gO3和O2混合气体中含有的氧原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
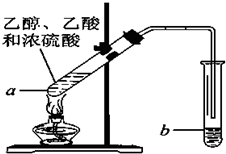 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题.
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题. ,结构简式H2C=CH2.
,结构简式H2C=CH2. ,反应类型是加聚反应.
,反应类型是加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
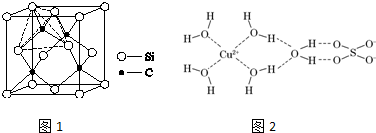
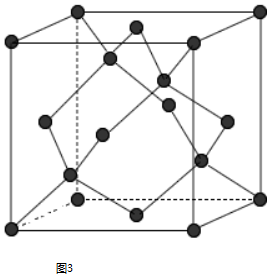
 ;亚铜离子(Cu+)基态时的电子排布式为1s22s22p63s23p63d10或[Ar]3d10.
;亚铜离子(Cu+)基态时的电子排布式为1s22s22p63s23p63d10或[Ar]3d10.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
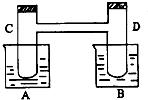 如图所示,在烧杯A中盛有20℃,50毫升水,B中盛有1摩/升盐酸50毫升,试管C、D相通,其中盛有红棕色气体,它处于下列平衡状态,2NO2?N2O4(△H<0,放热).当向A中加入50克硝酸铵使其溶解,往B中加入2克苛性钠,也使其溶解时,问:(注:硝酸铵溶于水吸热)
如图所示,在烧杯A中盛有20℃,50毫升水,B中盛有1摩/升盐酸50毫升,试管C、D相通,其中盛有红棕色气体,它处于下列平衡状态,2NO2?N2O4(△H<0,放热).当向A中加入50克硝酸铵使其溶解,往B中加入2克苛性钠,也使其溶解时,问:(注:硝酸铵溶于水吸热)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com