
【题目】回答下列问题:
(1)碳原子的核外电子排布式为____________。与碳同周期的非金属元素N的第一电离能大于O的第一电离能,原因是_________________。
(2)A、B均为短周期金属元素。依据下表数据,写出B原子的电子排布式:________。

(3)下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据。
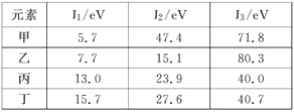
下列说法正确的是________(填字母)。
A.甲的金属性比乙强 B.乙的化合价为+1价
C.丙不可能为非金属元素 D.丁一定为金属元素
(4)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
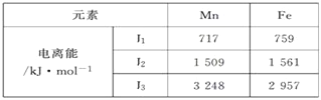
锰元素位于第四周期第ⅦB族。请写出基态Mn2+的价电子排布式:________,比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是_________________________。
【答案】 1s22s22p2 N原子的2p轨道达到半充满结构,比较稳定 1s22s22p63s2 A 3d5 由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态需要的能量相对要少
【解析】(1)碳原子的核外电子排布式为:1s22s22p2;N原子的核外电子排布式为:1s22s22p3,O原子核外电子排布式为1s22s22p4,2p轨道半充满的原子能量低,较稳定,所以与碳同周期的非金属元素N的第一电离能大于O的第一电离能;(2)从表中电离能数值来看,A、B的第三电离能出现突跃,可见它们是第ⅡA族元素,因A、B均为短周期元素,且B的第一、二电离能均比A的小,故B是镁。镁原子的电子排布式为:1s22s22p63s2;(3)甲、乙、丙、丁为第三周期元素,甲元素的第一电离能远远小于第二电离能,说明A元素最外层有1个电子,失去1个电子时达到稳定结构,所以甲为Na元素;乙元素的第二电离能远远小于第三电离能,则乙元素最外层有2个电子,失去两个电子后达到稳定结构,所以乙为Mg元素;丙、丁元素的第一电离、第二电离能、第三电离能相差不大,说明丙元素最外层大于3个电子,丙、丁一定为非金属元素。A.甲为Na元素,乙为Mg元素,故甲的金属性比乙强,选项A正确;B.乙为Mg元素,化合价为+2价,选项B错误;C、丙、丁一定为非金属元素,选项C错误;D、丙、丁一定为非金属元素,选项D错误。答案选A;(4)Mn的原子序数为25,失去2个电子变为Mn2+,则Mn2+基态的电子排布式可表示为1s22s22p63s23p63d5(或[Ar]3d5),故其价电子排布式为:3d5;由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态需要的能量相对要少,故气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难。


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】下列物质属于原子晶体的是( )
A. 熔点是1070℃,易溶于水,水溶液能导电
B. 熔点是10.31℃,液态不导电,水溶液能导电
C. 不溶于水,熔点3550℃,不导电
D. 熔点是97.80℃,质软、导电,密度是0.97gcm-3.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丁基甲酸(![]() )是有机合成中一种重要的中间体。实验室以链状分子A为原料合成环丁基甲酸的路线如下:
)是有机合成中一种重要的中间体。实验室以链状分子A为原料合成环丁基甲酸的路线如下:
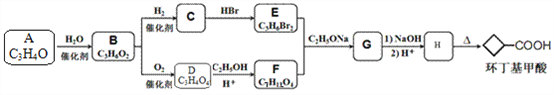
已知: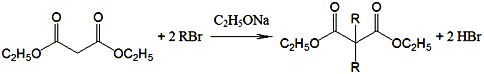
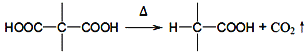
请回答下列问题:
(1)化合物A的化学名称是______,由A生成B的反应类型是_______。
(2)化合物B中所含官能团的名称为___________。
(3)化合物C和D反应所形成高聚物的结构简式是___________。
(4)写出E+F→G的化学方程式: ___________。
(5)X是环丁基甲酸的同分异构体,能与饱和碳酸氢钠溶液反应放出气体,且能使溴水褪色,X共有______种;其中核磁共振氢谱为三组峰,峰面积比为6:1:1的结构简式为___________。
(6)写出用1,3一丁二烯和化合物F为原料制备环戊基甲酸的合成路线___________。(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用如图装置进行铁与水蒸气反应的实验,并检验产物的性质,请回答下列问题:
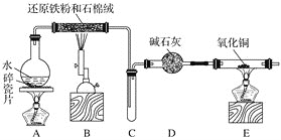
(1)A装置的作用是____________,烧瓶底部放碎瓷片的作用是_________________________。
(2)装置B中发生反应的化学方程式是____________________________________,该反应中氧化剂是__________,氧化产物是__________________。
(3)D的作用是__________________________________。
(4)E中的实验现象是____________________________。
(5)A、B两个装置中应先点燃________________处的酒精(喷)灯,点燃E处酒精灯之前应进行的操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法中正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法中正确的是( )
A. KClO3在反应中是还原剂
B. 1 mol KClO3参加反应,在标准状况下能得到22.4 L气体
C. 在反应中H2C2O4既不是氧化剂也不是还原剂
D. 1 mol KClO3参加反应有1 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有21.6 g由CO和CO2组成的混合气体,在标准状况下其体积为13.44 L。回答下列问题:
(1)该混合气体的平均摩尔质量为________。
(2)混合气体中碳原子的质量为________。

(3)将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。
①气球中收集到的气体的摩尔质量为________。
②气球的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关各实验的叙述中正确的是
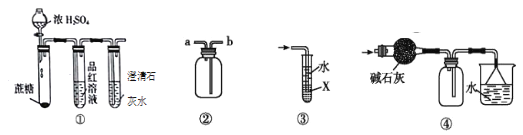
A. ①澄清石灰水变浑浊,证明蔗糖与浓硫酸反应生成了CO2
B. ②进行H2、NH3、CO2、Cl2、NO、NO2等气体的收集
C. ③当X选用苯时可进行NH3或HCl的吸收,并防止倒吸
D. ④可用于NH3的干燥,收集并吸收多余NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中少量杂质所需除杂试剂及方法不正确的是( )
物质(杂质) | 除杂试剂 | 除杂方法 | |
A | 乙醇(水) | CaO | 蒸馏 |
B | 淀粉溶液(NaCl) | ——— | 渗析 |
C | CO2(HCl) | NaOH溶液 | 洗气 |
D | NaCl溶液(I2) | CCl4 | 萃取分液 |
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com