
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
I.将NaOH 溶液与NH4Cl 溶液混合生成NH3·H2O,从而验证NaOH 的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理? 并说明理由:_____。
II.根据下图所示装置图回答以下问题。
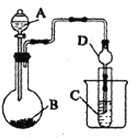
(1)利用如图装置可以验证非金属性的变化规律。图中A装置名称是_______。干燥管D的作用是___________。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫: 烧瓶中发生反应的离子方程式为_________。装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________。
(3)若要用此装置证明酸性: HNO3>H2CO3>H2SiO3进而证明非金属性: N>C>Si,从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液②稀盐酸 ③碳酸钙 ④Na2SiO3 溶液 ⑤SiO2
试剂A与C分别为______(填序号);试管中发生反应的离子方程式为________。有同学认为此实验不能说明N、C、Si的非金属性强弱,你认为原因是________。
【答案】 不合理,NH3·H2O并非为N的最高价氧化物对应的水化物 分液漏斗 防倒吸 2MnO4-+10Cl-+16H+=2Mn2++5Cl2+8H2O Cl2+S2-=S↓+2Cl- ①④ CO2+H2O+![]() ===H2SiO3+
===H2SiO3+![]() HNO3有挥发性,也会和硅酸钠反应生成硅酸
HNO3有挥发性,也会和硅酸钠反应生成硅酸
【解析】将NaOH溶液与![]() 溶液混合生成NH3·H2O,可以说明NaOH的碱性大于NH3·H2O,但不能说明Na的金属性大于N,因为要验证金属性的强弱,必须通过比较最高价氧化物所对应的水化物的碱性来进行比较,而
溶液混合生成NH3·H2O,可以说明NaOH的碱性大于NH3·H2O,但不能说明Na的金属性大于N,因为要验证金属性的强弱,必须通过比较最高价氧化物所对应的水化物的碱性来进行比较,而![]()
![]() 不是氮元素的最高价氧化物的水化物;正确答案: 不合理,NH3·H2O并非为N的最高价氧化物对应的水化物。
不是氮元素的最高价氧化物的水化物;正确答案: 不合理,NH3·H2O并非为N的最高价氧化物对应的水化物。
Ⅱ.(1) 图中A装置名称是分液漏斗;球形干燥管D能够防止倒吸,可以避免C中液体进入锥形瓶中,正确答案: 分液漏斗;防止倒吸。
(2)设计实验验证非金属性:![]() ,利用氯气与
,利用氯气与![]() 的氧化还原反应可验证,则装置A、B、C中所装药品应分别为浓盐酸、
的氧化还原反应可验证,则装置A、B、C中所装药品应分别为浓盐酸、![]() 、
、![]() 溶液,烧瓶中发生反应的离子方程式为2MnO4-+10Cl-+16H+=2Mn2++5Cl2+8H2O ;装置C中的实验现象为有淡黄色沉淀生成,装置C中发生反应的离子方程式为Cl2+S2-=S↓+2Cl-;正确答案:2MnO4-+10Cl-+16H+=2Mn2++5Cl2+8H2O ;Cl2+S2-=S↓+2Cl-。
溶液,烧瓶中发生反应的离子方程式为2MnO4-+10Cl-+16H+=2Mn2++5Cl2+8H2O ;装置C中的实验现象为有淡黄色沉淀生成,装置C中发生反应的离子方程式为Cl2+S2-=S↓+2Cl-;正确答案:2MnO4-+10Cl-+16H+=2Mn2++5Cl2+8H2O ;Cl2+S2-=S↓+2Cl-。
(3)探究元素非金属性,由图可知应是利用最高价含氧酸的酸性强弱比较,所以A中试剂为稀硝酸,B中为碳酸钙, C中为Na2SiO3溶液; 所以试剂选用①④试管中为Na2SiO3溶液中通CO2生成硅酸白色沉淀,发生反应的离子方程式为CO2+H2O+SiO32-=H2SiO3+CO32-;通入试管中的CO2气体中混有挥发性的硝酸,硝酸也能与硅酸钠溶液反应生成硅酸,无法确定CO2是否与与硅酸钠溶液反应,即不能说明N、C、Si的非金属性强弱;正确答案:①④ ;CO2+H2O+![]() ===H2SiO3+
===H2SiO3+![]() ;HNO3有挥发性,也会和硅酸钠反应生成硅酸。
;HNO3有挥发性,也会和硅酸钠反应生成硅酸。


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
【题目】已知某碱性硼化矾(VB2)﹣空气电池工作时发生反应为:11O2+4VB2═2V2O5+4B2O3 . 以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( ) 
A.VB2电极发生的电极反应为:2VB2+11H2O﹣22e﹣═V2O5+2B2O3+22H+
B.若B装置内的液体体积为400mL,则CuSO4溶液的物质的量浓度为0.025mol/L
C.电解过程中,b电极表面先有红色物质析出,然后有气泡产生
D.外电路中电子由a电极流向b电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质结构的化学用语或模型图正确的是( )
A. H2O2的电子式:![]() B. CO2的比例模型:
B. CO2的比例模型:![]()
C. 质子数与中子数相等的氢原子符号:21H D. HClO的结构式为:H-Cl-O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(BaSO4 )=1.1×10﹣10 , Ksp(BaCO3)=2.5×10﹣9 . 下列说法中正确的是( )
A.BaCO3可以转化为BaSO4 , 反过来则不行
B.BaCO3、BaSO4均不溶于水,所以都可以做钡餐试剂
C.向 Na2CO3溶液中加入BaCl2和Na2SO4 , 当两种沉淀共存时, ![]() =
= ![]()
D.常温下,BaCO3固体若要在Na2SO4溶液中开始转化为BaSO4 , 则Na2SO4的浓度须大于2.2×10﹣6mol?L﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg﹣H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液(加入一定量酸),示意图如图.该电池工作时,下列说法正确的是( ) 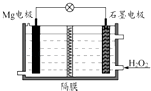
A.电池工作时,石墨周围海水的pH减少
B.电池工作时,溶液中的H+向负极移动
C.电池总反应为Mg+H2O2+2H+═Mg2++2H2O
D.Mg电极是该电池的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德常数,下列说法正确的是
A. 在同温同压时,相同体积的任何气体单质所含的原子数目相同
B. 2g氢气所含原子数目为NA
C. 在常温常压下,11.2L氮气所含的原子数目为NA
D. 17g氨气所含电子数目为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据图1中氮元素及其化合物的转化关系,回答问题:

(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为____________________。
(2)若要收集一瓶氨气,请将下列装置补充完整,在图2虚框内画出连接图。____________
(3)下列试剂可用于干燥NH3的是________________________________。
A.浓硫酸 B.碱石灰 C.CuSO4固体 D.P2O5
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO化学方程式为________________________________;
②NO→NO2实验现象是________________________________;
③将32.64g铜与l40mL一定浓度的HNO3反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。则其中NO、NO2的物质的量比为____________________。
(5)图1中在标准状况下将NO2、NO、O2混合并充满容器,将该容器倒置于水中,气体完全溶解,无气体剩余,若产物也不扩散,则所得溶液的物质的量浓度M,其数值大小范围为___________
A.0<M<l/22.4 B. 1/39.2<M<1/22.4 C.1/39.2<M<1/28 D.1/28<M<1/22.4
(6)图1中X转化为HNO3的化学方程式为:________________________________。
(7)若要将NH3→N2,从原理上看,下列试剂可行的是_______________。
A.O2 B.Na C.NH4Cl D. NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把Ba(OH)2溶液滴入明矾[KAl(SO4)2·12H2O]溶液中,使SO42-全部转化成BaSO4沉淀,此时铝元素的主要存在形式是( )
A. Al3+ B. AlO2- C. Al(OH)3 D. Al3+和Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水解方程式的书写中,正确的是( )
A.CH3COO﹣的水解方程式:CH3COO﹣+H2O?CH3COOH+OH﹣
B.HCO3﹣的水解方程式:HCO ![]() +H2O?CO
+H2O?CO ![]() +H3O+
+H3O+
C.CO ![]() 的水解方程式:CO
的水解方程式:CO ![]() ?+2H2O?H2CO3+2OH﹣
?+2H2O?H2CO3+2OH﹣
D.Fe3+的水解方程式:Fe3++3OH﹣?Fe(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com