
【题目】2015年10月,中国的女科学家屠呦呦获得诺贝尔生理学或医学奖,理由是她发现了青蒿素,这种药品可以有效降低疟疾患者的死亡率.青蒿素的化学式为C15H22O5 , 易溶于丙酮、乙醚等有机溶剂,故提取青蒿素的方法之一为乙醚浸取法.提取粗品的主要工艺为:
回答下列问题
(1)操作Ⅰ的分离方法是 , 操作Ⅱ的分离方法是 .
(2)青蒿素的摩尔质量为 , 其中碳氧原子的质量比为 .
【答案】
(1)过滤;蒸馏
(2)282g/mol;9:4
【解析】解:(1)操作Ⅰ用于分离固体和液体,则可用过滤的方法分离,而操作Ⅱ用于分离乙醚,可用蒸馏的方法,故答案为:过滤;蒸馏;(2)摩尔质量的单位是g/mol,青蒿素C15H22O5的相对分子质量=(12×15)+(1×22)+(16×5)=282,其摩尔质量为282g/mol,由分子式C15H22O5可知,碳氧原子的质量比为15×12:5×16=9:4,故答案为:282g/mol;9:4.
(1)操作Ⅰ用于分离固体和液体,而操作Ⅱ用于分离乙醚,可用蒸馏的方法;(2)摩尔质量在数值上等于相对分子质量,由分子式C15H22O5可知,碳氧原子的质量比为15×12:5×16.


科目:高中化学 来源: 题型:
【题目】无水氯化铝是一种重要的化工原料,工业上利用明矾石制备无水氯化铝的流程如图,请回答下列问题: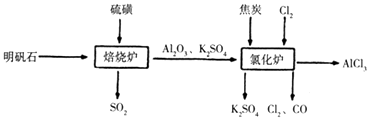
(1)实验室中,可制得Cl2的组合是(填代号).
①MnO2和浓盐酸混合共热 ②MnO2、NaCl和浓硫酸混合共热
③NaClO和盐酸混合共热 ④漂白粉和硫酸混合共热
(2)吸收焙烧炉中产生的尾气,下列装置合理的是(填代号).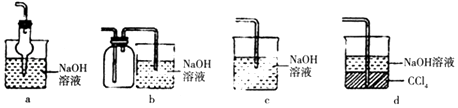
(3)写出氧化炉中反应的化学方程式
(4)生产氯化铝的过程中焙烧炉和氯化炉中产生的SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少污染.试设计简单实验检验二者是否恰好完全反应,简要描述实验步骤、现象和结论(仪器自选).
可供选择试剂如下:
①滴加酚酞的氢氧化钠溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
(5)某同学设计用如图装置验证二氧化硫的某些化学性质.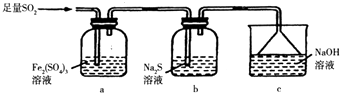
①能说明二氧化硫具有氧化性的实验现象为 .
②写出a瓶中发生反应的离子方程式 .
③充分反应后,取a瓶中的溶液分成三份,分别进行如下实验.
实验I:向第一份溶液中加入足量的NaOH溶液,生成白色沉淀,迅速变为灰绿色,最终变为红褐色.
实验II:向第二份溶液中加入少量KMnO4溶液,紫色褪去.
实验III:向第三份溶液中加入BaCl2溶液,生成白色沉淀.
上述实验中能充分证明二氧化硫具有还原性的是:(填实验代号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子反应可用H++OH﹣=H2O表示的是( )
A.Cu(OH)2与H2SO4
B.Ba(OH)2与H2SO4
C.Fe(OH)3与HCl
D.HNO3与KOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不计).其中能表示等质量的氢气与氦气的是( )
A.
B.
C.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可用于合成除草剂、杀草丹等农药。H2S与CO2在高温下反应可制得COS: H2S(g)+CO2(g)![]() COS(g) +H2O(g) △H > 0。在 2 L 容器中充入一定量的H2S和CO2发生上述反应,数据如下:
COS(g) +H2O(g) △H > 0。在 2 L 容器中充入一定量的H2S和CO2发生上述反应,数据如下:

下列判断不正确的是( )
A. K1=l/81
B. 实验2中平衡时的c(COS)约为0.0286 mol·L-1
C. 初始反应速率:实验3 >实验2 >实验1
D. K2=K3 且n3=2n2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中微粒浓度关系一定正确的是( )
A.室温下,氨水与氯化铵的pH=7的混合溶液中:c(Cl﹣)=c(NH4+)
B.向NaHCO3溶液中加入少量NaOH固体,可抑制HCO3﹣的水解,使c(HCO3﹣)增大
C.0.1 molL﹣1的(NH4)2SO4溶液中:c(NH4+)>c(SO42﹣)>c(H+)>c(OH﹣)
D.常温下,等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,a+b=14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中.从废料中回收氧化钴(CoO)的工艺流程如下: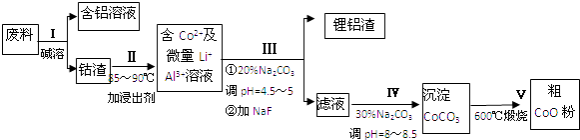
(1)为了提高废料溶浸的效率,可以采取的措施有(写一条即可)
(2)过程Ⅰ中采用NaOH溶液溶出废料中的Al,反应的离子方程式为 .
(3)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴.则浸出钴的化学反应方程式为(产物中只有一种酸根) . 在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请从反应原理分析不用盐酸浸出钴的主要原因 .
(4)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3 , 请写出产生Al(OH)3反应的离子方程式 .
(5)碳酸钠溶液在过程Ⅲ和IV中所起作用有所不同,请写出在过程Ⅳ中起的作用是 .
(6)实验室模拟生产过程V中,必须使用的仪器,除酒精灯、三脚架外,还需、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2 , 再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题: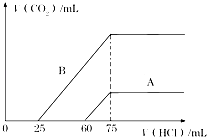
(1)原NaOH溶液的物质的量浓度为 .
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是 , 其物质的量之比为 .
(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为mL.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com