
【题目】三氯化六氨合钴(Ⅲ)是一种重要的配合物原料,实验室制备实验流程如下:
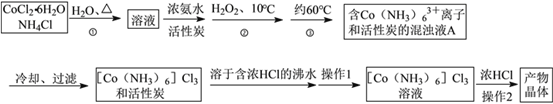
已知:[Co(NH3)6]Cl3在水中电离为[Co(NH3)6]3+和Cl-,[Co(NH3)6]Cl3的溶解度如下表:
温度(℃) | 0 | 20 | 47 |
溶解度(g) | 4.26 | 6.96 | 12.74 |
(1)第①步需在煮沸NH4Cl溶液中加入研细的CoCl2·6H2O晶体,加热煮沸与研细的目的是__
(2)实验室制备三氯化六氨合钴(III)的化学方程式为:____________
(3)实验操作1为 _________[Co(NH3)6]Cl3溶液中加入浓盐酸的目的是_____
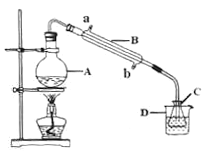
(4)现称取0.2675g[Co(NH3)6]Cl3(相对分子质量为267.5),在A中发生如下反应:[Co(NH3)6]Cl3+3NaOH![]() Co(OH)3↓+6NH3↑+3NaCl(装置见右下图),C中装0.5000mol·L-1的盐酸25.00mL,D中装有冰水。加热烧瓶,使NH3完全逸出后,用少量蒸馏水冲洗导管下端外壁上粘附的酸液于C中,加入2-3滴甲基红指示剂,用0.5000mol·L-1的NaOH滴定。
Co(OH)3↓+6NH3↑+3NaCl(装置见右下图),C中装0.5000mol·L-1的盐酸25.00mL,D中装有冰水。加热烧瓶,使NH3完全逸出后,用少量蒸馏水冲洗导管下端外壁上粘附的酸液于C中,加入2-3滴甲基红指示剂,用0.5000mol·L-1的NaOH滴定。
已知: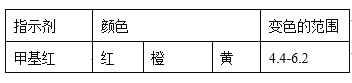
①当滴定到终点时,共需消耗NaOH溶液___mL(准确到0.01mL)。
②当用上述原理测定某[Co(NH3)x]Cl3晶体中x值,实验过程中未用少量蒸馏水冲洗导管下端内外壁上粘附的酸液于C中,则x值将______(填“偏大”、“偏小”或“不变”)
【答案】 加速固体的溶解 实验室制备三氯化六氨合钴(III)的化学方程式为:2CoCl2·6H2O + 10NH3+ 2NH4Cl + H2O2 ![]() 2[Co(NH3)6]Cl3+14H2O 趁热过滤 有利于[Co(NH3)x]Cl3析出,提高产率 13.00 偏大
2[Co(NH3)6]Cl3+14H2O 趁热过滤 有利于[Co(NH3)x]Cl3析出,提高产率 13.00 偏大
【解析】(1)第①步需在煮沸NH4Cl溶液中加入研细的CoCl2·6H2O晶体,加热煮沸与研细的目的是加速固体的溶解;(2)实验室制备三氯化六氨合钴(III)的化学方程式为:2CoCl2·6H2O + 10NH3+ 2NH4Cl + H2O2 ![]() 2[Co(NH3)6]Cl3+14H2O ;(3)流程图提供的信息可知,实验操作Ⅰ为趁热过滤;[Co(NH3)6]Cl3溶液中加入浓盐酸的目的是:[Co(NH3)6]Cl3 溶液中加入浓HCl增大氯离子浓度,依据沉淀溶解平衡理论,平衡向析出晶体的方向移动,所以加入浓盐酸的目的是有利于[Co(NH3)6]Cl3析出,提高产率;(4)0.2675g[Co(NH3)6]Cl3(相对分子质量为267.5),物质的量=0.2675g/267.5g·mol-1=0.001mol,滴定过程分析发生的反应依次为[Co(NH3)6]Cl3+3NaOH═Co(OH)3↓+6NH3↑+3NaCl,NH3+HCl=NH4Cl,HCl+NaOH=NaCl+H2O,放出氨气物质的量总计为0.006mol,消耗HCl物质的量0.006mol,HCl总物质的量=0.0250L×0.5mol·L-1=0.0125mol,所以消耗剩余HCl需要氢氧化钠物质的量=0.0125mol-0.006mol=0.0065mol,当滴定到终点时,共消耗NaOH溶液的体积=0.0065mol/0.5mol·L-1=0.0013L=13.00ml;②当用上述原理测定某[Co(NH3)x]Cl3晶体中x值,实验过程中未用少量蒸馏水冲洗导管下端内外壁上粘附的酸液于C中,导致酸液减少,消耗氢氧化钠的量减少,测定氨气量增多,x值将偏大。
2[Co(NH3)6]Cl3+14H2O ;(3)流程图提供的信息可知,实验操作Ⅰ为趁热过滤;[Co(NH3)6]Cl3溶液中加入浓盐酸的目的是:[Co(NH3)6]Cl3 溶液中加入浓HCl增大氯离子浓度,依据沉淀溶解平衡理论,平衡向析出晶体的方向移动,所以加入浓盐酸的目的是有利于[Co(NH3)6]Cl3析出,提高产率;(4)0.2675g[Co(NH3)6]Cl3(相对分子质量为267.5),物质的量=0.2675g/267.5g·mol-1=0.001mol,滴定过程分析发生的反应依次为[Co(NH3)6]Cl3+3NaOH═Co(OH)3↓+6NH3↑+3NaCl,NH3+HCl=NH4Cl,HCl+NaOH=NaCl+H2O,放出氨气物质的量总计为0.006mol,消耗HCl物质的量0.006mol,HCl总物质的量=0.0250L×0.5mol·L-1=0.0125mol,所以消耗剩余HCl需要氢氧化钠物质的量=0.0125mol-0.006mol=0.0065mol,当滴定到终点时,共消耗NaOH溶液的体积=0.0065mol/0.5mol·L-1=0.0013L=13.00ml;②当用上述原理测定某[Co(NH3)x]Cl3晶体中x值,实验过程中未用少量蒸馏水冲洗导管下端内外壁上粘附的酸液于C中,导致酸液减少,消耗氢氧化钠的量减少,测定氨气量增多,x值将偏大。


科目:高中化学 来源: 题型:
【题目】下列各组物质互为同系物的是
A. O2和O3 B. CH3CH2CH2CH3和CH(CH3)3
C. 12C和13C D. CH3和CH3CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面有关晶体的叙述中,不正确的是 ( )
A. 氯化铯晶体中,每个Cs+周围紧邻8个Cl-
B. 金刚石为网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子
C. 金属铜属于六方最密堆积结构,金属镁属于面心立方最密堆积结构
D. 干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分:

(1)元素⑩原子结构示意图为__________.
(2)元素③④的第一电离能大小关系为_______(填化学用语,下同),原因是__________________。④-⑧中最高价氧化物对应水化物酸性最强的是_______.
(3)写出元素⑦的最高价氧化物与NaOH溶液反应的离子方程式_________。
(4)元素⑤ 与⑧ 元素相比,非金属性较强的是__________(用元素符号表示),下列表述中能证明这一事实的是__________。
A.气态氢化物的挥发性和稳定性
B.两元素的电负性
C.单质分子中的键能
D.含氧酸的酸性
E.氢化物中X—H键的键长
F.两单质在自然界中的存在形式
(5)根据下列五种元素的第一至第四电离能数据(单位:KJ·mol﹣1),回答下面各题:
元素代号 | I1 | I2 | I3 | I4 |
Q | 2080 | 4000 | 6100 | 9400 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
U | 420 | 3100 | 4400 | 5900 |
①T元素最可能是________(填“s”、“p”、“d”、“ds”等)区元素;
在周期表中,最可能处于同一主族的是_________.(填元素代号),
②下列离子的氧化性最弱的是______________。
A.S2+ B.R2+ C.U+ D.T3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2K2CrO4+H2SO4![]() K2Cr2O7+K2SO4+H2O
K2Cr2O7+K2SO4+H2O
②K2Cr2O7+6FeSO4+7H2SO4![]() 3Fe2(SO4)3+ Cr2(SO4)3 +K2SO4+7H2O
3Fe2(SO4)3+ Cr2(SO4)3 +K2SO4+7H2O
③Fe2(SO4)3+2HI![]() 2FeSO4+I2+H2SO4
2FeSO4+I2+H2SO4
下列结论正确的是
A. ①②③均是氧化还原反应
B. 氧化性强弱顺序是K2Cr2O7>Fe2(SO4)3>I2
C. 反应②中氧化剂与还原剂的物质的量之比为6∶1
D. 反应③中0.1 mol还原剂共失去电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的是
A. 标准状况下,22.4 L H2O 的分子数为 NA
B. 1 mol NH4+ 所含质子数为10NA
C. 物质的量浓度为0.5mol·L-1 的 MgCl2 溶液,含有的 Cl-数为 NA
D. 常温常压下,32g O2和O3的混合气体所含原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加快的是( )
A.加热
B.将稀硫酸改成98%的浓硫酸
C.滴加少量CuSO4溶液
D.不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
已知:①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A的化学名称为_______。
(2)B的结构简式为______,其核磁共振氢谱显示为______组峰,峰面积比为______。
(3)C中官能团的名称为:_______。
(4)由C生成D的化学方程式:___________________________________。
(5)由C生成E的化学方程式:___________________________________。
(6)已知F是A的同系物,F的相对分子质量比A多28,则与F互为同分异构体且能发生银镜反应的结构种类有_____________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅有一种原子轨道,也是宇宙中最丰富的元素,B元素原子的核外p轨道电子数比s轨道电子数少1,C为金属元素且原子核外p轨道电子数和s轨道电子数相等,D元素的原子核外所有p轨道全充满或半充满。
(1)写出四种元素的元素符号:A_______,B_______,C_______,D_______。
(2)写出C、D两种基态原子核外电子排布图:
C________________________________________________________________________;
D________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com