
 氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.| 氖 | 氧 | 溴 | 碘 | |
| 第一电离能 (Kj/mol) | 1681 | 1251 | 1140 | 1008 |
| 4+2 |
| 2 |
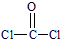 ,据此判断分子空间构型,溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子,据此写出价电子排布式;
,据此判断分子空间构型,溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子,据此写出价电子排布式;
| ||
| 2 |
| 4+2 |
| 2 |
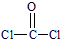 ,所以它的空间构型为平面三角形,溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子,其价电子排布式为4s24p5,
,所以它的空间构型为平面三角形,溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子,其价电子排布式为4s24p5,| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 4 |
| ||
| a3 |
| 3 |
| ||
| ||
| 2 |
| ||
| 2 |
| 3 |
| ||
| ||
| 2 |
| 3 |
| ||


科目:高中化学 来源: 题型:
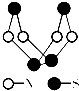 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.如图是已经合成的最著名的
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.如图是已经合成的最著名的| A、该物质的分子式为SN |
| B、该物质的分子中既有极性键又有非极性键 |
| C、该物质可能是离子化合物 |
| D、该物质的一个分子中含有9个N-S键 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硅是一种亲氧元素,在自然界中大多以氧化物和硅酸盐的形式存在 |
| B、硅在地壳中的含量居第一位 |
| C、利用硅的半导体性能,可以制作光电池 |
| D、硅晶体的结构与金刚石类似 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、85 | B、24 | C、39 | D、7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡含有食品添加剂的食物对人体健康均有害,不可食用 |
| B、提倡人们购物时不用塑料袋,是为了防止白色污染 |
| C、防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
| D、利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
| B、能使湿润的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| C、SiO2与酸、碱均不反应 |
| D、分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com