
| A、2Na2O2+2CO2═2Na2CO3+O2↑ |
| B、2Na2O2+2SO3═2Na2SO4+O2↑ |
| C、Na2O2+H2SO4═Na2SO4+H2O2 |
| D、3Na2O2+Cr2O3═2Na2CrO4+Na2O |


 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、通入标准状况下的HCl气体22.4V L |
| B、将溶液加热浓缩到0.5V L |
| C、加入10.00 mol?L-1的盐酸0.2V L,再稀释至1.5V L |
| D、加入V L 3 mol?L-1的盐酸混合均匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属阳离子一定只具有氧化性 |
| B、金属单质作反应物时一定不是氧化剂 |
| C、氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原 |
| D、氧化还原反应中的反应物,不是氧化剂就是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、该反应是置换反应 |
| B、该反应是复分解反应 |
| C、CO是氧化剂 |
| D、NO发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
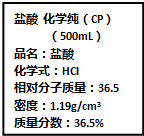 按要求完成下列小题.
按要求完成下列小题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由130 56Ba 可推断其原子核外电子排布及元素的相对原子质量 |
| B、通过化学变化无法实现16O2与18O2间的相互转化 |
| C、Ca(HCO3)2、Fe(OH)3、FeCl2均可通过化合反应制得 |
| D、等物质的量KMnO4和MnO2分别与足量的浓盐酸反应,前者生成氯气体积大(标况) |
查看答案和解析>>
科目:高中化学 来源: 题型:
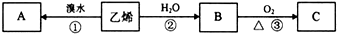
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com