
【题目】已知阿伏加德罗常数的值为NA,根据所学知识填空。
(1)3molH2O含有__个H2O;
(2)含0.4molAl3+的Al2(SO4)3中所含的SO42-的质量是__g;
(3)已知NH3的相对分子质量为17,则NH3的摩尔质量为__g/mol;
(4)若某原子的摩尔质量为Mg·mol-1,则一个该原子的真实质量是___g;
(5)CO2中含有6.02×1023个O,则CO2的物质的量为__mol;
(6)6.02×1022个OH-的电子物质的量为___mol。
(7)已知一个铁原子的质量为bg,则铁的摩尔质量为___g/mol。
【答案】3NA 57.6 17 ![]() 0.5 1 bNA
0.5 1 bNA
【解析】
(1)3molH2O中含有3NA个H2O;
(2)Al2(SO4)3中n(Al3+):n(SO42-)=2:3,故n(SO42-)=![]() n(Al3+)=
n(Al3+)=![]() ×0.4mol=0.6mol,m(SO42-)=96g·mol-1×0.6mol=57.6g,含0.4molAl3+的Al2(SO4)3中所含的SO42-的质量是57.6g;
×0.4mol=0.6mol,m(SO42-)=96g·mol-1×0.6mol=57.6g,含0.4molAl3+的Al2(SO4)3中所含的SO42-的质量是57.6g;
(3)NH3的相对分子质量为17,NH3的摩尔质量以g/mol单位时,数值上与相对分子质量相等,NH3的摩尔质量为17g/mol;
(4)若某原子的摩尔质量为Mg·mol-1,则一个该原子的真实质量是Mg·mol-1÷NAmol-1=![]() g;
g;
(5)CO2中含有6.02×1023个O,n(O)=1mol,则CO2的物质的量为1mol÷2=0.5mol;
(6)6.02×1022个OH-,n(OH-)=6.02×1022÷(6.02×1023)mol-1=0.1mol,每个OH-含有10个电子,6.02×1022个OH-电子物质的量为1mol。
(7)已知一个铁原子的质量为bg,则铁的摩尔质量为bg×NAmol-1=bNAg/mol。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】“对氨基苯甲酸丁酯”是防晒霜中能吸收紫外线的防晒剂。下列关于“对氨基苯甲酸丁酯”的说法正确的是( )
A. 从有机物分类看,它可属于“氨基酸类”“酯类”“芳香烃类”
B. 它能与盐酸反应,但不能与苛性钠溶液反应
C. 甲酸丁酯基(—COOC4H9)有3种不同结构
D. 它的分子式为C11H15NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用VSEPR模型预测下列分子或离子的立体结构,其中正确的是 ( )
A. H2O与BeCl2为角形(V形) B. CS2与SO2为直线形
C. SO3与CO![]() 为平面三角形 D. BF3与PCl3为三角锥形
为平面三角形 D. BF3与PCl3为三角锥形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示,单位为kJ·mol-1)

下列关于元素R的判断中一定正确的是( )
A. R的最高正价为+3价
B. R元素位于元素周期表中第ⅡA族
C. R元素的原子最外层共有4个电子
D. R元素基态原子的电子排布式为1s22s2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和钴是两种重要的过渡元素。请回答下列问题:
(1)钴在元素周期表中的位置是___________,其基态原子的价电子排布图为___________。
(2)FeCO3是菱铁矿的主要成分,其中C原子的杂化方式为________;分子中的大π键可用符号Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π![]() ),则CO32-中的大π键应表示为________。
),则CO32-中的大π键应表示为________。
(3)已知Fe2+半径为61pm,Co2+半径为65pm,在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3受热分解温度低于CoCO3,其原因可能是______。
(4)Co(NH3)5Cl3是钴的一种配合物,向含0.01mol该配合物的溶液中加入足量AgNO3溶液,生成白色沉淀2.87g。则该配合物的配位数为_____。
(5)奥氏体是碳溶解在r-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构(如图所示),则该晶体中与铁原子距离最近的铁原子数目为___________;若该晶胞参数为a pm,则该晶体的密度为___________g·cm-3(阿伏加德罗常数的值用NA表示)。
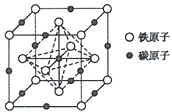
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu3N具有良好的电学和光学性能,在电子工业领城、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的作用。
(1)Cu+的核外电子排布式为__________;N元素与O元素的第一电离能比较:N____O(填“>”、“<”或“=”)。
(2)与N3-含有相同电子数的四原子分子的空间构型为____________________。
(3)在Cu催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中醛其(![]() )碳原子的杂化方式为_________。
)碳原子的杂化方式为_________。
(4)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被C1-取代可生成Cu(H2O)2Cl2,试画出其具有极性的分子的结构式________________。
(5)Cu3N的晶胞结构如图所示,N3-的配位数为________;若晶胞棱长为anm,NA表示阿伏加德罗常数的值,则Cu3N的密度p=______g/cm3 [用含a 和NA 的式子表示,Mr(Cu3N)=206]

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是
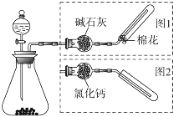
选项 | 发生装置中的药品 | 干燥和集气装置 |
A | 电石和饱和食盐水 | 图2 |
B | 大理石和稀盐酸 | 图1 |
C | 铜和稀硝酸 | 图2 |
D | 氧化钙和浓氨水 | 图1 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过以下反应可获得新型能源二甲醚(![]() )。下列说法不正确的是
)。下列说法不正确的是
①![]()
![]()
②![]()
![]()
③![]()
![]()
④![]()
![]()
A. 反应①、②为反应③提供原料气
B. 反应③也是![]() 资源化利用的方法之一
资源化利用的方法之一
C. 反应![]() 的
的![]()
D. 反应![]() 的
的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对溴苯乙烯与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点。完成下列填空:
(1)写出该共聚物的结构简式____________。
(2)实验室由乙苯制取对溴苯乙烯,需先经两步反应制得中间体![]() ,写出该两步反应所需的试剂及条件____________。
,写出该两步反应所需的试剂及条件____________。
(3)将![]() 与足量氢氧化钠溶液共热得到A,A在酸性条件下遇FeCl3溶液不显色。A的结构简式为____________。由上述反应可推知____________。由A生成对溴苯乙烯的反应条件为____________。
与足量氢氧化钠溶液共热得到A,A在酸性条件下遇FeCl3溶液不显色。A的结构简式为____________。由上述反应可推知____________。由A生成对溴苯乙烯的反应条件为____________。
(4)丙烯催化二聚得到2,3-二甲基-1-丁烯,B与2,3-二甲基-1-丁烯互为同分异构体,且所有碳原子处于同一平面。
写出B的结构简式____________。
设计一条由2,3-二甲基-1-丁烯制备B的合成路线____________。(合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com