
【题目】Cu3N具有良好的电学和光学性能,在电子工业领城、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的作用。
(1)Cu+的核外电子排布式为__________;N元素与O元素的第一电离能比较:N____O(填“>”、“<”或“=”)。
(2)与N3-含有相同电子数的四原子分子的空间构型为____________________。
(3)在Cu催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中醛其(![]() )碳原子的杂化方式为_________。
)碳原子的杂化方式为_________。
(4)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被C1-取代可生成Cu(H2O)2Cl2,试画出其具有极性的分子的结构式________________。
(5)Cu3N的晶胞结构如图所示,N3-的配位数为________;若晶胞棱长为anm,NA表示阿伏加德罗常数的值,则Cu3N的密度p=______g/cm3 [用含a 和NA 的式子表示,Mr(Cu3N)=206]

【答案】 [Ar]3d10或1s22s22p63s23p63d10 > 三角锥形 sp2 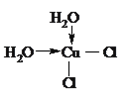 6
6 ![]()
【解析】(1)Cu原子序数为29,Cu+的核外有28个电子,根据构造原理,核外电子排布式为1s22s22p63s23p63d10;同周期从左向右第一电离能呈增大趋势,但N元素原子的2p能级有3个电子,处于半充满稳定状态,第一电离能高于同周期相邻元素,故第一电离能N>O。
(2)与N3-含有相同电子数的四原子分子为NH3,NH3中N原子形成3个σ键,有一对未成键的孤对电子,杂化轨道数为4,采取sp3型杂化,孤对电子对成键电子的排斥作用较强,N-H之间的键角小于109°28′,所以氨气分子空间构型是三角锥形。
(3)乙醛分子中醛基上的碳原子含有3个σ键和1个π键,无孤对电子,采用sp2杂化。
(4)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被C1-取代可生成Cu(H2O)2Cl2,有两种不同的结构,其具有极性的分子结构不对称,故结构式为: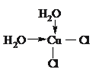 。
。
(5)Cu3N的晶胞结构如图,Cu+个数=12×![]() =3,N3-=8×
=3,N3-=8×![]() =1,所以N3-的配位数=3×2=6,晶胞体积=(a nm)3=(a×10-7 cm)3,晶胞质量=
=1,所以N3-的配位数=3×2=6,晶胞体积=(a nm)3=(a×10-7 cm)3,晶胞质量=![]() g,Cu3N的密度p=
g,Cu3N的密度p=![]() g÷(a×10-7 cm)3=
g÷(a×10-7 cm)3=![]() g/cm3。
g/cm3。


科目:高中化学 来源: 题型:
【题目】已知:Ksp(ZnS)=2.0×1022,Ksp(CuS)=1.3×1036,向等物质的量浓度ZnSO4和CuSO4的混合溶液中,逐滴加入1.5 mol·L1的Na2S溶液直至溶液中无沉淀产生,然后过滤。下列说法不正确的是
A. 先生成CuS后生成ZnS沉淀,属于沉淀的转化
B. 当ZnS沉淀完全时,溶液中![]() =6.5×1015
=6.5×1015
C. 过滤得到的沉淀是CuS和ZnS的混合物
D. 过滤后得到的溶液中仍有极少量的Cu2+和Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解饱和硫酸铜溶液,装置由右图所示,则直流电源左端为______极(填“正”或“负”),b电极的电极反应式为:_______________;电解一段时间后,电解质溶液的pH_______(填“变大”、“变小”或“不变”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室只有36.5%(d=1.19)的浓盐酸,现需配制100 mL 10%(d=1.08)的盐酸,需36.5%的浓盐酸________mL。在配制过程中,用到的仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要______。定容时,如果眼睛仰视刻线,配制的溶液的浓度将__________(填“偏高”“偏低”或“无影响”),10%的盐酸逐滴加入到纯碱溶液中,反应的离子方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g) ![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
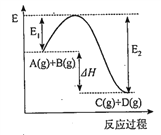
(1)该反应是___________反应(填“吸热”或“放热”)。
(2)△H=_______________。
(3)反应体系中加入催化剂对反应热是否有影响?___________________(填“有影响”“无影响”)。
(4)升高温度,该反应的平衡常数K将_________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁和铝分别与等浓度、等体积的足量稀硫酸反应,相同条件下产生气体的体积(V)与时间(t)关系如图。反应中镁和铝的( )

A. 物质的量之比为3:2 B. 质量之比为3:2
C. 转移电子数之比为3:2 D. 气体的体积之比为2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向沸水中滴加几滴饱和氯化铁溶液并继续煮沸至溶液呈红褐色时停止加热,此时当一束平行光线通过该红褐色液体时,从侧面可观察到一条光亮的“通路”。说明该红褐色液体是( )
A. 溶液 B. 胶体 C. 悬浊液 D. 乳浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,体积均为20 mL、浓度均为0.1mol/L的两种酸HX、HY分别与0.1mol/L的NaOH溶液反应,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是

A. 加入10 mL NaOH溶液时,a点c(X-)<b点c(Y-)
B. b点溶液中,c(Y-)+2c(OH-)=c(HY)+2c(H+)
C. HY中加NaOH溶液至pH=7 时,所得溶液中c(Y-)=c(Na+)=c(OH-)=c(H+)
D. 25℃时,HX为强酸,HY为弱酸且Kb=10-8
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com