
【题目】Q、X、Y、Z、W五种元素的原子序数依次递增,W为第四周期元素,其余均为短周期主族元素。已知:
①Q原子的最外层电子数是次外层电子数的2倍;
②Y、Z同主族,Y原子价电子排布图为![]()
③W元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。
请回答下列问题:
(1)W的元素名称为________,其基态原子的电子排布式为_________。
(2)具有相同价电子数和相同原子数的分子或离子具有相同的结构特征,这一原理称为“等电子原理”,五种元素中电负性最强的非金属元素形成的一种单质A与Y、Z形成的化合物B是等电子体物质,A、B分子式分别为____________、____________。
(3)Q、X、Y三种元素的第一电离能最大的是_______(填元素符号)。
【答案】铜元素 1s22s22p63s23p63d104s1(或[Ar]3d104s1) O3 SO2 N
【解析】
Q、X、Y、Z、W五种元素的原子序数依次递增,W为第四周期元素,其余均为短周期主族元素,Q原子的最外层电子数是次外层电子数的2倍,则Q的电子层结构为2,4,Q为C元素;Y原子价电子排布图为![]() ,则Y为O元素,Y、Z同主族,则Z为S元素;X位于C和O之间,则X为N元素;W元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,则其核外电子排布为1s22s22p63s23p63d104s1,为Cu元素。
,则Y为O元素,Y、Z同主族,则Z为S元素;X位于C和O之间,则X为N元素;W元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,则其核外电子排布为1s22s22p63s23p63d104s1,为Cu元素。
(1)根据分析可知W为铜元素,基态铜原子的核外电子排布为1s22s22p63s23p63d104s1(或[Ar]3d104s1);
(2)非金属性越强,电负性越强,五种元素中非金属性最强的是O元素,所以O元素的电负性最强,O元素可以形成单质O2和O3,O元素和S元素可以形成化合物SO2和SO3,其中O3和SO2为等电子体,所以A为O3,B为SO2;
(3)Q、X、Y分别为C、N、O,三种元素位于同一周期,同周期自左至右第一电离能呈增大的趋势,虽然O比N位置靠右,但N原子最高能级电子为半满状态,更稳定,所以其第一电离能大于O,所以三种元素中第一电离能最大的是N。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】工业上可用甲苯合成苯甲醛(苯甲醛),下列说法正确的是( )
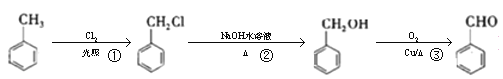
A.![]() 可以作为萃取剂萃取溴水中的溴单质
可以作为萃取剂萃取溴水中的溴单质
B.反应①②③的反应类型相同
C.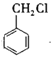 的同分异构体有3种
的同分异构体有3种
D. 和
和![]() 可以通过酸性高锰酸钾鉴别
可以通过酸性高锰酸钾鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以苯、乙烯和乙炔为原料合成化工原料G的流程如下:
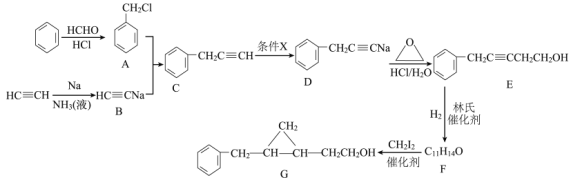
(1)A的名称__,条件X为__;
(2)D→E的化学方程式为__,E→F的反应类型为__。
(3)实验室制备乙炔时,用饱和食盐水代替水的目的是__,以乙烯为原料原子利率为100%的合成![]() 的化学方程式为__。
的化学方程式为__。
(4)F的结构简式为___。
(5)写出符合下列条件的G的同分异构体的结构简式__。
①与G具有相同官能团的芳香族类化合物;②有两个通过C-C相连的六元环;
③核磁共振氢谱有8种吸收峰;
(6)参照上述合成路线,设计一条以1,2二氯丙烷和二碘甲烷及必要试剂合成甲基环丙烷的路线:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁氧体是一种磁性材料,具有广泛的应用。
(1)基态铁原子的核外电子排布式为________。
(2)工业制备铁氧体常使用水解法,制备时常加入尿素[CO(NH2)2 ]、醋酸钠等碱性物质。尿素分子中四种不同元素的电负性由大至小的顺序是__________;醋酸钠中碳原子的杂化类型是______。
(3)工业制备铁氧体也可使用沉淀法,制备时常加入氨(NH3)、联氨(N2H4)等弱碱。比较下表中氨(NH3)、联氨(N2H4)的熔沸点,解释其高低的主要原因:___________。
物质 | N2H4 | NH3 |
熔点/℃ | 2 | -77.8 |
沸点/℃ | 113.5 | -33.5 |
(4)Fe3O4晶体晶胞如图所示,计算Fe3O4晶体的密度________g·cm-3。 (图中a=0.42 nm,计算结果保留两位有效数字)
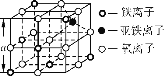
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入润洗过的锥形瓶中,并加入1或2滴酚酞溶液
⑤滴入一滴标准液后,溶液颜色由无色变为红色立即停止滴定,记录液面读数
请回答:

(1)以上步骤有错误的是(填编号)________。
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入______中。(从图中选填“甲”或“乙”)
(3)下列操作会引起实验结果偏大的是:______(填编号)
A 酸式滴定管未润洗
B 滴定前,滴定管尖嘴无气泡,滴定后有气泡
C 锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D 滴定结束时仰视滴定管,并记录数据
E 滴定过程中有一滴标准液飞溅出锥形瓶
(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视_______________。
II.利用中和滴定的原理,在工业生产中还可以进行氧化还原滴定测定物质含量。
(5)水泥中钙经处理得草酸钙沉淀经稀H2SO4处理后,用![]() 标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反为:
标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反为:![]() .实验中称取0.400g水泥样品,滴定时消耗了0.0500 mol·L-1的
.实验中称取0.400g水泥样品,滴定时消耗了0.0500 mol·L-1的![]() 溶液36.00 mL,则该水泥样品中钙的质量分数为__________
溶液36.00 mL,则该水泥样品中钙的质量分数为__________
(6)滴定终点的现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是( )
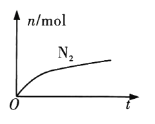
A.该反应的还原剂是Cl-
B.消耗1 mol还原剂,转移6 mol电子
C.氧化剂与还原剂的物质的量之比为2:3
D.反应后溶液的酸性明显增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C是一种常见的工业原料,实验室制备C的化学方程式如下,下列说法正确的( )
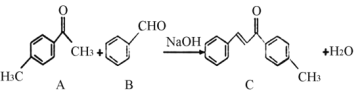
A.l mol的C最多能与7 mol的H2反应
B.分子C中所有碳原子一定共平面
C.可以用酸性KMnO4溶液鉴别A和B
D.A的同分异构体中含有苯环和醛基的结构有14种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g)2NH3(g) H<0,下列研究目的和图示相符的是( )
A.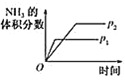 压强对反应的影响
压强对反应的影响
B.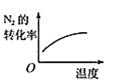 温度对反应的影响
温度对反应的影响
C.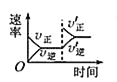 平衡体系增加N2对反应的影响
平衡体系增加N2对反应的影响
D.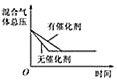 催化剂对反应的影响
催化剂对反应的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究乙醇和金属钠反应生成![]() 的原理,某同学做了如下四个实验。
的原理,某同学做了如下四个实验。
甲:向小烧杯中加入无水乙醇,再放入一小块金属钠,观察现象,并收集产生的气体
乙:设法检验甲收集到的气体。
丙:向试管中加人![]() 水,并加入绿豆粒大小的金属钠,观察现象。
水,并加入绿豆粒大小的金属钠,观察现象。
丁:向试管中加人![]() 乙醚(
乙醚(![]() ),并加入绿豆粒大小的金属钠,发现无明显变化。
),并加入绿豆粒大小的金属钠,发现无明显变化。
回答以下问题:
(1)从结构上分析,该实验选取水和乙醚作参照物的原因是__________。
(2)丙的目的是证明_____________;丁的目的是证明_______;根据丙和丁的结果,可以得出乙醇和金属钠反应的化学方程式应为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com