
【题目】按要求写方程式
(1)过氧化钠与水的离子方程式_________________。
(2)氢氧化亚铁在空气中被氧化的化学方程式___________。
(3)氢氟酸刻蚀玻璃的化学方程式____________________。
(4)除去Na2CO3固体中混有的NaHCO3的化学方程式____________。
(5)除去FeCl2溶液中混有的FeCl3的离子方程式___________。
【答案】2Na2O2 + 2H2O = 4Na++4OH— + O2↑ 4Fe(OH)2 + O2+ 2H2O = 4Fe(OH)3 SiO2 + 4HF = SiF4↑+ 2H2O 2NaHCO3![]() Na2CO3+CO2↑+H2O 2Fe3++ Fe = 3Fe2+
Na2CO3+CO2↑+H2O 2Fe3++ Fe = 3Fe2+
【解析】
(1)过氧化钠与水反应生成氢氧化钠和氧气;
(2)氢氧化亚铁在空气中被氧化生成氢氧化铁,白色沉淀变为灰绿色,最后变为红褐色;
(3)氢氟酸是弱酸,可与玻璃的成分SiO2发生反应;
(4)NaHCO3受热分解生成Na2CO3,水和CO2;
(5)铁粉与FeCl3反应,可将Fe3+还原为Fe2+。
(1)过氧化钠与水反应生成氢氧化钠和氧气,离子方程式为:2Na2O2 + 2H2O = 4Na++4OH- + O2↑;
(2)氢氧化亚铁在空气中被氧化生成氢氧化铁,反应方程式为:4Fe(OH)2 + O2+ 2H2O = 4Fe(OH)3;
(3)氢氟酸是弱酸,可与玻璃的成分SiO2发生反应,反应的方程式为:SiO2 + 4HF = SiF4↑+ 2H2O;
(4)NaHCO3受热分解生成Na2CO3,可用于除去Na2CO3固体中混有的NaHCO3,反应的方程式为:2NaHCO3![]() Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
(5)铁粉与FeCl3反应,可将Fe3+还原为Fe2+,可用于除去FeCl2溶液中混有的FeCl3,离子方程式为:2Fe3++ Fe = 3Fe2+。


科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,由CO合成甲醇:CO(g)+2H2(g)![]() CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是

A.CO合成甲醇的反应为吸热反应B.平衡常数![]()
C.该反应在![]() 时的平衡常数比
时的平衡常数比![]() 时的小D.处于A点的反应体系从
时的小D.处于A点的反应体系从![]() 变到
变到![]() ,达到平衡时
,达到平衡时![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1 L 0.1 mol/L的醋酸溶液用蒸馏水稀释到10 L,下列叙述正确的是( )
A. c(CH3COOH)变为原来的1/10
B. c(H+)变为原来的![]()
C. c(CH3COO-)/c(CH3COOH)的比值增大
D. 溶液的导电性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是元素的摇篮,海水中含有大量卤族元素。NaCl晶胞结构示意图如下所示(晶胞边长为a nm).

(1)元素 Na的价电子被激发到相邻高能级后形成的激发态Na原子,其价电子轨道表示式为__________。
(2)除了 NaCl,Cl 元素还能形成多种价态的化合物,如NaClO、NaClO2、NaClO3、NaClO4,这四种钠盐对应的酸的酸性依次增强,试解释HClO4的酸性强于HClO3的原因:__________。
(3)在适当条件下,电解NaCl水溶液可制得 NaClO3。
①NaCl水溶液中存在的微粒间作用力有________(填序号)。
A.离子键 B.极性键 C.配位键 D.氢键
②根据价层电子对互斥理论,预测ClO3-的空间构型为________,写出一个ClO3-的等电子体的化学符号:______________
(4)在NaCl晶体中,Na 位于Cl 所围成的正______面体的体心,该多面体的边长是______nm。
(5)Na 半径与Cl半径的比值为______(保留小数点后3位,![]() =1.414)。
=1.414)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将V1 mL 1.00mol·L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是

A.做该实验时环境温度为22℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约为1.00mol·L-1
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组变化中,前者小于后者的是( )
①CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1
CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH2
②2H2(g)+O2(g)═2H2O(l) ΔH1
H2(g)+![]() O2(g)===H2O(l) ΔH2
O2(g)===H2O(l) ΔH2
③t ℃时,在一定条件下,将1 mol SO2和1 mol O2分别置于恒容和恒压的两个密闭容器中,达到平衡状态时分别反应放出的热量
④CaCO3(s)===CaO(s)+CO2(g) ΔH1
CaO(s)+H2O(l)===Ca(OH)2(s) ΔH2
A. ①②③ B. ②④ C. ②③④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10.7g 氯化铵固体与足量氢氧化钙固体混合加热,使之充分反应。请计算:
(1)生成的氨气在标准状况下的体积是多少升____?
(2)若将这些氨气配成500mL氨水,该氨水的物质的量浓度是多少____________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2分子在催化剂的作用下发生的一系列转化如图所示。下列叙述正确的是( )
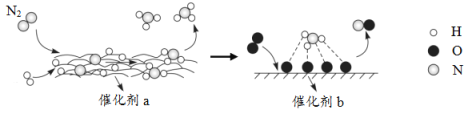
A.![]() 在反应过程中作催化剂
在反应过程中作催化剂
B.催化剂a表面发生了分解反应和化合反应
C.催化剂a、b增大了该历程中的最大能垒(活化能)
D.催化剂b表面发生的反应为:4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,用Fe2O3、NiO或Cr2O3作催化剂对燃煤烟气进行回收,使SO2转化生成S。催化剂不同,其他条件相同(浓度、温度、压强)情况下, 相同时间内SO2的转化率随反应温度的变化如下图,下列说法不正确的是
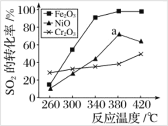
A.不考虑催化剂价格因素,选择Fe2O3作催化剂可以节约能源
B.选择Fe2O3作催化剂,最适宜温度为340 ℃左右
C.a 点后SO2的转化率减小的原因可能是温度升高催化剂活性降低了
D.其他条件相同的情况下,选择Cr2O3作催化剂,SO2的平衡转化率最小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com