
【题目】起固定氮作用的化学反应是
A.氮气与氢气在一定条件下反应生成氨气
B.一氧化氮与氧气反应生成二氧化氮
C.氨气经催化氧化生成一氧化氮
D.由氨气制碳酸氢铵和硫酸铵
科目:高中化学 来源: 题型:
【题目】X、R、Y、Z、M为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示,R的原子序数大于Z。下列说法错误的是
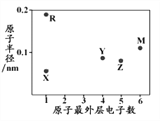
A. R的氧化物只含有离子键
B. 最高价含氧酸的酸性:Y<M
C. 最简单氢化物的稳定性:Y<Z
D. Z的简单氢化物可用作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
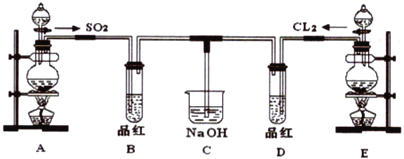
(1)实验室用装置A制备SO2,某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:_________________________________________。
(2)实验室用装置E制备Cl2,其反应化学化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
①指出该反应中在反应中HCl(浓)所表现出的化学性质_____________、___________。
②请把(2)中的化学方程式改写为离子方程式_______________________________________。
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现__________的现象(填选项,下同。
A.品红都褪色 B.品红都不褪色
C.试管B 中品红褪色D 中不褪色 D.试管D 中品红褪色B 中不褪色
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象又分别为__________。
A.无色 红色 B.无色 无色 C.红色 红色 D.红色 无色
(4)C 烧杯氢氧化钠溶液的作用是________________________。
(5)另一个实验小组的同学认为SO2 和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是( )
A.一定浓度的醋酸钠溶液可使酚酞溶液变红,其原因是发生了如下反应:CH3COO﹣+H2OCH3COOH+OH﹣ , 使得溶液中的c(OH﹣)>c(H+)
B.在常温下,10 mL 0.2 molL﹣1盐酸与10 mL 0.2 molL﹣1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=13
C.在0.1 molL﹣1 NH4Cl溶液中:c(H+)+c(NH4+=c(Cl﹣)
D.5 mL 1 molL﹣1 CH3COONa溶液与5 mL 1 molL﹣1盐酸混合液中c(Cl﹣)=c(Na+)>c(H+)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的离子方程式正确的是:( )
A. 向NaOH溶液中通入足量SO2: SO2 + 2OH- = SO32-+ H2O
B. 向KI与稀硫酸的混合溶液中通入氧气: 4H+ + 4I-+ O2= 2I2 +2H2O
C. 等体积等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合:2HCO![]() +Ba2++2OH-=BaCO3↓+ 2H2O
+Ba2++2OH-=BaCO3↓+ 2H2O
D. 硫酸亚铁溶液与稀硫酸、双氧水混合: Fe2+ + 2H2O2 + 4H+ = Fe3+ + 4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中各微粒的浓度关系正确的是( )
A.pH相等的①NH4Cl溶液、②(NH4)2SO4溶液、③NH4HSO4溶液,溶液中c(NH4+)的大小顺序为①>②>③
B.pH相等的NaF溶液与CH3COOK溶液:[c(Na+)﹣c(F﹣)]>[c(K+)﹣c(CH3COO﹣)]
C.0.2 mol?L﹣1Na2CO3溶液:c(OH﹣)=c(HCO![]() )+c(H+)+c(H2CO3)
)+c(H+)+c(H2CO3)
D.0.2 mol?L﹣1盐酸与0.1 mol?L﹣1NaAlO2溶液等体积混合:c(Cl﹣)>c(Na+)>c(Al3+)>c(H+)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:Cu2+(aq)+Fe(s)═Fe2+(aq)+Cu(s)设计的原电池如图所示.
请回答下列问题:
(1)电解质溶液Y是;
(2)Cu电极发生的电极反应为X电极上发生的电极反应为;
(3)外电路中的电流是从电极流向电极.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国产铜主要取自黄铜矿(CuFeS2),湿法炼铜工艺的核心是黄铜矿的浸出,目前主要有氧化浸出、配位浸出和生物浸出三种方法。
I.氧化浸出
(1)在硫酸介质中用双氧水将黄铜矿氧化,测得有SO42-生成。
①该反应的离子方程式为________________________________.
②该反应在25—50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,试分析其原因为__________________________________________________
Ⅱ,配位浸出
反应原理为:CuFeS2+NH3·H2O+O2+OH-→ Cu(NH3)42++Fe2O3+SO42-+H2O(未配平)
(2)用化学用语解释氨水溶液的酸碱性______________________________.
(3)生产中为了稳定溶液的pH,可以在浸出液加入___________________(物质名称)Ⅲ.生物浸出
在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。
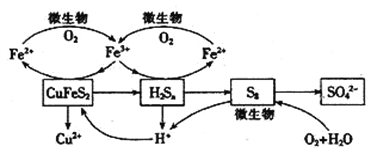
(4)在微生物的作用下,可以循环使用的物质有_________(填化学式),微生物参与的离子反应方程式为_______________________________(任写一个)。
(5)假如黄铜矿中的铁元素最终全部转化为Fe3+,当有2 mol SO42-生成时,理论上消耗O2的物质的量为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
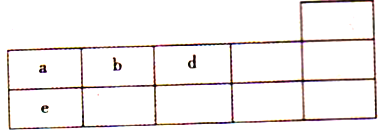
(1)a原子结构示意图为___________,d的一种氢化物为常见溶剂,其电子式为__________。
(2)e的最高价氧化物对应水化物的钠盐液中通入少量a的最高价氧化物会发生反应,写出相应的离子方程式:____________________________________。
(3)X、Y为同周期元素,它们简单离子的电子层与d离子的电子层结构相同,Y离子半径在同周期元素简单离子半径中最小,X、Y两种元素最高价氧化物对应的水化物之间可以相互反应生成盐和水,写出该反应的化学方程式:____________________________,X在周期表中的位置为________________。
(4)与Y同周期的W元素,其原子半径是同周期主族元素中最小的。工业上制取Y和W的无水化合物方法如下:Y的氧化物与a、W的单质在高温条件下反应,每消耗6kg a的单质,过程中转移1×103mol电子,写出相应反应的化学方程式:_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com