
【题目】下列实验装置符合实验目的的是( )
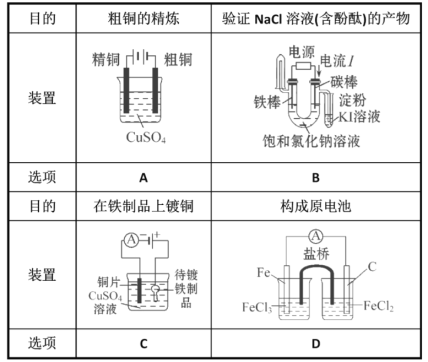
A. AB. BC. CD. D
【答案】B
【解析】
A.电解精炼粗铜时,粗铜作阳极,精铜作阴极,电解质溶液为可溶性的硫酸铜溶液,故A错误;
B.根据电流方向知,碳棒作阳极,铁棒作阴极,阳极上氯离子失电子生成氯气,氯气能和碘离子反应生成碘单质,碘遇淀粉试液变蓝色,阴极上氢离子放电生成氢气,同时阴极附近生成氢氧根离子而使溶液呈碱性,无色酚酞试液遇碱变红色,所以该装置能检验氯化钠溶液的产物,故B正确;
C.电镀时,镀层铜作阳极,镀件铁作阴极,铁应该连接电源负极,电解质溶液为可溶性的铜盐,故C错误;
D.该装置要形成原电池,铁作负极、碳作正极,正极所在的电解质溶液为氯化铁溶液,负极所在溶液为氯化亚铁溶液,故D错误;
故答案为B。


科目:高中化学 来源: 题型:
【题目】实验室用Na2CO3·10H2O晶体配制240 mL 0.1 mol·L-1 Na2CO3溶液,回答下列问题:
(1)实验所需仪器除托盘天平、烧杯、玻璃棒和胶头滴管外,还需要一种主要仪器X。则仪器X的名称是__________;
(2)用托盘天平称取Na2CO3·10H2O的质量为_____________________;
(3)配制时,正确的操作顺序是(用字母表示,每个字母只能用一次)______________ED;
A.用蒸馏水洗涤烧杯及玻璃棒2~3次,洗涤液均注入仪器X,振荡
B.用托盘天平称量所需的Na2CO3·10H2O晶体,放入烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其完全溶解
C.将已冷却的Na2CO3溶液沿玻璃棒注入仪器X中
D.将仪器X盖紧,振荡摇匀
E.改用胶头滴管加水,使溶液凹液面的最低点恰好与刻度线相切
F.继续往仪器X内小心加水,直到液面接近刻度线1~2 cm处
(4)若出现如下情况,会使所配溶液的浓度偏高的是______________。
①没有进行A操作
②称量时,Na2CO3·10H2O已失去部分结晶水
③进行E操作时俯视
④D操作完成后,发现液面低于刻度线,又用胶头滴管加水至刻度
⑤称量时,按照左码右物的操作进行称量。
⑥溶液未冷却,就转移到容量瓶中。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列有关叙述正确的是( )
A. 1 molCH4(g)和2 molO2(g)的能量总和小于1 mol CO2(g)和2 mol H2O(g)的能量总和
B. 标准状况下,44.8L NO与22.4L O2混合后气体中分子总数小于2NA
C. 1 molFe在氧气中充分燃烧失去3NA个电子
D. 在标准状况下,NA个CHCl3分子所占的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下发生反应 2SO3(g)![]() 2SO2(g)+O2(g),将2 mol SO3通入2 L容积恒定的密闭容器中,若维持容器内温度不变,5 min末测得SO3的物质的量为0.8 mol。则下列说法正确的是
2SO2(g)+O2(g),将2 mol SO3通入2 L容积恒定的密闭容器中,若维持容器内温度不变,5 min末测得SO3的物质的量为0.8 mol。则下列说法正确的是
A.若某时刻消耗了1 molSO3同时生成了0.5molO2,则表明该反应达到了平衡状态
B.若起始时充入3 mol SO3,起始时SO3分解速率不变
C.0~5min,SO2的生成速率v(SO2)=0.12mol·L-1·min-1
D.达到平衡时,SO2和SO3的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法一定错误的是( )
A.某些花岗石产生氡(![]() Rn),从而对人体产生伤害,Rn元素的相对原子质量是222
Rn),从而对人体产生伤害,Rn元素的相对原子质量是222
B.Se是人体必需的微量元素,![]() Se和
Se和![]() Se互为同位素,是两种不同的核素
Se互为同位素,是两种不同的核素
C.![]() U的浓缩一直被国际社会关注,其中子数和质子数之差为51
U的浓缩一直被国际社会关注,其中子数和质子数之差为51
D.112号元素属于过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含硫酸铝和氯化铝的混合溶液中逐滴加入氢氧化钡溶液至过量,加入氢氧化钡溶液的体积和所得沉淀的物质的量的关系如图所示。
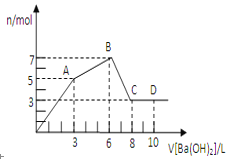
(1)氢氧化钡溶液浓度为_____________________。
(2)原混合溶液中SO42-和Cl-的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】COCl2俗名称作光气,是有毒气体。在一定条件下,可发生的化学反应为:COCl2(g) ![]() CO(g)+Cl2(g) ΔH<0 下列有关说法不正确的是
CO(g)+Cl2(g) ΔH<0 下列有关说法不正确的是
A. 在一定条件下,使用催化剂能加快反应速率
B. 当反应达平衡时,恒温恒压条件下通入Ar,COCl2的转化率不变
C. 单位时间内生成CO和消耗Cl2的物质的量比为1∶1时,反应达到平衡状态
D. 平衡时,其他条件不变,升高温度可使该反应的平衡常数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1。回答有关中和反应的问题:
(1)用0.1molNaOH配成稀溶液与足量稀硝酸反应,放出_____热量。
(2)如图装置中缺少的一种玻璃仪器是___,碎泡沫塑料的作用____。
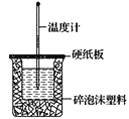
(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3kJ·mol-1,其原因可能是____。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热ΔH会___(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法不正确的是
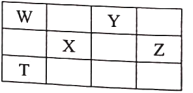
A.原子半径:r(X)>r(Z)>r(W)>r(Y)
B.单质Z2、Y3和Z与Y形成的化合物ZY2均可用于自来水消毒
C.X元素可形成两种或以上的单质,且在一定条件下可以相互转化
D.T元素的单质具有半导体的特性,其最高价氧化物对应水化物是一种强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com