
 在催化剂表面NH3脱硫的原理为:8NH3(g)+6SO2(g)=3S2(g)+4N2(g)+12H2O(g)△H,实验测定在不同$\frac{n(N{H}_{3})}{n(S{O}_{2})}$下,温度与SO2的转化率关系如图,下列说法正确的是( )
在催化剂表面NH3脱硫的原理为:8NH3(g)+6SO2(g)=3S2(g)+4N2(g)+12H2O(g)△H,实验测定在不同$\frac{n(N{H}_{3})}{n(S{O}_{2})}$下,温度与SO2的转化率关系如图,下列说法正确的是( )| A. | 脱硫反应△H<0 | |
| B. | 及时从体系中除去水,平衡常熟增大 | |
| C. | 相同条件下,催化剂活性越大,SO2的平衡转化率越高 | |
| D. | $\frac{n(N{H}_{3})}{n(S{O}_{2})}$:a<b<c |
分析 A、依据图象判断,温度越高,二氧化硫的转化率越大;
B、平衡常数只与温度有关,据此解答即可;
C、由图可知:相同温度下,NH3物质的量越大,SO2的转化率也越大;
D、加入催化剂只会改变化学反应速率,不影响转化率.
解答 解:A.在相同氨硫比下由于温度越高二氧化硫转化率越大,故正反应为吸热反应,则△H>0,故A错误;
B.平衡常数只与温度有关,故B错误,
C.催化剂只能改变化学反应速率,不影响化学平衡,故C错误;
D.在相同温度,NH3物质的量越大,SO2的转化率也越大,故D正确;
故选D.
点评 本题主要考查的是转化率与温度图象的分析,涉及化学平衡常数的影响因素,吸热与放热的判断等,难度不大,会读图是解决本题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 大量生产、使用能过滤PM2.5的口罩 | |
| B. | 用石灰对煤燃烧后形成的烟气进行脱硫处理 | |
| C. | 开发利用太阳能、氢能、风能等清洁能源 | |
| D. | 研究廉价、高效的催化剂,以降低汽车尾气中有害物质的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 催化剂组分质量分数(%) | CuO | 0 | 25 | 50 | 75 | 100 |
| ZnO | 100 | 75 | 50 | 25 | 0 | |
| 到达平衡所需时间(h) | 2.5 | 7.4 | 8.1 | 12 | 无催化活性 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽油、柴油和植物油都是碳氢化合物 | |
| B. | 葡萄糖和银氨溶液发生银镜反应可用作制镜子 | |
| C. | 往花生油中加入稀硫酸能发生皂化反应 | |
| D. | 鸡蛋清中加入胆矾可以使蛋白质发生盐析 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、H+、NO3-、HCO3- | B. | K+、Al3+、SO42-、NH3•H2O | ||
| C. | Na+、K+、SO32-、Cl2 | D. | Na+、Mg2-、SO42-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向硫酸铜溶液中加入NaHS溶液:Cu2++HS-=CuS↓+H+ | |
| B. | 用醋酸除去水垢中的碳酸钙:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| C. | 用强碱溶液吸收工业制取硝酸尾气:NO+NO2+2OH-=2NO3-+H2O | |
| D. | 将少量SO2气体通入氨水中:SO2+NH3•H2O=NH4++HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 饱和氯水中:Cl-、NO3-、Na+、CO32- | |
| B. | c(H+)=1.0×10-13mol•L的溶液中:MnO4-、K+、SO42-、AlO2- | |
| C. | c(AlO2-)=1.0mol•L的溶液中:SO42-、K+、Cl-、HCO3- | |
| D. | pH=7的溶液中:NO2-、I-、Na+、Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

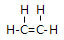 ;由元素④和元素②形成的化合物的电子式为
;由元素④和元素②形成的化合物的电子式为 ;元素⑦的原子结构示意图为
;元素⑦的原子结构示意图为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (若有配位键,用箭号表示)
(若有配位键,用箭号表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com