
【题目】请回答下列问题:
![]() 已知:
已知:![]() 、
、![]() 分子中化学键的键能分别是
分子中化学键的键能分别是![]() 、
、![]()
![]()
![]()
则相同条件下破坏1molNO中化学键需要吸收的能量为______kJ。
![]() 如图所示,U形管内盛有100mL的溶液,
如图所示,U形管内盛有100mL的溶液,
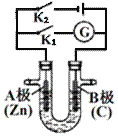
![]() 断开
断开![]() ,闭合
,闭合![]() ,若所盛溶液为
,若所盛溶液为![]() 溶液:则A为______极。若所盛溶液为KCl溶液:
溶液:则A为______极。若所盛溶液为KCl溶液:![]() 移向______极
移向______极![]() 填“A”、“B”
填“A”、“B”![]()
![]() 断开
断开![]() ,闭合
,闭合![]() ,若所盛溶液为滴有酚酞的NaCl溶液,则:A电极附近可观察到的现象是______。反应一段时间后打开
,若所盛溶液为滴有酚酞的NaCl溶液,则:A电极附近可观察到的现象是______。反应一段时间后打开![]() ,若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的______。
,若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的______。
![]() 若是电解精炼粗铜,断开
若是电解精炼粗铜,断开![]() ,闭合
,闭合![]() ,电解液选用
,电解液选用![]() 溶液,则A电极的材料应换成______,反应一段时间后电解质溶液中
溶液,则A电极的材料应换成______,反应一段时间后电解质溶液中![]() 浓度______
浓度______![]() 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”![]()
【答案】![]() 正 B 产生无色气泡,溶液变红色 HCl 纯铜 减小
正 B 产生无色气泡,溶液变红色 HCl 纯铜 减小
【解析】
(1)断键吸收能量,成键放出能量,设NO的键能为x,![]() +
+![]() -2x=
-2x=![]() ,解得x=631.5 kJ·mol—1,破坏1molNO中化学键需要吸收的能量为631.5KJ
,解得x=631.5 kJ·mol—1,破坏1molNO中化学键需要吸收的能量为631.5KJ
(2)①原电池中,阴离子向负极移动,阳离子向正极移动,![]() 移向正极。
移向正极。
②断开![]() ,闭合
,闭合![]() ,该装置是电解池,A为阴极,B为阳极,所盛溶液为滴有酚酞的NaCl溶液,A级发生的反应:2H2O+2e—=2OH—+H2↑电解一段时间,导致碱性增强,酚酞变红,产生无色气泡;
,该装置是电解池,A为阴极,B为阳极,所盛溶液为滴有酚酞的NaCl溶液,A级发生的反应:2H2O+2e—=2OH—+H2↑电解一段时间,导致碱性增强,酚酞变红,产生无色气泡;
反应一段时间后打开![]() ,若要使电解质溶液恢复到原状态,根据“析出什么就加入什么”的原则,分析方程式:
,若要使电解质溶液恢复到原状态,根据“析出什么就加入什么”的原则,分析方程式: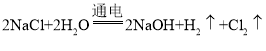 ,反应放出H2和Cl2,相当于析出HCl,所以通入HCl。
,反应放出H2和Cl2,相当于析出HCl,所以通入HCl。
③A级是阴级,B级是阳级,电解精炼粗铜粗铜在阳极,精铜在阴极,A电极的材料应换成纯铜。
(3)用电荷守恒就可以因为阳极上存在的杂质也发生了电极反应,而阴极上只有铜析出,溶解的铜小于析出的铜。换言之,进入溶液的Cu2+少于阴极消耗的Cu2+,所以c(Cu2+)减小。


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】一定质量的铁铝合金完全溶于过量的稀硝酸中,反应过程中共产生4.48 LNO(标准状况下测定),若在反应后的溶液中加入足量的氢氧化物溶液,则生成沉淀的质量不可能是
A.21.4 gB.18.7 gC.15.6 gD.7.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,水的电离达到平衡: H2O![]() H++ OH-ΔH > 0 ,下列叙述正确的是
H++ OH-ΔH > 0 ,下列叙述正确的是
A. 将水加热,Kw增大,pH不变
B. 向水中加入少量盐酸,c(H+)增大,Kw不变
C. 向水中加入NaOH固体,平衡逆向移动,c(OH-) 降低
D. 向水中加入AlCl3固体,平衡逆向移动,c(OH-) 增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在固态金属氧化物电解池中,高温电解H2OCO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是( )

A.X是电源的负极
B.阴、阳两极生成的气体的物质的量之比是1∶1
C.总反应可表示为H2O+CO2![]() H2+CO+O2
H2+CO+O2
D.阴极的电极反应式是H2O+2e-=H2+O2-、CO2+2e-=CO+O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用三室式电解池(装置结构如图所示,电极均为惰性电极)可以实现用硫酸钠溶液制取硫酸和氢氧化钠。下列叙述正确的是
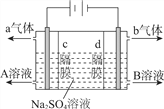
A.a气体为氢气,b气体为氧气
B.A为氢氧化钠溶液,B为硫酸溶液
C.通电后中问隔室的SO42-向阴极迁移,阳极区溶液的pH增大
D.该电解反应的方程式为2Na2SO4+6H2O![]() 2H2SO4+4NaOH+O2↑+2H2↑
2H2SO4+4NaOH+O2↑+2H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。CO2 可以被NaOH溶液捕获,其基本过程如下图所示(部分条件及物质未标出)。
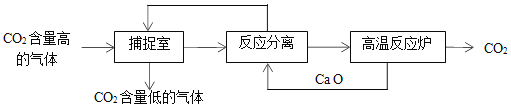
(1)下列有关该方法的叙述中正确的是______。
a.能耗大是该方法的一大缺点
b.整个过程中,只有一种物质可以循环利用
c.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤
d.该方法可减少碳排放,捕捉到的 CO2还可用来制备各种化工产品
(2)若所得溶液 pH=13,CO2 主要转化为______(写离子符号)。已知 CS2与 CO2分子结构相似, CS2的电子式是______,CS2熔点高于 CO2,其原因是______。
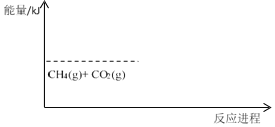
(3)CO2 与 CH4 经催化重整,制得合成气:CH4(g)+CO2(g)→2CO(g)+2H2(g)-120kJ,补全下图中 CO2 与 CH4 催化重整反应的能量变化示意图(即,注明生成物能量的大致位置及反应热效应数值)_______________
(4)常温下,在 2L 密闭容器中,下列能说明该反应达到平衡状态的是______。
a.每消耗 16gCH4 的同时生成 4gH2
b.容器中气体的压强不再改变
c.混和气体的平均相对分子质量不发生改变
d.容器中气体的密度不再改变
反应进行到 10 min 时,CO2 的质量减少了 8.8 g,则 0~10 min 内一氧化碳的反应速率是______。
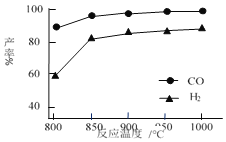
(5)按一定体积比加入 CH4 和 CO2,在恒压下发生反应,温度对 CO 和 H2 产率的影响如图所示。此反应优选温度为 900℃的原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
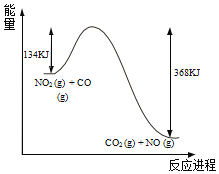
【题目】如图是NO2气体和CO气体反应生成CO2 气体和NO气体过程的能量变化示意图。则该反应的热化学方程式为( )
A.NO2+CO→CO2+NO-134kJ
B.NO2(g)+CO(g)→CO2(g)+NO(g)-234kJ
C.NO2(g)+CO(g)CO2(g)+NO(g)+368kJ
D.NO2(g)+CO(g)CO2(g)+NO(g)+234kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】传统接触法制取硫酸能耗大,污染严重。将燃料电池引入 硫酸生产工艺可有效解决能耗和环境污染问题,同时提供电能 以燃料电池为电源电解硫酸铜溶液的工作原理示意图如下所示。下列说法不正确的是( )
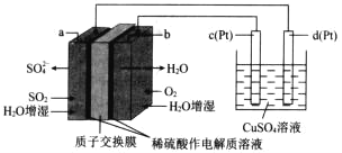
A.若 a 极消耗 2.24LSO2,理论上 c 极有 6.4g 铜析出
B.H+由 a 极通过质子交换膜向 b 极移动
C.该燃料电池的总反应式为 2SO2+O2+2H2O=2H2SO4
D.b 极为正极,电极反应式为 O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华文化源远流长,如![]() 本草图经
本草图经![]() 中曾有对青矾的描述:“形似朴硝
中曾有对青矾的描述:“形似朴硝![]() 而绿色,取此物置于铁板上,聚碳,封之囊袋,吹令火炽,其矾即沸,流出,色赤如融金升者是真也。”对于文中描述,下列说法正确的是
而绿色,取此物置于铁板上,聚碳,封之囊袋,吹令火炽,其矾即沸,流出,色赤如融金升者是真也。”对于文中描述,下列说法正确的是![]()
![]()
A.朴硝既不属于电解质也不属于非电解质
B.青矾的成分为![]()
C.文中使用了蒸发结晶的分离方法
D.文中的反应涉及了氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com