
【题目】20mL 0.1000 molL-1氨水用0.1000 molL-1的盐酸滴定,滴定曲线入右下图,下列说法正确的是

A. 该中和滴定适宜用酚酞作指示剂
B. 两者恰好中和时,溶液的pH=7
C. 达到滴定终点时,溶液中:c(H+)= c(OH-)+ c(NH3·H2O)
D. 当滴入盐酸达30mL时,溶液中c(NH4+)+c(H+)-)+c(Cl-)
科目:高中化学 来源: 题型:
【题目】碳酸二甲酯[(CH3O)2CO]是一种具有发展前景的“绿色”化工产品,电化学合成碳酸二甲酯的工作原理如图所示(加入两极的物质均是常温常压下的物质)。下列说法正确的是

A. 电解一段时间后,阴极和阳极消耗的气体的物质的量之比为l:2
B. 石墨l极发生的电极反应为2CH3OH+CO-e-=(CH3O)2CO+H+
C. 石墨2极与直流电源正极相连
D. H+由石墨2极通过质子交换膜向石墨l极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为原子序数依次增大的前四周期元素。BA3能使湿润的红色石蕊试纸变蓝,A、B、C三种原子的电子数之和等于25,DC晶体中D+的3d能级上电子全充满。
请回答下列问题:
(1)以上四种元素中,第一电离能最大的是_______(填元素符号);D的基态原子的核外电子排布式为_________。
(2)在BA3、AC中,沸点较高的是______。(填化学式),其原因是_______。DA的晶体类型是_______。
(3)BA4C晶体中_____(填“含”或“不含”)配位键,在该晶体中B原子的价层电子对数为_______。

(4)化合物BC3的立体构型为_____,其中心原子的杂化轨道类型为_______。
(5)由B、D形成的晶体的晶胞如图所示,已知紧邻的B原子与D原子间的距离为acm。
①该晶胞的化学式为_________。②B元素原子的配位数为_________。
③该晶体的密度为______(用含a、NA的代数式表示,设NA为阿伏加德罗常数的数值)g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同学们请游爷爷讲述抗战故事,爷爷打开一个珍藏的箱子,拿出一件粗棉布军装、一把黄铜军号、一副玻璃眼镜和一本记有烈士名单的塑料封皮笔记本,给同学们讲述了当年的惨烈战事。下列说法不正确的是( )
A. 棉是天然高分子材料 B. 黄铜是合金
C. 塑料是合成高分子材料 D. 玻璃是合成纤维材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同分异构现象是有机物种类繁多的原因之一。与CH3CH2CH2CH2OH互为同分异构体的是( )
A. (CH3)3CHO
B. (CH3)2CHCH2COOH
C. CH3CH2CH2CHO
D. CH3CH2CH2CH2CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应 CH4(g) + H2O(g)==CO(g)+3H2(g) △H1
已知:
①CH4、H2、CO 的燃烧热(△H)分别为-a kJmol-1、-b kJmol-1、-c kJmol-1;
②H2O(l) =H2O(g) △H=+dkJmol-1
则△H1= ___________(用含字母a、b、c、d的代数式表示)kJmol-1。
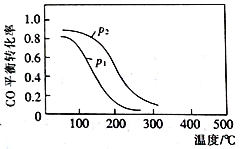
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g) △H2,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如右图所示,200℃时n(H2)随时间的变化如下表所示:
CH3OH(g) △H2,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如右图所示,200℃时n(H2)随时间的变化如下表所示:
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①△H2_________(填“>”“<”或“ = ”)0。
②写出两条可同时提高反应速率和CO转化率的措施:________________________ 。
③下列说法正确的是____________(填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
C.容器内气体压强不再变化时,反应达到最大限度
D.图中压强p12
④03 min内用CH3OH表示的反应速率v(CH3OH)=_________mol L-1·min-1。
⑤200℃时,该反应的平衡常数K =_______。向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡____________(填“正向”、“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6 L甲烷,测得电路中转移1.2 mol电子,则甲烷的利用率为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往下列溶液中加入足量NaOH溶液,充分反应后,不会出现沉淀的是( )
A. MgCl2溶液 B. AlCl3溶液 C. CaCl2溶液 D. FeCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素最高正价与负价绝对值之差为4,该元素的离子与跟其核外电子排布相同的离子形成的化合物是( )
A.K2S B.MgO C.MgS D.NaF
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用10mL 0.1mol/L的BaCl2溶液分别和相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液反应,均恰好使三份溶液中的SO42-离子完全转化为BaSO4沉淀,则三种硫酸盐溶液的物质的量浓度之比是( )
A. 3∶2∶2 B. 1∶2∶3 C. 3∶1∶1 D. 1∶3∶3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com