
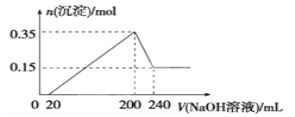
����Ŀ����һ��������þ�������Ͷ��200 mLϡ�����У�����ȫ���ܽ����������Һ����μ��� NaOH ��Һ�����ɳ��������ʵ��������� NaOH ��Һ����ı仯��ϵ��ͼ��ʾ��������˵������ȷ���ǣ� ��
A. þ������������Ϊ9 g
B. ���ɵ������ڱ�״���µ����Ϊ11.2 L
C. ���20 mL NaOH��Һ�����к���������
D. ����������Һ�����ʵ���Ũ��Ϊ5 mol��L-1
���𰸡�B
����������ͼ���֪���ӿ�ʼ������NaOH��Һ20mL��û�г������ɣ�˵��ԭ��Һ�������ܽ�Mg��Al��������ʣ�࣬��ʱ�����ķ�ӦΪ��H2SO4+2NaOH=Na2SO4+2H2O����V��NaOH��Һ��=200mLʱ�����������ʱΪMg��OH��2��Al��OH��3���������ʵ���֮��Ϊ0.35mol����Һ������ΪNa2SO4��������Ԫ���غ��֪��ʱn��Na2SO4������200mL����������Һ�к��е�n��NaOH����1/2������200mL��240mL��NaOH�ܽ�Al��OH��3��NaOH+Al��OH��3=NaAlO2+2H2O����V��NaOH��Һ��=240mLʱ���������ټ��٣���ʱȫ��ΪMg��OH��2�����ʵ���Ϊ0.15mol����Al��OH��3Ϊ0.35mol-0.15mol=0.2mol�����ڴ�200mL��240mL��NaOH�ܽ�Al��OH��3��NaOH+Al��OH��3=NaAlO2+2H2O�����Ըý�����n��NaOH��=n[Al��OH��3]=0.2mol���������Ƶ�Ũ��Ϊ0.2mol��(0.24L0.20L)=5mol/L��A����Ԫ���غ��֪n��Al��=n[Al��OH��3]=0.2mol��n��Mg��=n[Mg��OH��2]=0.15mol����þ������������Ϊ0.2mol��27g/mol+0.15mol��24g/mol=9g��A��ȷ��B����A�п�֪n��Al��=0.2mol��n��Mg��=0.15mol�����ݵ���ת���غ��֪2n��H2��=3n��Al��+2n��Mg��=3��0.2mol+2��0.15mol=0.9mol������n��H2��=0.45mol���������Ϊ0.45mol��22.4mol/L=10.08L��B����C����ͼ���֪���ӿ�ʼ������NaOH��Һ20mL��û�г������ɣ�˵��ԭ��Һ�������ܽ�Mg��Al��������ʣ�࣬��ʱ�����ķ�ӦΪH2SO4+2NaOH=Na2SO4+2H2O��C��ȷ��D���������Ϸ�����֪����������Һ�����ʵ���Ũ��Ϊ5 mol��L-1��D��ȷ����ѡB��


 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д� �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯��Ҫ���뻹ԭ������ʵ�ֵ��ǣ��� ��
A. HCl��Cl2B. Fe��Fe3��C. KClO3��O2D. KMnO4-��Mn2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������;�㷺������ʹ��ʱ��һ�������Ȼ��⣮��ҵ�Ͽ���O2��HClת��ΪCl2 �� �����Ч�棬������Ⱦ����ӦΪ��O2+4HCl ![]() 2Cl2+2H2O
2Cl2+2H2O 
���������գ�
��1���÷�Ӧ��ѧƽ�ⳣ��K�ı���ʽΪ��ʵ����P0ѹǿ�£�HClƽ��ת���ʦ���HCl���淴Ӧ�¶�T�ı仯��ͼ1��ʾ��������Ӧ����Ӧ������ȡ����ߡ����ȡ�����
��2������ʵ������ѹ�����ʹѹǿ��P0������P1 �� ��ͼ�л���P1ѹǿ��HClƽ��ת���ʦ���HCl���淴Ӧ�¶�T�仯�����ߣ�����Ҫ˵�����ɣ�
��3���÷�Ӧ��P0��320��C�����½��У���ƽ��״̬Aʱ�����������n��Cl2��=7.2��10��3mol�����ʱ�����е�n��HCl��=mol��
��4���Ը÷�Ӧ�ﵽƽ������·�����ȷ������ѡ���ţ���a������n��HCl����������Ӧ�ķ�Ӧ����Ӱ�����
b������������ϡ�����壬������Ӧ�ķ�Ӧ����Ӱ�����
c��ѹǿ�������ϡ�����壬���淴Ӧ�ķ�Ӧ����Ӱ�����
d�����ƽ�ⳣ��Kֵ�����淴Ӧ������Ӱ�����
��5����Ԫ�����γɶ������ӣ���ˮ��Һ��1molCl����1mol ClOx����x=1��2��3��4����������Դ�С��ͼ2��ʾ��д��B��A+C��Ӧ���Ȼ�ѧ����ʽ�������ӷ��ű�ʾ��������1.5molB������Ӧ��ת�Ƶ���mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ����һ��2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ��ش��������⣺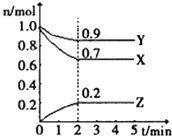
��1���÷�Ӧ��minʱ�ﵽ��ѧƽ��״̬��
��2���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3���ӿ�ʼ��2min��Z��ƽ����Ӧ������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˳�ȥNO��NO2��N2O4�Դ�������Ⱦ��������NaOH��Һ�������մ�������Ӧ����ʽ��2NO2+2NaOH=NaNO3+NaNO2+H2O��NO2 +NO+2NaOH=2NaNO2+H2O ��������a mol NO��b mol NO2�� c mol N2O4��ɵĻ������ǡ�ñ� V L NaOH ��Һ���գ�������ʣ�ࣩ����� NaOH ��Һ�����ʵ���Ũ��Ϊ( ) mol/L
A. ��a+b+c��/V B. 2��a+b+c��/3V C. ��b+2c��/V D. ��a+b+2c��/V
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡһС���Ʒ�����������ȣ�����ʵ��������ȷ����
���������ۻ�
���ڿ�����ȼ�գ�����ʻ�ɫ
��ȼ��ʱ��������
��ȼ�պ����ɵ���ɫ����
��ȼ�պ����ɰ�ɫ����
A���٢ڢ� B���٢ڢ� C���٢ڢ� D���ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Թ���ʢ��������ݹ���������U�ι���ʢ��һ�κ�īˮ����ʼʱU����˺�īˮˮ���½���һ��ʱ���U����˺�īˮˮ��������������˵������ȷ���ǣ� �� 
A.��ʼʱ�����������ⸯʴ
B.����ʱ���������������ʴ
C.����ʱ���ڸ����ĵ缫��Ӧ��ͬ
D.����ʱ���������ĵ缫��Ӧ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�������ԭ��Ӧʵ�ʵ�˵������ȷ���ǣ� ��
A���Ƿ���Ԫ�ػ��ϼ۵ı仯 B���Ƿ�����Ԫ�صIJμ�
C���Ƿ��е��ӵ�ת�� D���Ƿ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ�����Ԫ�ص����ݼ���ͼ��˵����ȷ���ǣ� �� 
A.��Ԫ�ص���������16
B.��Ԫ�ص����ԭ��������16.00
C.��ԭ��2p�Dz���һ��δ�ɶԵ���
D.��ԭ���������6��������ͬ�ĵ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com