
【题目】下列操作或装置,不能达到实验目的的是( )。

A.图Ⅰ用于实验室制氨气并收集干燥的氨气
B.图Ⅱ用于检验浓硫酸与铜反应后的产物中是否含有铜离子
C.图Ⅲ用于验证牺牲阳极的阴极保护法
D.图Ⅳ用于制取![]() 晶体
晶体
【答案】B
【解析】
A.实验室用加热NH4Cl和Ca(OH)2的混合物的方法制取氨气,氨气是碱性气体,密度比空气小,用碱石灰干燥,采用向下排空气法收集,A选项不符合题意;
B.由于可能还有过剩的浓硫酸,因此在检验浓硫酸与铜反应后的产物中是否含有铜离子时应将反应后的溶液倒入水中,类似于浓硫酸的稀释,B选项符合题意;
C.原电池中锌作负极失去电子发生氧化反应,铁作正极被保护,可用K3[Fe(CN)6]来检验是否生成Fe2+从而验证牺牲阳极的阴极保护法,C选项不符合题意;
D.CO2和NH3通入饱和的氯化钠溶液中反应生成碳酸氢钠晶体,反应的化学方程式为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,蘸有稀硫酸的棉花可吸收氨气,防止污染空气,D选项不符合题意;
答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某学生为比较镁、铝的金属性强弱,设计了如下实验:
(1)向两支试管中分别加入3 mL同浓度的稀盐酸,再将两块大小相同且纯净的镁片和铝片分别加入试管中,反应初始时观察到如图所示的现象,则试管b内加入的金属为____________(写化学式)。

(2)若加入的两块金属的物质的量相等,且试管中稀盐酸足量,充分反应后,气球状态也如上图所示,则试管b中反应的离子方程式为___________。
(3)分析判断,实验________[填“(1)”或“(2)”]能证明镁的金属性强于铝。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,单质只作氧化剂的是
A.2F2+2H2O═4HF+O2↑
B.Cl2+2NaOH═NaCl+NaClO+H2O
C.2Na+2H2O═2NaOH+H2↑
D.H2+CuO![]() H2O+Cu
H2O+Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状态下,气态分子断开1 mol化学键的焓变称为键焓。已知H—H、H—O和O===O键的键焓ΔH分别为436 kJ·mol-1、463 kJ·mol-1和495 kJ·mol-1。下列热化学方程式正确的是
A. H2O(g)===H2+1/2O2(g)ΔH=-485 kJ·mol-1
B. H2O(g)===H2(g)+1/2O2(g) ΔH=+485 kJ·mol-1
C. 2H2(g)+O2(g)===2H2O(g) ΔH=+485 kJ·mol-1
D. 2H2(g)+O2(g)===2H2O(g) ΔH=-485 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是接触法生产硫酸的催化剂,属于两性氧化物,可从富钒炉渣(主要含有
是接触法生产硫酸的催化剂,属于两性氧化物,可从富钒炉渣(主要含有![]() 、
、![]() 和少量
和少量![]() 、
、![]() )中提取,其工艺流程如下:
)中提取,其工艺流程如下:
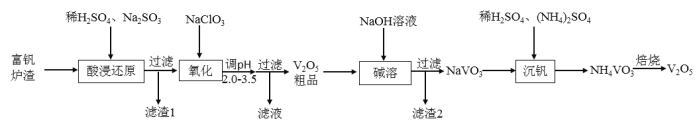
已知:①![]()
②一些金属阳离子沉淀的pH范围:
开始沉淀pH | 完全沉淀pH | |
| 6.5 | 9.0 |
| 2.2 | 3.5 |
| 4.1 | 5.4 |
(1)“酸浸还原”时![]() 转化为
转化为![]() ,写出有关
,写出有关![]() 反应的离子方程式________;经“氧化”后钒以
反应的离子方程式________;经“氧化”后钒以![]() 存在,写出生成
存在,写出生成![]() 反应的离子方程式________。
反应的离子方程式________。
(2)调节溶液![]() 至2.0~3.5,宜选用的试剂是________(填标号)。/span>
至2.0~3.5,宜选用的试剂是________(填标号)。/span>
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(3)“滤渣1”的主要成分是________;![]() 粗品中的杂质为________。
粗品中的杂质为________。
(4)“沉钒”时需加入稀![]() ,其目的是________。
,其目的是________。
(5)焙烧产生的气体用________吸收后,其产物可以在该工艺中循环利用。
(6)![]() 在一定条件下可转化为不同价态的钒离子(
在一定条件下可转化为不同价态的钒离子(![]() 、
、![]() 、
、![]() 、
、![]() ),可作为全钒液充电流电池的电极液,电池总反应为
),可作为全钒液充电流电池的电极液,电池总反应为![]() 。下图是钒电池基本工作原理示意图:
。下图是钒电池基本工作原理示意图:
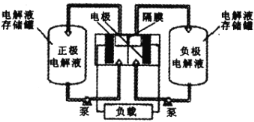
充电时阳极的反应式为____;能够通过钒电池基本工作原理示意图中“隔膜”的离子是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示,其中M单质为淡黄色固体。下列说法错误的是( )。

A.简单离子半径:Z>R
B.元素非金属性的顺序:Z>X>Y
C.M的氧化物对应的水化物均为强酸
D.Y的单质在加热条件下能与Z的最高价氧化物对应的水化物的浓溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T0℃时,在2 L的密闭容器中发生反应:X(g)+Y(g)![]() Z(g)(未配平),各物质的物质的量随时间变化的关系如图a所示。其他条件相同,温度分别为T1℃、T2℃时发生反应,X的物质的量随时间变化的关系如图b所示。下列叙述正确的是( )
Z(g)(未配平),各物质的物质的量随时间变化的关系如图a所示。其他条件相同,温度分别为T1℃、T2℃时发生反应,X的物质的量随时间变化的关系如图b所示。下列叙述正确的是( )
图a 图b
图b
A.该反应的正反应是吸热反应
B.T1℃时,若该反应的平衡常数K =50,则T1<T0
C.图a中反应达到平衡时,Y的转化率为37.5%
D.T0℃,从反应开始到平衡时:v(X)=0.083 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以熔融![]() 和
和![]() 为电解质,天然气经重整催化作用提供反应气的燃料电池如图。下列说法正确的是
为电解质,天然气经重整催化作用提供反应气的燃料电池如图。下列说法正确的是
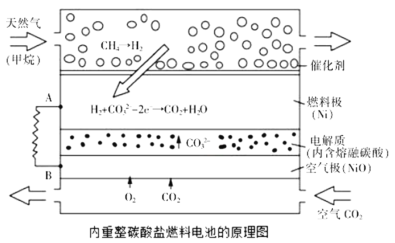
A.当外电路中通过![]() 电子时,将消耗
电子时,将消耗![]()
B.通天然气的电极为负极,发生还原反应
C.该电池使用过程中需补充![]() 和
和![]()
D.以此电池为电源电解精炼铜,当有![]() 转移时,有
转移时,有![]() 铜析出
铜析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的容器中加入一定量的A和B,发生反应∶2A(g)+B(g)![]() 2C(g), 在相同时间内,测得不同温度下A的转化率如下表所示,下列说法正确的是
2C(g), 在相同时间内,测得不同温度下A的转化率如下表所示,下列说法正确的是
温度/°C | 100 | 200 | 300 | 400 | 500 |
转化率 | 30% | 75% | 75% | 50% | 18% |
A.该反应随着温度升高,反应速率先变大后变小
B.200°C,A的转化率为75%时,反应达到平衡状态
C.当单位时间内生成n mol B的同时消耗2n molC时,反应达到平衡状态
D.400°C时,B的平衡浓度为0.5 mol/L,则该反应的平衡常数K=2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com