
【题目】阿伏加德罗常数的值为NA。下列说法正确的是
A. 标准状况下,11.2 L四氯化碳中含有的共价键数为2NA
B. 20g T218O分子中含有的中子数为10N A
C. 0.1 mol NO与O2的混合气体中,所含原子总数为0.2 NA
D. 0.1 mol KI与0.1 mol FeCl3在溶液中反应,转移的电子数为0.1 NA
【答案】C
【解析】A项,CCl4在标准状况下呈液态,无法用22.4L/mol计算CCl4物质的量;B项,T218O的摩尔质量为24g/mol,1个T218O分子中含14个中子;C项,根据原子守恒作答;D项,KI与FeCl3的反应为2I-+2Fe3+![]() I2+2Fe2+,该反应为可逆反应。
I2+2Fe2+,该反应为可逆反应。
A项,CCl4在标准状况下呈液态,无法用22.4L/mol计算CCl4物质的量,A项错误;B项,T218O的摩尔质量为24g/mol,n(T218O)=![]() =
=![]() mol,1个T218O分子中含14个中子,20gT218O中含有中子物质的量为
mol,1个T218O分子中含14个中子,20gT218O中含有中子物质的量为![]() mol
mol![]() 14=
14=![]() mol,B项错误;C项,NO与O2都是双原子分子,根据原子守恒,0.1molNO与O2的混合气体中所含原子物质的量为0.2mol,C项正确;D项,KI与FeCl3的反应为2I-+2Fe3+
mol,B项错误;C项,NO与O2都是双原子分子,根据原子守恒,0.1molNO与O2的混合气体中所含原子物质的量为0.2mol,C项正确;D项,KI与FeCl3的反应为2I-+2Fe3+![]() I2+2Fe2+,该反应为可逆反应,0.1molKI与0.1molFeCl3的反应中转移电子物质的量小于0.1mol,D项错误;答案选C。
I2+2Fe2+,该反应为可逆反应,0.1molKI与0.1molFeCl3的反应中转移电子物质的量小于0.1mol,D项错误;答案选C。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】烯烃被酸性高锰酸钾溶液氧化的规律是,双键两端的基团=CH2变成CO2 , =CHR变成RCOOH, ![]() 变成
变成 ![]() ,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( )
,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( )
A.只有CH3COOH
B.CO2和 CH3COCH3
C.CO2和CH3CH2COOH
D.HCOOH和CH3CH2COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 78gNa2O2固体中含有的离子数之和为3NA
B. 标准状况下22.4LCl2通入足量水中,反应中转移的电子数为NA
C. 18gD2O所含有的质子数、电子数均为10NA
D. pH=1的醋酸溶液中含有的H+数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核黄素又称为维生素B2 , 可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳.核黄素分子的结构为  已知:
已知: ![]()
有关核黄素的下列说法中,不正确的是( )
A.该化合物的分子式为C17H22N4O6
B.酸性条件下加热水解,有CO2生成
C.酸性条件下加热水解,所得溶液加碱后有NH3生成
D.能发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两个烧杯里的溶液为同浓度的稀硫酸,甲中G为电流计。经过一段时间后,以下说法中正确的是
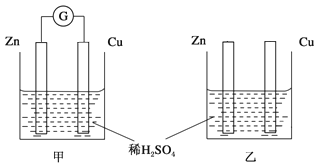
A. 两烧杯中铜片表面均无气泡产生
B. 甲中铜片是阳极,乙中铜片是负极
C. 甲中电子从锌片经溶液流向铜片,实现化学能转化为电能,而乙中实现化学能转化为热能
D. 产生气泡的速率甲比乙快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】E的产量是衡量一个国家石油化工水平发展的标志,F为高分子化合物,能进行如图所示的反应. 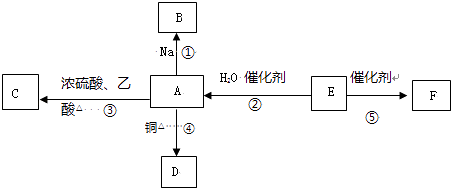
(1)请写出E的电子式 .
(2)下列反应的化学方程式:(要求有机物必须写结构简式) 反应②: 反应类型 .
反应④:反应类型 .
反应⑤:反应类型 .
(3)比较反应①剧烈程度(填>、=或<)钠和水反应的烈程度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】沉淀转化广泛应用于工业生产和科学实验。为了探究AgCl、Ag2S(黑色)的溶解性及转化等相关性质,做以下实验:
步 骤 | 现 象 |
Ⅰ.将NaCl溶液滴入AgNO3溶液中至恰好完全反应。 | 产生白色沉淀。 |
Ⅱ.过滤出Ⅰ中的白色沉淀置于试管中,在试管中加入过量Na2S溶液并充分振荡。 | 白色沉淀变为黑色。 |
Ⅲ.过滤出Ⅱ中的黑色沉淀置于试管中,在试管中加入过量的NaCl溶液并充分振荡后静置。 | 沉淀由黑色最后完全变为乳白色。 |
回答下列问题:
(1)Ⅰ中的白色沉淀是__________。
(2)写出Ⅱ中沉淀变黑的离子方程式__________ ,沉淀转化的主要原因是______________。
(3)滤出步骤Ⅲ中的乳白色沉淀,加入过量的浓HNO3使之充分反应,有红棕色气体生成,尚有部分沉淀未溶解,过滤得到滤液X和白色沉淀Y。
ⅰ.向X中滴加Ba(NO3)2溶液,产生白色沉淀;
ⅱ.将Y与足量的KI溶液充分混合,白色沉淀最终转化为黄色沉淀。
① 由ⅰ判断,滤液X中被检出的离子是_______。
② 由ⅰ、ⅱ可确认步骤Ⅲ中乳白色沉淀含有__________和__________。
(4)为了证明实验步骤Ⅲ中的黑色沉淀只有在NaCl存在下,才能和氧气反应转化为乳白色沉淀,设计了如下对照实验并将实验结果记录在右侧的表格中。
装置 | 实验结果 |
B | 一段时间后,出现乳白色沉淀 |
C | 一段时间后,无明显变化 |
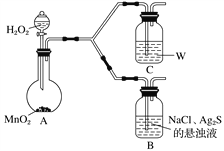
①A中,盛有MnO2的玻璃仪器名称是_________________。
②C中盛放的是物质W的悬浊液,W是________(填化学式)。
③请完成B中发生反应的反应式并配平:_____
Ag2S+ + + H2O![]() AgCl+ + NaOH
AgCl+ + NaOH
________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有些朋友看一眼就喜欢了。关于图所示原电池的说法正确的是
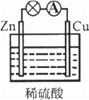
A. Cu为正极,Zn为负极
B. 电子由铜片通过导线流向锌片
C. 正极反应式为Cu-2e- = Cu2+
D. Zn发生还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com