
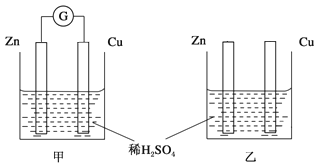
【题目】两个烧杯里的溶液为同浓度的稀硫酸,甲中G为电流计。经过一段时间后,以下说法中正确的是
A. 两烧杯中铜片表面均无气泡产生
B. 甲中铜片是阳极,乙中铜片是负极
C. 甲中电子从锌片经溶液流向铜片,实现化学能转化为电能,而乙中实现化学能转化为热能
D. 产生气泡的速率甲比乙快
【答案】D
【解析】甲装置为原电池,乙装置不是原电池。由于Zn比Cu活泼,甲装置中Zn为负极,Zn极电极反应式为Zn-2e-=Zn2+,Cu为正极,Cu极电极反应式为2H++2e-=H2↑,电子由锌片通过导线流向铜片;乙装置中Zn片上发生反应Zn+H2SO4=ZnSO4+H2↑。
甲装置为原电池,乙装置不是原电池。A项,由于Zn比Cu活泼,甲装置中Cu为正极,Cu极电极反应式为2H++2e-=H2↑,甲装置中Cu片表面有气泡产生,乙装置中Cu与稀硫酸不反应,Cu片上没有气泡产生,A项错误;B项,甲中铜片为正极,乙不是原电池,B项错误;C项,甲中Zn为负极,Cu为正极,电子由锌片经导线流向铜片,实现化学能转化为电能,乙装置中Zn片上发生反应Zn+H2SO4=ZnSO4+H2↑,实现化学能转化为热能,C项错误;D项,甲形成原电池,乙不是原电池,产生气泡的速率甲比乙快,D项正确;答案选D。


科目:高中化学 来源: 题型:
【题目】化学与生活、生产密切相关,下列说法错误的是( )
A.以电解饱和食盐水制取氯气等产品的工业称为“氯碱工业”
B.氯气可用来对自来水杀菌消毒
C.碘化银可用于人工降雨
D.为了消除碘缺乏病,在食用盐中加入一定量的碘单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有水参与或生成的反应不属于取代反应的是( )
A.CH2═CH2+H2O ![]() CH3CH2OH
CH3CH2OH
B.![]()
C.CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
D.CH3CH2Cl+H2O ![]() CH3CH2OH+HCl
CH3CH2OH+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)被称为第三代半导体材料,其应用已经取得了突破性的进展。
已知:(i)氮化镓性质稳定,不与水、酸反应,只在加热时溶于浓碱。
(ii)NiCl2 溶液在加热时,先转化为Ni(OH)2,后分解为NiO。
(iii)制备氮化镓的反应为:2Ga+2NH3![]() 2GaN+3H2
2GaN+3H2
某学校化学兴趣小组实验室制备氮化镓,设计实验装置如图所示:

设计实验步骤如下:
①滴加几滴NiCl2 溶液润湿金属镓粉末,置于反应器内。
②先通入一段时间后的H2,再加热。
③停止通氢气,改通入氨气,继续加热一段时间。
④停止加热,继续通入氨气,直至冷却。
⑤将反应器内的固体转移到盛有盐酸的烧杯中,充分反应过滤、洗涤、干燥。
(1)仪器X中的试剂是___________,仪器Y的名称是__________________。
(2)指出该套装置中存在一处明显的错误是________________________。
(3)步骤①中选择NiCl2 溶液,不选择氧化镍的原因是____________________。
a.增大接触面积,加快化学反应速率
b使镍能均匀附着在镓粉的表面,提高催化效率
c.为了能更好形成原电池,加快反应速率
(4)步骤③中制备氮化镓,则判断该反应接近完成时观察到的现象是____________________。
(5)请写出步骤⑤中检验产品氮化镓固体洗涤干净的操作________________________。
(6)镓元素与铝同族,其性质与铝类似,请写出氮化镓溶于热NaOH溶液的离子方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷的分子结构可简写成键线式结构 ![]() ,有机物A的键线式结构为
,有机物A的键线式结构为 ![]() ,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是( )
,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是( )
A.有机物A的一氯取代物只有4种
B.用系统命名法命名有机物A,名称为2,2,3﹣三甲基戊烷
C.有机物A的分子式为C8H18
D.B的结构可能有3种,其中一种名称为3,4,4﹣三甲基﹣2﹣戊烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA。下列说法正确的是
A. 标准状况下,11.2 L四氯化碳中含有的共价键数为2NA
B. 20g T218O分子中含有的中子数为10N A
C. 0.1 mol NO与O2的混合气体中,所含原子总数为0.2 NA
D. 0.1 mol KI与0.1 mol FeCl3在溶液中反应,转移的电子数为0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示各组物质间反应的化学(离子)方程式的是
A. 铜与浓硝酸:Cu+4H++2NO3- =Cu2++2NO2↑+2H2O
B. 氯化铵与氢氧化钠两种稀溶液:NH4++OHˉ=NH3↑+H2O
C. 铜与浓硫酸:Cu+2H2SO4(浓) =CuSO4+SO2↑+2H2O
D. 用稀HNO3溶解FeS固体:FeS+2H+=Fe2++H2S↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。根据表中所列①~⑨元素,请按要求回答下列问题:
⑩ | ||||||||
① | ② | ③ | ||||||
④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素①形成的最高价氧化物的电子式为__________ ,⑤⑨两种元素形成的化合物的电子式为__________,①~⑨元素的最高价氧化物的水化物酸性最强的是__________ (填化学式)。
(2)①、⑦两种元素的最高价氧化物的熔点较高的是___________(填化学式)。
(3)由②③⑩三种元素组成的离子化合物中所含有的化学键有____________ 。
(4)①的单质与②的最高价氧化物的水化物的浓溶液反应的化学方程式为____________________。
(5)下列事实能说明③非金属性比⑧强的有___________。
a.③的单质与⑧的氢化物溶液反应,溶液变浑浊
b.③⑧形成简单离子时,得电子数目的多少
c.③与⑧两元素的简单氢化物受热分解,前者的分解温度高
d.③原子半径比⑧小
e.③与⑧两元素的简单氢化物的沸点,前者高
Ⅱ. 短周期元素W、X、Y、Z的原子序数依次增大。m、p、q、r、s是由这些元素组成的二元化合物,常温常压下r为液体,其余均为无色气体, m 的摩尔质量为p的2倍,n是元素Y的单质, p物质能使湿润的红色石蕊试纸变蓝,q能使品红溶液褪色。上述的转化关系如图所示。下列说法正确的是__________ 。

A.原子半径:Y< X< Z
B.非金属性:Y> X> W
C.q与s均为酸性氧化物
D.常温下,m与q,n与s均不能共存
E.若n过量,q还可以继续燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某主族元素R的最高正化合价与最低负化合价的代数和为4,下列有关叙述正确的是
A.R一定是第4周期元素
B.R的气态氢化物化学式为H2R
C.R的气态氢化物比同周期其他元素的气态氢化物稳定
D.R的气态氢化物的水溶液显碱性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com