
【题目】(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H﹤0
CH4(g)+2H2O(g) △H﹤0
则升高温度平衡体系中H2的体积分数将___________;(选填“增大”、“减小”或“不变”)
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[CO2]/mol·L-1 | [H2]/mol·L-1 | [CH4]/mol·L-1 | [H2O]/mol·L-1 | |
平衡Ⅰ | a | b | c | d |
平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为_________。
(3)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3-![]() H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。____________________
H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。____________________
(4)查阅资料获知如下信息:
i.H2CO3:Ki1=4.3×10-7,Ki2=5.6×10-11(以Ki1为主)
ii.标况下,CO2的溶解度为约为1:1
iii.H2O+CO2 ![]() H2CO3
H2CO3 ![]()
iv. ![]()
![]()
![]() ㏒(6)=0.8
㏒(6)=0.8
请尝试估算:
①饱和二氧化碳溶液中碳酸的物质的量浓度c(H2CO3)约为_______________mol/L;
②饱和二氧化碳溶液中碳酸的电离度α约为_____________。
③正常雨水的pH约为____________。
【答案】(1)增大;(2)![]()
(3)当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液中的pH基本不变;当少量碱性物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变。
(4)① 7.5×10-5mol/L;②电离度α约为7.7×10-2;③5.2
【解析】
试题分析:(1)反应:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H﹤0,升高温度,平衡逆向移动,平衡体系中H2的体积分数将增大;
CH4(g)+2H2O(g) △H﹤0,升高温度,平衡逆向移动,平衡体系中H2的体积分数将增大;
(2)化学平衡常数等于生成物平衡浓度系数次幂的积与反应物平衡浓度系数次幂的积的比值。相同温度时,反应的平衡常数不变。根据表中数据知a、b、c、d与m、n、x、y之间的关系式为![]() 。
。
(3)人体血液中存在平衡:H++ HCO3-![]() H2CO3,当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液中的pH基本不变;当少量碱性物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变。
H2CO3,当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液中的pH基本不变;当少量碱性物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变。
(4)①标况下,CO2的溶解度为约为1:1,即1L水中溶解1LCO2,物质的量为0.045mol,CO2的浓度约为0.045mol/L,又H2O+CO2![]() H2CO3 的平衡常数K=c(H2CO3)/c(CO2)=1/600,饱和二氧化碳溶液中碳酸的物质的量浓度c(H2CO3)约为7.5×10-5mol/L ;②H2CO3:Ki1=4.3×10-7,Ki2=5.6×10-11(以Ki1为主),即c(H+)c(HCO3—)/ c(H2CO3)= 4.3×10-7,c(H+)=c(HCO3—),则c2(H+)=32×10-12,c(H+)=6×10-6,饱和二氧化碳溶液中碳酸的电离度α约为(5.6×10-6)÷7.5×10-5=7.7×10-2;③c(H+)=5.6×10-6正常雨水的pH=lgc(H+)=5.2。
H2CO3 的平衡常数K=c(H2CO3)/c(CO2)=1/600,饱和二氧化碳溶液中碳酸的物质的量浓度c(H2CO3)约为7.5×10-5mol/L ;②H2CO3:Ki1=4.3×10-7,Ki2=5.6×10-11(以Ki1为主),即c(H+)c(HCO3—)/ c(H2CO3)= 4.3×10-7,c(H+)=c(HCO3—),则c2(H+)=32×10-12,c(H+)=6×10-6,饱和二氧化碳溶液中碳酸的电离度α约为(5.6×10-6)÷7.5×10-5=7.7×10-2;③c(H+)=5.6×10-6正常雨水的pH=lgc(H+)=5.2。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是一种化学电源,如图所示,以石墨为电极,两极分别通入氢气和氧气,KOH溶液为电解质溶液,下列说法不正确的是( )

A. 在电池反应中每转移2mol电子,正极消耗O2的体积为11.2L
B. b极的电极反应式为:O2+2H2O+4e-=4OH-
C. 工作一段时间后,电解质溶液碱性减弱
D. 该装置将化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填写下列问题:
(1)某些共价化合物(如H2O、NH3、N2O4等)在液态时会发生微弱的电离,如:2H2O ![]() H3O+ + OH—,则液态NH3电离的方程式是________________
H3O+ + OH—,则液态NH3电离的方程式是________________
(2)某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH=12,则该温度下水的KW= ,在此温度下,将pH=b的NaOH溶液Vb L与pH=a的H2SO4溶液Va L混合,若所得混合液为中性,且a+b=13,则Va:Vb=_________
(3)若在0.10 molL-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是 ,在0.10 molL-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=___________(已知Ksp[Cu(OH) 2]=2.2x10-20)。
(4)在常温下,中和相同体积,相同pH的Ba(OH)2、NH3H2O、NaOH三种稀溶液所用相同浓度的盐酸的体积分别为V1、V2、V3,则三种关系为 (用“V1、V2、V3”和“>、<、=”表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向 100 mL0.01 mol·L-1HA 溶液中逐滴加入0.02 mol·L-1MOH 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
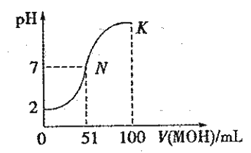
(1)由图中信息可知HA为 酸(填“强”或“弱”)。
(2)常温下一定浓度的MA稀溶液的pH = a,则a______________7(填“ > ”、“,< ”或“=”),用离子方程式表示其原因: _____________________,此时,溶液中由水电离出的c(OH-)=_________
(3)请写出K点所对应的溶液中离子浓度的大小关系______________________。
(4)K点对应的溶液中,溶液的 pH = 10,则 c(MOH) +c(OH-) =_________________mol· L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:aA(g)+bB(g)![]() cC(g)+dD(g);根据图回答:
cC(g)+dD(g);根据图回答:

(1)压强p1比p2 (填“大”或“小”)
(2)(a+b)比(c+d) (填“大”或“小”)
(3)温度t1比t2℃ (填“高”或“低”)
(4)正反应为 热反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.炒过菜的铁锅为及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
(1)铁锅的锈蚀是 腐蚀(填“析氢“或“吸氧”)。
(2)写出铁锅腐蚀时正极的电极反应式: 。
II.①某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑。请画出能够实验这一反应的装置图。
②某同学在做一定条件下铜与稀硫酸的反应实验时,看到碳棒上有气泡产生,但铜棒却没有被腐蚀。请你分析其原因:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,如果取0.1molL-1HA溶液与0.1molL-1NaOH溶液等体积混合,测得混合液的pH=8。混合液中由水电离出的OH-浓度与0.1molL-1NaOH溶液中由水电离出的OH-浓度之比为__________.
(2)相同温度下,将足量硫酸钡固体分别放入相同体积的
①0.1molL-1硫酸铝溶液
②0.1molL-1氯化钡溶液
③蒸馏水
④0.1molL-1硫酸溶液中,
Ba2+浓度由大到小的顺序是 。(用序号填写)
(3)常温下,将a molL-1的氨水与0.1molL-1的盐酸等体积混合,当溶液中c(NH4+)=c(Cl-)时,用含a的代数式表示NH3H2O的电离常数Kb= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原子结构及元素周期律的知识,下列推断正确的是
A. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
B. 核外电子排布相同的微粒化学性质也相同
C. Cl-、S2-、Ca2+、K+半径逐渐减小
D. ![]() 与
与![]() 得电子能力相同
得电子能力相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com