
����Ŀ�����ΪԪ�����ڱ���һ���֣�����a��f�������ֶ���������Ԫ�ء����������գ�
a | b | c |
d | e | f |
��1������Ԫ���У�ԭ�Ӱ뾶������____(��Ԫ�ر��)��d��e��f����Ԫ�ص�ԭ�ӽṹ�ϵ���ͬ����___��
��2����a����̬�⻯���ˮ��Һ�ʼ��ԣ���a����̬�⻯��ĵ���ʽ��____������Ԫ���У�����������Ӧˮ�����������ǿ����____(��Ԫ�ط���)��
��3����fԪ�ص�ԭ��L���������M���������1������eԪ�صķǽ����Ա�fԪ�صķǽ�����_____(ѡ����ǿ������������)��
��4����bΪ�ǽ���Ԫ�أ��������ƶ���ȷ����____(ѡ����)��
��aһ���ǽ���Ԫ�� ��dһ���ǽ���Ԫ�� ��fһ���Ƿǽ���Ԫ��
���𰸡�d ���Ӳ�����ͬ ![]() Cl �� ��
Cl �� ��
��������
��������Ԫ�ض�Ϊ������Ԫ�أ���a��b��cΪ�ڶ�����Ԫ�أ�����Ԫ�������ڱ����������ڣ�d��e��fΪ��������Ԫ�أ��������ڱ����������ڡ��ڽ���Ԫ�����ʷ���ʱ���ɽ�Ԫ�������ڱ��н��ж�λ��Ҳ�����ý�����ǽ����ķֽ��߽����жϡ�
(1) ����Ԫ���У�ԭ�Ӱ뾶����Ԫ���ǵ��Ӳ����ࡢλ�����·���Ԫ�أ���Ϊd����Ϊd��
d��e��f����Ԫ��λ��ͬһ���ڣ����ǵĵ��Ӳ�����ͬ�������������������ࡣ��Ϊ���Ӳ�����ͬ��
(2) ��a����̬�⻯���ˮ��Һ�ʼ��ԣ���aΪ��Ԫ�أ�����̬�⻯��ĵ���ʽΪ![]() ����Ϊ
����Ϊ![]() ��
��
����Ԫ���У�����������Ӧˮ����������ǿ��Ԫ��Ӧλ�����Ͻ�λ�õ�Ԫ�ء�����aΪNԪ�ؽ����ƶϣ�cΪF����F�����ۣ�����fΪCl������������Ӧˮ����������ǿ����ΪHClO4����ΪCl��
(3)��fԪ�ص�ԭ��L���������M���������1������ΪCl����eԪ��ΪS�����ķǽ����Ա�fԪ�صķǽ�����������Ϊ����
(4) ��bΪ�ǽ���Ԫ�أ����ݽ�����ǽ����ķֽ��߽����жϣ�c��fһ���Ƿǽ���Ԫ�ء�
��aλ��b��ǰ�棬�����ǽ���Ԫ�أ�Ҳ�����Ƿǽ���Ԫ�أ�����ȷ��
��dλ��b�����·��������ǽ���Ԫ�أ�Ҳ�����Ƿǽ���Ԫ�أ�����ȷ��
��������ɷ�����fһ���Ƿǽ���Ԫ�أ���ȷ��
��Ϊ�ۡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ��������������ȷ���ǣ� ��
A. �����£�1 L 0.1 mol��L��1 MgCl2��Һ�к�Mg2+��Ϊ0.1NA
B. ���³�ѹ�µ�33.6 L Cl2��27g Al��ַ�Ӧ��ת�Ƶ�����Ϊ3 NA
C. 1mol������������ʱһ��ʧȥ3NA������
D. �����£�2.7g�������������ᷴӦ��ʧȥ�ĵ�����Ϊ0.3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ζ�������һ�ֲ�����㡢ȷ�ȺܸߵĶ����������������ɹ㷺Ӧ�����к͵ζ���������ԭ��Ӧ�ȵζ��С�ij�о���ѧϰС���ͬѧ���õζ��������������������������
��1���ⶨNaOH��Na2CO3�Ļ��Һ��NaOH�ĺ�����ʵ�����Ϊ������Һ�мӹ�����BaCl2��ҺʹNa2CO3��ȫת����BaCO3������Ȼ���ñ�����ζ�(�÷�̪��ָʾ��)��
�������BaCO3������NaOH��Һ��ֱ�ӵ������ᣬ���յ���ɫ�ı仯Ϊ____��Ϊ�δ�������ܲ��NaOH�ĺ�����____��
�ڵζ�ʱ�����ζ����еĵζ�Һһֱ�½����������Ŵﵽ�ζ��յ㣬���ܷ��ɴ�ȷ�ؼ���������____����˵�����ɣ�___��
��2���ⶨijƷ�Ƶĵ���(���е����)�е�Ԫ�صİٷֺ�����ȷ��ȡ5.0000g�õ��Σ���������ˮ��Ȼ����������KI��Һ�����������»��(�����ķ�ӦΪKIO3��3H2SO4��5KI��3K2SO4��3I2��3H2O)����ַ�Ӧ�����Һϡ����250 mL��Ȼ����5.0��10��4mol��L��1��Na2S2O3����Һ���еζ�(�õ�����ָʾ������ӦΪI2��2S2O32-��2I����S4O62-)��ȡ��Na2S2O3�ı���ҺӦ����_____ʽ�ζ��ܡ��й�ʵ����ֵ�����ʾ(��һ�εζ��յ��������ͼ��ʾ���뽫���õ������������)��
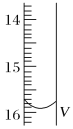
�ζ����� | ����Һ�����(mL) | �ζ�ǰ�Ķ���(mL) | �ζ���Ķ���(mL) |
��һ�� | 25.00 | 0.00 | V��_____ |
�ڶ��� | 25.00 | 0.00 | 14.99 |
������ | 25.00 | 0.00 | 15.01 |
�õ����е�Ԫ�صİٷֺ���Ϊ_____�����в����У��ᵼ������õĵ�Ԫ�صİٷֺ���ƫ�����____��
a���ζ��յ�ʱ�����ӿ̶�
b��û����Na2S2O3����Һ��ϴ��Ӧ�ĵζ���
c����ƿ��������������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������200 mL MgCl2��AlCl3�����Һ������Mg2+Ũ��0.2mol/L�� Cl��Ũ��Ϊ1.3 mol/L��ҪʹMg2+ת����Mg(OH)2��ʹMg2+��Al3+���뿪����������Ҫ4 mol/L NaOH��Һ(����)
A. 80mLB. 100mLC. 120mLD. 140mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NaOH��AlCl3��MgCl2���ֹ�����ɵĻ��������������ˮ�У���0.58g��ɫ���������������õ���Һ���μ���0.5 mol��L-1�����ᣬ�����������������ɳ�����������ͼ��ʾ������ʾ��Na[Al(OH)4]+HCl��Al(OH)3��+NaCl+H2O��
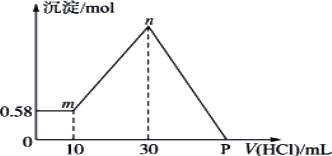
��1���������NaOH��������________g��AlCl3��������________g��MgCl2��������________g��
��2��P������ʾ������������________ mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ��ȷ���ǣ� ��
A.�����ȼ����Ϊ890.3kJ/mol�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪCH4(g)+2O2(g)![]() CO2(g)+2H2O(g) ��H=��890.3kJ/mol
CO2(g)+2H2O(g) ��H=��890.3kJ/mol
B.��200�桢101KPaʱ��H2���������������1 mol HI�ų�����7.45kJ�����Ȼ�ѧ����ʽΪI2(g)+H2(g)=2HI(g) ��H=��14.9kJ/mol
C.��֪��101kPa�£�1gH2ȼ������ˮ�����ų�121kJ���������Ȼ�ѧ����ʽΪH2(g)+![]() O2(g)=H2O(g) ��H=��242kJ/mol
O2(g)=H2O(g) ��H=��242kJ/mol
D.25�棬101kPaʱ��ǿ����ǿ���ϡ��Һ�����кͷ�Ӧ���к���Ϊ57.3kJ/mol����ʾ������Һ������������Һ��Ӧ���к��ȵ��Ȼ�ѧ����ʽΪH2SO4(aq)+2KOH(aq)=K2SO4(aq)+2H2O(l) ��H=��114.6kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�Dz��ֶ�����Ԫ��ԭ�Ӱ뾶��ԭ�������Ĺ�ϵ��������˵����ȷ����
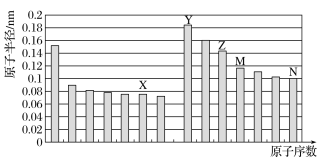
A.M�����ڱ��е�λ��Ϊ���������ڣ�IV��
B.Y��N�γɵĻ�����Ϊ���ӻ�����
C.X��N����Ԫ�ص���̬�⻯��ķе���ȣ�ǰ�߽ϵ�
D.YԪ�غ�XԪ�ؿ����γ�Y2X2�ͻ�����������������ʵ���֮��Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ʻ���(COS)����Ϊһ����ʳѬ�������ܷ�ֹijЩ���桢�߳�������Σ������2L�����ܱ������У���CO��H2S��ϼ��Ȳ��ﵽ����ƽ�⣺CO(g)��H2S(g)![]() COS(g)��H2(g) K��0.1����ӦǰCO���ʵ���Ϊ10mol��2min�ﵽƽ���CO���ʵ���Ϊ8mol������˵����ȷ���ǣ� ��
COS(g)��H2(g) K��0.1����ӦǰCO���ʵ���Ϊ10mol��2min�ﵽƽ���CO���ʵ���Ϊ8mol������˵����ȷ���ǣ� ��
A.�����¶ȣ�H2SŨ�����ӣ������÷�Ӧ�����ȷ�Ӧ
B.ͨ��CO������Ӧ����������
C.��ӦǰH2S���ʵ���Ϊ7mol
D.CO��ƽ����Ӧ����Ϊ0.5mol/(L��s)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ҫ�������Ƹ�Ѫѹ���Ѫ������˥�ߣ���ϳ�·�����£�
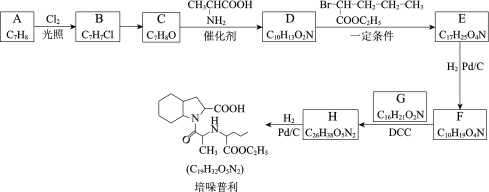
��֪������ ![]()
����DCC��һ�ֺ�ǿ����ˮ����
(1)������A��������___________________��
(2)B��C������Լ���������________________��
(3)C��D�Ļ�ѧ����ʽ��____________________��
(4)D��E�ķ�Ӧ������______________________��
(5)F�Ľṹ��ʽ��____________________________��
(6)K���ڻ����칹��K����G��������·�ߺϳɣ�

��X������Ԫ����̼̼˫������ṹ��ʽ��______��
�������ϳ�����������·���У���Yת��ΪG������F��Ӧ������ֱ����Y����ҪĿ����______����ϳ�·����______________����ĸ����ת��Ŀ����ͬ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com