
【题目】Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同的粉末状和块状的MnO2分别加入盛有15 ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(1)写出上述实验中发生反应的化学方程式: 。
(2)实验结果表明,催化剂的催化效果与 有关。
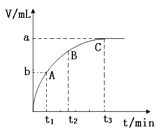
(3)某同学在10 mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的反应速率最慢的是 。
Ⅱ.某反应在体积为5L的恒容密闭容器中进行, 在0-3分钟内各物质的量的变化情况如右下图所示(A,B,C均为气体,且A气体有颜色)。
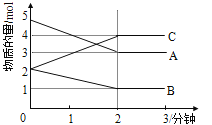
(4)该反应的的化学方程式为 。
(5)反应开始至2分钟时,B的平均反应速率为 。
(6)能说明该反应已达到平衡状态的是 。
a.v(A)= 2v(B) b.容器内各物质的物质的量相等
c.v逆(A)=v正(C) d.容器内气体的颜色保持不变
(7)由图求得平衡时A的转化率为 。
【答案】(1)2H2O2 ![]() 2H2O + O2↑ (2)催化剂的表面积(3)C(4)2A + B
2H2O + O2↑ (2)催化剂的表面积(3)C(4)2A + B ![]() 2C(写等号不得分)(5)0.1mol·(L·min)-1(6)cd (7)40%
2C(写等号不得分)(5)0.1mol·(L·min)-1(6)cd (7)40%
【解析】
试题分析:Ⅰ.(1)H2O2在二氧化锰作催化剂的条件下发生分解反应生成水和氧气,发生反应的化学方程式为2H2O2 ![]() 2H2O + O2↑。
2H2O + O2↑。
(2)实验结果表明,粉末状二氧化锰作催化剂反应剧烈,反应速率较快,故催化剂的催化效果与催化剂的表面积有关。
(3)随着反应的进行,过氧化氢的浓度逐渐减小,反应速率逐渐变慢,则A、B、C三点所表示的反应速率最慢的是C。
Ⅱ.(4)根据题给信息知A、B的物质的量随反应的进行逐渐减小最后不变,C的物质的量随反应的进行逐渐增大,最后不变,则A、B为反应物,C为生成物,反应为可逆反应,A、B、C的物质的量变化分别为2mol、1mol和2mol,则该反应的的化学方程式为2A + B ![]() 2C。
2C。
(5)根据公式v=△n/V△t计算反应开始至2分钟时,B的平均反应速率为0.1mol·(L·min)-1 。
(6)a.没有明确正、逆反应速率,v(A)= 2v(B)不能说明反应达到平衡状态,错误;b.容器内各物质的物质的量相等,反应不一定达到平衡状态,错误;c.v逆(A)=v正(C) ,正、逆反应速率相等,反应达到平衡状态,正确;d.容器内气体的颜色保持不变,A的浓度保持不变,反应达到平衡状态,正确,选cd。
(7)平衡时A的转化率为(5-3)mol/5mol×100%=40%。


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
【题目】2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(37Rb)同周期。下列说法不正确的是
A. In是第五周期第ⅢA族元素
B. 11549In的中子数与电子数的差值为17
C. 原子半径:In>Al
D. 碱性:In(OH)3>RbOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且![]() 的值与温度高低有关。当n(KOH)=a mol,下列有关说法错误的是
的值与温度高低有关。当n(KOH)=a mol,下列有关说法错误的是
A.若某温度下,反应后![]() =11,则溶液中
=11,则溶液中![]() =
=![]()
B.参加反应的氯气的物质的量等于![]() a mol
a mol
C.改变温度,反应中转移电子的物质的量ne的范围:![]() a mol = ne =
a mol = ne = ![]() a mol
a mol
D.改变温度,产物中KClO3的最大理论产量为![]() a mol
a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O![]() Cd(OH)2+2Ni(OH)2有关该电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2有关该电池的说法正确的是( )
A.充电过程中镉元素被氧化
B.充电时阳极反应:Ni(OH)2-e—+ OH—=== NiOOH + H2O
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH—向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,R和T是两种生活中常见的金属单质,C、F是无色无味的气体。
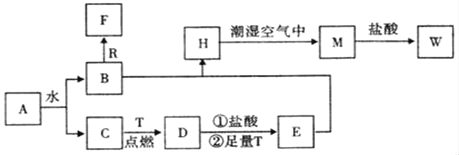
(1)物质A的化学式为_____,D化学式为_____,W的化学式为_____;
(2)B与R反应生成F的离子反应式为___________;
(3)A与CO2反应的化学反应方程式为____________;
(4)H转化为M的化学反应方程式为_____________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质按照纯净物、混合物、电解质和非电解质顺序排列的是 ( )
A. 盐酸、水煤气、醋酸、干冰 B. 冰醋酸、福尔马林、硫酸钠、乙醇
C. 单甘油酯、混甘油酯、苛性钾、石灰石 D. 胆矾、漂白粉、氯化钾、氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化物法生产亚氯酸钠的工艺流程图:
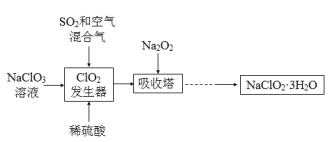
已知:
①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O;
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释至10%以下较安全;
(1)NaClO2中Cl的化合价为______。
(2)在发生器中鼓入SO2和空气混合气的原因是______ (填序号)。
A 空气稀释ClO2以防止爆炸
B SO2将NaClO3氧化成ClO2
C 稀硫酸可以增强NaClO3的氧化性
(3)Na2O2可改为H2O2和NaOH的混合溶液,吸收塔中发生的反应的化学方程式______;吸收塔的温度不能超过20oC,主要原因是______。
(4)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是______ (填序号)。
A 蒸馏 B 蒸发浓缩 C 灼烧 D 过滤 E 冷却结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以惰性电极电解CuSO4和NaCl的混合溶液,两电极上产生的气体(标准状况下测定)体积如下图所示,下列有关说法正确的是

A.a表示阴极上产生的气体,t1前产生的为Cl2
B.原溶液中CuSO4和NaCl物质的量之比为1:1
C.若t2时溶液的体积为1 L,此时溶液的pH为13
D.若原溶液体积为1 L,则原溶液中SO42的物质的量浓度为0.2 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com