
【题目】用石墨作电极,电解盛放在U形管中的饱和NaCl溶液(滴有酚酞溶液),如图。下列叙述正确的是
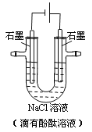
A. 通电后,NaCl发生电离
B. 通电一段时间后,阳极附近溶液先变红
C. 当阳极生成0.1 mol气体时,整个电路中转移了0.1 mol e-
D. 电解饱和食盐水的总反应式为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
【答案】D
【解析】
用石墨作电极电解饱和氯化钠溶液,阴极发生还原反应,电极反应式为:2H2O+2e-=H2↑+2OH-,生成NaOH,该极呈碱性;阳极发生氧化反应,电极反应式为:2Cl--2e-=Cl2↑,总反应为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,以此解答该题。
2NaOH+H2↑+Cl2↑,以此解答该题。
A.NaCl为强电解质,无论是否通电,在溶液中都发生电离,A错误;
B.阳极生成氯气,阴极生成NaOH,则阴极附近溶液先变红,B错误;
C.阳极发生氧化反应,电极反应式为:2Cl--2e-=Cl2↑,生成0.1mol氯气时,转移电子为0.2mol,C错误;
D.电解饱和食盐水,阳极生成氯气,阴极生成氢气和氢氧化钠,总方程式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,D正确。
2NaOH+H2↑+Cl2↑,D正确。
答案选D。


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:
【题目】用下图所示装置除去含有CN-、Cl-废水中的CN-时,控制溶液的pH值为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是

A. 用石墨作阳极,铁作阴极
B. 阳极的电极反应式为:Cl-+2OH--2e-=== ClO-+H2O
C. 阴极附近碱性增强,阳极附近碱性减弱
D. 除去CN-的反应:5ClO-+2CN-+2H+ === N2↑+2CO2↑+5Cl-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu,该反应的原电池的正确组成是( )
正极 | 负极 | 电解质溶液 | |
A | Zn | Cu | CuCl2 |
B | Zn | Cu | ZnCl2 |
C | Cu | Zn | CuSO4 |
D | Cu | Zn | ZnSO4 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸的电离方程式为CH3COOH(aq)![]() H+(aq)+CH3COO-(aq) ΔH>0。25℃时,0.1mol/L醋酸溶液中存在下述关系:Ka=c(H+).c(CH3COO-)/c(CH3COOH)=1.75×10-5,其中的数值是该温度下醋酸的电离平衡常数(Ka)。下列说法正确的是
H+(aq)+CH3COO-(aq) ΔH>0。25℃时,0.1mol/L醋酸溶液中存在下述关系:Ka=c(H+).c(CH3COO-)/c(CH3COOH)=1.75×10-5,其中的数值是该温度下醋酸的电离平衡常数(Ka)。下列说法正确的是
A. 向该溶液中滴加几滴浓盐酸,平衡逆向移动,c(H+)减小
B. 向该溶液中加少量CH3COONa固体,平衡正向移动
C. 该温度下0.01mol/L醋酸溶液Ka<1.75×10-5
D. 升高温度,c(H+)增大,Ka变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种高分子化合物,常用作有机合成的中间体,并可用作乳胶漆等。可以通过以下途径合成:

已知有机物A中含有C、H、O、Cl四种元素且同一个碳原子上不直接连接两个官能团,E是乙醇的同系物,F的分子式为C4H6O2。
完成下列填空:
(1)A的结构简式为______或_________,反应③的反应类型________。
(2)写出反应⑤和反应⑥的化学方程式:
反应⑤___________________;反应⑥_____________。
(3)写出两种与F含有相同官能团的同分异构体的结构简式_______、_______。
(4)试设计一条以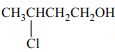 为原料合成
为原料合成![]() 的合成路线。(合成路线常用的表示方式为:
的合成路线。(合成路线常用的表示方式为:![]() )___________________
)___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤块的主要成分是MgCl2,此外还含有Fe3+、Fe2+和Mn2+等离子。若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁。
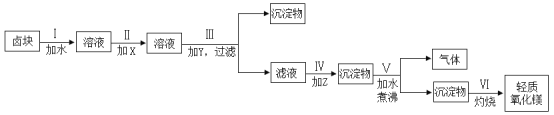
已知1:生成氢氧化物沉淀的pH
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)2 | 7.6 | 9.6 |
Fe(OH)3 | 2.7 | 3.7 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH)2 | 9.6 | 11.1 |
已知2:几种难溶电解质的溶解度(20℃)
物质 | 溶解度/g |
Fe(OH)2 | 5.2×10-5 |
Fe(OH)3 | 3×10-9 |
MgCO3 | 3.9×10-2 |
Mg(OH)2 | 9×10-4 |
(已知:Fe2+氢氧化物呈絮状,不易从溶液中除去)
请回答:
(1)步骤Ⅱ中加入的试剂X为漂液(含25.2%NaClO)。
①用玻璃棒蘸取漂液滴在pH试纸上,pH试纸先变蓝,后褪色。说明漂液具有的性质是________。
②用化学用语表示NaClO溶液使pH试纸变蓝的原因_________。
③步骤Ⅱ中漂液的主要作用是__________。
④若用H2O2代替漂液,发生反应的离子方程式为_________。
(2)步骤Ⅲ中加入的试剂Y为NaOH,应将溶液的pH调节为______,目的是_______。
(3)步骤Ⅳ中加入的试剂Z为Na2CO3,发生反应的离子方程式为_______。
(4)结合化学用语,应用化学平衡移动原理解释步骤Ⅴ中反应发生的原因_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要“持续实施大气污染防治行动,打赢蓝天保卫战。”下列措施不利于“打赢蓝天保卫战”的是
A.推广燃煤脱硫技术,防治SO2污染B.推广使用共享单车,倡导绿色出行
C.研制电动汽车,逐步取代燃油汽车D.加快石油开采速度,加大化石能源供应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、容积为2 L的密闭容器中充入2 mol SO2和一定量O2。发生反应2SO2+O2 ![]() 2SO3,当反应进行到4 min时,测得n (SO2)=0.4 mol。若反应进行到2 min时,容器中SO2的物质的量是
2SO3,当反应进行到4 min时,测得n (SO2)=0.4 mol。若反应进行到2 min时,容器中SO2的物质的量是
A. 等于1.6 mol B. 等于1.2 mol
C. 小于1.2 mol D. 大于1.6 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com