
【题目】在盛有溴水的三支试管中分别加入汽油、四氯化碳和酒精,振荡后静置,出现如图所示的现象。下列说法正确的是( )

A.①加入的是CCl4,②加入的是汽油,③加入的是酒精
B.①加入的是酒精,②加入的是CCl4,③加入的是汽油
C.①加入的是汽油,②加入的是酒精,③加入的是CCl4
D.①加入的是汽油,②加入的是CCl4,③加入的是酒精
科目:高中化学 来源: 题型:
【题目】有机物K是一种治疗缺血性脑卒药物,其合成路线如下:
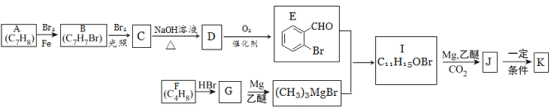
已知:ⅰ.有机物K是一种酯,分子中除苯环外还含有1个五元环;
ⅱ.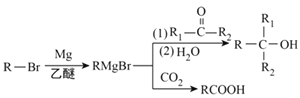 。
。
回答下列问题:
(1)有机物B的名称为____________,D的含氧官能团的名称是________________。
(2)C→D、F→G的反应类型分别为_________________、_________________。
(3)J的结构简式为______________,K的分子式为___________________。
(4)E与银铵溶液反应的化学方程式为____________________________。
(5)已知B在一定条件下可以水解生成X,与X互为同分异构体且含有苯环的有机物有_____种(不含X自身),写出其中核磁共振氢谱有4组吸收峰,且峰值比为3:2:2:1的结构简式__________________(任写一种)。
(6)利用题中信息所学知识,写出以甲烷和化合物A为原料,合成苯乙烯的路线流程图(其他试剂自选)__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)是一种重要的化工试剂,实验室合成硫酰氯的实验装置如下图所示:

已知:① SO2(g) + Cl2(g)![]() SO2Cl2(l) △H = -97.3 kJ/mol;
SO2Cl2(l) △H = -97.3 kJ/mol;
② 硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置甲为储气装置,用于提供氯气,则仪器A中盛放的试剂为______________。装置丙中活性炭的作用是______________。
(2)在上图方框内画出所缺装置,并注明相关试剂的名称。
(3)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为_____________,分离产物的方法是(填字母)_________。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有________(填序号)。
① 先通冷凝水,再通气 ② 控制气流速率,宜慢不宜快
③ 若三颈烧瓶发烫,可适当降温 ④ 加热三颈烧瓶
(5)在无活性炭存在的条件下SO2与Cl2也可发生反应,现将SO2、Cl2按照一定比例通入水中,请设计 一个简单实验验证二者是否恰好完全反应: (简要描述实验步骤、现象和结论)。
仪器自选,供选择试剂:滴加酚酞的氢氧化钠溶液、碘化钾溶液、淀粉溶液、品红溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A. 图1表示相同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
B. 图2中仅升高温度,纯水就可以从a点变到c点
C. 图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
D. 图3 表示H2与O2反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语使用正确的是( )
①甲基的电子式;![]() ②Cl的结构示意图:
②Cl的结构示意图: ;③乙烯的分子式:CH2=CH2 ④中子数为20的氯原子:
;③乙烯的分子式:CH2=CH2 ④中子数为20的氯原子:![]() Cl;⑤乙酸分子的比例模型:
Cl;⑤乙酸分子的比例模型: ;⑥氯乙烷的结构式:
;⑥氯乙烷的结构式:![]()
A. ④ B. ③④⑤ C. ④⑤⑥ D. ①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ:蒸馏是实验室制备蒸馏水的常用方法,如图所示两个装置都可以制取蒸馏水。

(1)图Ⅰ是实验室制取蒸馏水的常用装置,仪器A、B的名称分别是:A___________、B___________;
(2)温度计水银球应置于_______________________________________;
(3)实验时A 中除加入一定量的自来水外,还需加入少量_____________,其作用是 __________________________;
(4)图Ⅱ装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图I完全相同,该装置中使用的玻璃导管较长,其作用是__________________。
Ⅱ:现用质量分数为98℅、密度为1.84g/mL的浓硫酸来配制480mL 0.2mol/L 的稀硫酸。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙。完成下列问题:
(5)上述仪器中,在配制稀硫酸时不需要用到的是_____________(填序号);
(6)配制过程中需选用的容量瓶规格为_____________mL,经过计算,需要浓硫酸的体积为_______________;
(7)在配制过程中,能使所配溶液浓度偏高的是____________(填序号)
①洗涤量取浓硫酸后的量筒,并将洗涤液转移至容量瓶中
②为防止变质,稀释后的硫酸溶液应立即就转移到容量瓶中
③将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓硫酸
④移液前,容量瓶中含有少量蒸馏水
⑤量取浓硫酸时,俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,二氧化硫和氧气发生反应:2SO2(g)+O2(g) ![]() 2SO3(g)。
2SO3(g)。
(1)降低温度,化学反应速率________(填“增大”、“减小”、或“不变”)。
(2)600 ℃时,在一容积为2 L的密闭容器中,将二氧化硫和氧气混合,在反应进行至10 min和20 min时,分别改变了影响反应的一个条件,反应过程中SO2、O2、SO3物质的量变化如图所示,前10 min正反应速率逐渐____(填“增大”、“减小”或“不变”);前15 min内用SO3表示平均反应速率为________。

(3)图中反应进程,表示正反应速率与逆反应速率相等(即达到平衡状态)的时间段是_____________。
(4)根据如图判断,10 min时改变的条件可能是_______________________________(选填下面编号,下同);20 min时改变的反应条件可能是________。
a.加入催化剂 b.缩小容器容积
c.降低温度 d.增加O2的物质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种锂铜可充电电池,工作原理如下图。在该电池中,非水系电解液和水系电解液被锂离子固体电解质陶瓷片(Li+交换膜)隔开。下列说法不正确的是

A. 陶瓷片允许Li+通过,不允许水分子通过
B. 放电时,N极为电池的正极
C. 充电时,阳极反应为:Cu-2e-== Cu2+
D. 充电时,接线柱A应与外接电源的正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(CN)2的氧化性比Br2弱而比I2强,NaCN的水溶液呈碱性,则下列有关变化一般不能发生的是
A. CH2=CH2+(CN)2→NC-CH2-CH2-CN
B. (CN)2+2Br-→2CN-+Br2
C. (CN)2+2OH-→CN-+CNO-+H2O
D. HCN![]() H++CN-
H++CN-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com