
����Ŀ��������������ȡƯ��������ˮ������
��1��������ͨ��ˮ���Ƶ���ˮ����ˮ������Ư�ף�������Ư�����õ������� __________(��д
��ѧʽ����
��2����84������ҺҲ������Ư�ף��乤ҵ�Ʒ��ǿ����ڳ��������£�������ͨ��NaOH��
Һ�У���Ӧ�����ӷ���ʽΪ__________��
��3��ͬѧ��̽����84������Һ�ڲ�ͬpH��ʹ��ֽ��ɫ���������������ʵ�飺
����1����5mL������84������Һϡ��100�������ϡ�ͺ���Һ��pH=12;
����2��ȡϡ�ͺ���Һ��20 mL�ֱ����3���ྻ��С�ձ��У�
����3�������Ὣ3���ձ�����Һ��pH�ֱ����10��7��4������Һ����仯���Բ��ƣ�
����4����3���ձ��зֱ�����С��ͬ�ĺ�ֽ���۲�����¼���£�
�ձ� | ��Һ��pH | ���� |
a | 10 | 10 min��ֽ��������ɫ��4h���ֽ��ɫ |
b | 7 | 10 min��ֽ��ɫ��dz��4 h���ֽ��ɫ |
c | 4 | 10 min��ֽ��ɫ��ø�dz��4h���ֽ��ɫ |
��֪����Һ��Cl2��HC1O��ClO-���ʵ������������� ��pH�仯�Ĺ�ϵ����ͼ��ʾ��
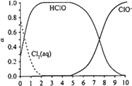
����ʵ������ɻ�����½��ۣ���Һ��pH��4 ~10��Χ�ڣ�pHԽ��ֽ��ɫ________��
�ڽ��ͼ����з�����b��c���ձ���ʵ��������ֲ����ԭ����________��
��4������������������ˮ�е��л������Ӧ�����ɶ������к������ʣ����dz����о���ʹ���µ�����ˮ����������ClO2�������һ������Ч������������
��һ���Ʊ�ClO2�ķ����ǽ�SO2ͨ�������ữ��NaC1O3��Һ�У���Ӧ�����ӷ���ʽΪ__________��
����һ���Ʊ�ClO2�ķ�������NaClO3�����ᷴӦ��ͬʱ��Cl2���ɣ�������Cl2���Լռ1/3����ÿ����0.5 mol ClO2��ת��__________mole-��
���𰸡� HClO Cl2+2OH-=Cl-+ClO-+H2O Խ�� b�ձ�����Һ��pH����c�ձ�����Һ��pH��HClOŨ�Ƚ�С����Ӧ���ʽ�������ɫ���� SO2+2ClO3-=2ClO2+SO42- 0.5
��������(1)������ˮ��Ӧ��������ʹ����ᣬ���������ǿ�����ԣ��ܹ�����ɫ����Ư�ף��ʴ�Ϊ��HClO��
(2)������������ͨ��NaOH��Һ�з�Ӧ�����Ȼ��ơ��������ƺ�ˮ����Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O���ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
(3)�ٸ���ʵ�����ݣ���Һ��pH��4 ~10��Χ�ڣ�pHԽ��ֽ��ɫԽ�����ʴ�Ϊ��Խ����
�ڸ�����Һ��Cl2��HC1O��ClO-���ʵ�������(��) ��pH�仯�Ĺ�ϵͼ��֪��b�ձ�����Һ��pH����c�ձ�����Һ��pH��HClOŨ�Ƚ�С����Ӧ���ʽ�������ɫ�������ʴ�Ϊ��b�ձ�����Һ��pH����c�ձ�����Һ��pH��HClOŨ�Ƚ�С����Ӧ���ʽ�������ɫ������
(4)�ٽ�SO2ͨ�������ữ��NaC1O3��Һ�з�Ӧ������ClO2������������ԭ��Ӧ�Ĺ��ɣ�ͬʱӦ�����������ƣ���Ӧ�����ӷ���ʽΪSO2+2ClO3-=2ClO2+SO42-���ʴ�Ϊ��SO2+2ClO3-=2ClO2+SO42-��
����NaClO3�����ᷴӦ����ClO2��ͬʱ��Cl2���ɣ�������Cl2���Լռ1/3����Ӧ�Ļ�ѧ����ʽΪ2NaClO3+4HCl= 2ClO2��+ Cl2��+ 2H2O+2NaCl����Ӧ��ת�Ƶĵ���Ϊ2e-����ÿ����0.5 mol ClO2��ת�Ƶĵ����ʵ���Ϊ0.5mol���ʴ�Ϊ��0.5��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܹ������������д�����Ԫ�ص�ʵ�������( )
A. ����������ֱ�Ӽ���AgNO3��Һ
B. ������ˮ����ֽ������AgNO3��Һ
C. ����NaOH��Һ�����Ⱥ����ϡ�����ữ��Ȼ�����AgNO3��Һ
D. ����NaOH���Ҵ���Һ�����Ⱥ����AgNO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�������������ԭ��Ӧ�����������ȷ�Ӧ����
A��пƬ��ϡ����ķ�Ӧ B�����ȵ�̼��ˮ�����ķ�Ӧ
C�������ڿ����е�ȼ�շ�Ӧ D��Ba(OH)2��8H2O��NH4Cl�ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵʩ�Լ�����Դ�˷Ѻͽ��ͷ����ŷ�Ϊ�������ݵĽ��ܼ������ߣ���Ӧ��ȫ���������⡢������Դ��Լ�͡������Ѻ������ı�Ȼѡ������ҵ�ķ�չ������Ϲ��ҽ��ܼ��ŵ�����Ҫ����������ѧ֪ʶ������������⣺
��1����֪ij��Ӧ��ƽ�����ʽΪ��
 ������Ӧ�Ļ�ѧ��ӦΪ��__________
������Ӧ�Ļ�ѧ��ӦΪ��__________
��2����֪��400��ʱ��N2(g)+3H2(g) ![]() 2NH3(g) ��H<0��K=0.5����400��ʱ����0.5L�ķ�Ӧ�����н��кϳɰ���Ӧ��һ��ʱ����N2��H2��NH3�����ʵ����ֱ�Ϊ2mol��1mol��2mol�����ʱ��Ӧv(N2)��_____v(N2)��(��:��������=������ȷ��);��ʹ�ø÷�Ӧ�Ļ�ѧ��Ӧ���ʼӿ죬ͬʱʹƽ��ʱNH3������������ӣ�
2NH3(g) ��H<0��K=0.5����400��ʱ����0.5L�ķ�Ӧ�����н��кϳɰ���Ӧ��һ��ʱ����N2��H2��NH3�����ʵ����ֱ�Ϊ2mol��1mol��2mol�����ʱ��Ӧv(N2)��_____v(N2)��(��:��������=������ȷ��);��ʹ�ø÷�Ӧ�Ļ�ѧ��Ӧ���ʼӿ죬ͬʱʹƽ��ʱNH3������������ӣ�
�ɲ�ȡ����ȷ��ʩ��____________(�����)
A. ��С�������ѹǿ B.�����¶� C.�Ӵ��� D.ʹ����Һ������
��3����һ��������ܱ������У��������»�ѧ��Ӧ��
A(g)+3B(g) ![]() 2C(g)+D(s) ��H���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
2C(g)+D(s) ��H���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t/K | 300 | 400 | 500 | ���� |
K/(mol��L-1)2 | 4��106 | 8��107 | K1 | ���� |
�������������:
���жϸ÷�Ӧ�Ħ�H _______0(���������)
����һ�������£����жϸ÷�Ӧһ���ﻯѧƽ��״̬����________ (�����)��
A. 3v(B)(��)=2v(C)(��) B.������ѹǿ���ֲ���
C.A��B��ת������� D.���������ܶȱ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѭ�����ղ���������SO2���ͻ�����Ⱦ��ͬʱ�����Ƶ������������������£�

����˵����ȷ����
A. �������е����ʷ������Ϊ����
B. Ĥ��Ӧ���У�����ѹǿ���������HI�ķֽ����ʺ�ƽ��ת����
C. �ù�����I2��HI���ת������������ѭ����
D. ��ѭ�����յ��ܷ�ӦΪ2SO2+4H2O+I2 == H2+2H2SO4+ 2HI
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����������Ļ���Ӫ�����ʵ�˵������ȷ����
A. �������ڣ���֬����Ҫ��Ӧ����֬��ø����ˮ��Ϊ��֬�������
B. ��øϴ�·��е�ø��ʵ�ǵ�����
C. ���ࡢ��֬�������ʶ�����һ�������·���ˮ�ⷴӦ
D. �����C��H��O����Ԫ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����Һ��ͨ��������������,ʹ��Һ����������ǿ���� ( )
A. ������ͨ������NH3 B. ������ͨ������NH3
C. ��ˮ�м�������H2O D. �����м�������AgNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������X��һ�ֻ�ͪ�������м��壬��ṹ��ʽ��ͼ��ʾ�������йػ�����X��˵����ȷ����

A. ���л������ʽΪC24H22O5
B. �ܷ���ȡ����Ӧ���ӳɷ�Ӧ��������Ӧ
C. 1mol������X�������2mol NaOH��Ӧ
D. 1mol������X������11mol H2�����ӳɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�ij�ݻ�Ϊ2L���ܱ������ڣ�ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯��������ͼ��ʾ������˵����ȷ���ǣ� �� 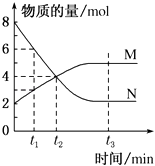
A.��Ӧ��ʼ��t2ʱ����Ӧ�ﵽƽ��״̬
B.��Ӧ��ʼ��t1��t1=1s����N�����ʵ���Ũ�ȱ仯��2mol/L
C.��Ӧ��ʼ��t2��t2=2s������M��ʾ��Ӧ����Ϊ0.5mol/��L��s��
D.��Ӧ�Ļ�ѧ����ʽΪ��N��g��2M��g��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com