
| A、2mol水的摩尔质量是36g?mol-1 | ||
B、一个钠原子的实际质量约等于
| ||
| C、1.5mol O2的体积约为33.6L | ||
| D、将 100mL水加入到 100mL 1mol/L的NaOH溶液中,所得溶液为0.5mol/L |
| 23 |
| 6.02×1023 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 元素 | 信息 |
| A | 阳离子核外无电子 |
| B | 形成的化合物种类最多 |
| C | |
| D | 原子的L层有2个未成对电子 |
| E | 焰色反应呈黄色 |
| F | 与D 同主族 |
| G | 二价阳离子与氩原子具有相同的电子层结构 |
| H | H3+的M层3d轨道电子为半充满状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+ Na+NO3- Cl- |
| B、K+ Na+Cl- NO3- |
| C、K+ Na+ Cl-AlO2- |
| D、K+ NH4+ SO42-NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在蒸馏的实验中,温度计的水银球位于支管口处是为了测出馏分的沸点 |
| B、可用四氯化碳萃取溴水中的溴 |
| C、在重结晶的实验中,使用短颈漏斗趁热过滤是为了减少被提纯物质的损失 |
| D、作为重结晶实验的溶剂,杂质在此溶剂中的溶解度受温度影响应该很大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| pH | Ca2+、Mg2+总浓度 | 细菌总数 |
| 6.5~8.5 | <0.0045mol?L-1? | <100个?mL-1? |
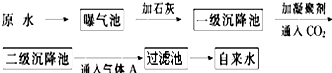
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用完后的废电池应该集中回收处理 |
| B、天然果汁中不含任何化学物质 |
| C、“绿色食品”指颜色为绿色的食品 |
| D、“白色污染”是白色粉尘造成的污染 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com