
【题目】某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。

(1)由图中的数据分析,该反应的化学方程式为____________________________________________
(2)反应开始至2min、5minZ的平均反应速率为__________________、_______________;
(3)5min后Z的生成速率比5min末Z的 生成速率___________(大、小、相等)。
【答案】3X+Y![]() 2Z 0.05 mol·(L·min)-1 0.04 mol·(L·min)-1 相等
2Z 0.05 mol·(L·min)-1 0.04 mol·(L·min)-1 相等
【解析】
(1)根据图像可知,反应进行到5min时反应达到平衡状态,此时X和Y的物质的量分别减少了0.6mol和0.2mol,而Z的物质的量增加了0.4mol。当反应达到5min时,各种物质的浓度都不发生变化,因此该反应是可逆反应。根据变化量之比是相应的化学计量数之比可知,反应的方程式是3X+Y![]() 2Z。
2Z。
(2)根据图像可知,反应开始至2min、5minZ的增加量分别是0.2mol、0.4mol,
所以反应开始至2min时V(Z)=(0.2mol÷2L)÷2min=0.05mol·L-1·min-1;
反应开始至5min时V(Z![]() )=(0.4mol÷2L)÷5min=0.04mol·L-1·min-1;
)=(0.4mol÷2L)÷5min=0.04mol·L-1·min-1;
(3)根据图像可知,反应进行到5min时反应达到平衡状态,所以5min后反应处于平衡状态,此时Z的生成速率比5min末Z的生成速率相等。


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案科目:高中化学 来源: 题型:
【题目】某同学称取一定质量的MgCl2固体配成溶液,在该溶液中加入一定量的盐酸,然后向此混合溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示。

请回答下列问题。
(1)溶解MgCl2固体所用的玻璃仪器有________ (填字母)。
a. 天平 b. 烧杯 c. 漏斗 d. 玻璃棒
(2)OA段反应的离子方程式为_____________________________________。
(3)AB段反应的离子方程式为________________________________________。
(4)在B点对应的溶液中滴加AgNO3溶液,观察到的现象是______________________,反应的离子方程式为___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是硫酸试剂瓶标签上的内容:

(1)某化学兴趣小组进行硫酸性质的实验探究时,需要490mL 4.6mol·L-1的稀硫酸,现要配制该浓度的溶液所需的玻璃仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要__________(填仪器名称);需要量取98%浓硫酸____________mL进行配制;
(2)配制溶液时有如下操作:a.稀释溶解b.摇匀c.洗涤d.冷却e.量取f.将溶液移至容量瓶g.定容,实验操作顺序正确的是(___________)。
A. e→a→f→d→c→f→g→b B. e→a→d→f→c→f→g→b
C. e→a→f→d→c→f→b→g D. e→a→d→f→c→f→b→g
(3)下列为配制过程中部分操作的示意图,其中有错误的是____(填序号);

(4)在配制4.6mol·L-1稀硫酸的过程中,下列情况会引起配制所得的硫酸溶液物质的量浓度偏高的是___;
A.未经冷却趁热将溶液注入容量瓶中 B.容量瓶洗涤后,未干燥处理
C.定容时仰视观察液面 D.未洗涤烧杯和玻璃棒
(5)为中和100mL 2.3 mol·L-1KOH溶液后显中性,需要加入________mL 4.6mol·L-1稀硫酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于硫酸和硝酸的叙述中,下列叙述不正确的是
A.浓硫酸和浓硝酸都具有很强的腐蚀性、脱水性
B.冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装
C.王水是浓盐酸和浓硝酸按 3:1 混合,具有很强的腐蚀性,可以腐蚀金和铂
D.硫酸和硝酸都是重要的化工原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F、G七种短周期元素,原子序数依次增大。已知A与E、D与F分别同主族, E、F、G同周期;A、C的最外层电子数之和与D的最外层电子数相等,A与D形成的化合物常温下为液态,A分别与F、G形成的气体分子电子总数相等、B有多种同素异形体,其中一种是原子晶体,是自然界中最硬的物质,可做首饰品或做切削工具。
请回答下列问题:
(1)元素C在周期表中的位置是_______________
元素E的原子结构示意图为________________
(2)C的气态氢化物的水化物与其最高价氧化物的水化物可发生反应,离子方程式为:
______________________________________________________________________________
(3)在一定条件下,A、D的单质和A、D、E形成的离子化合物的水溶液可构成电池,该电池负极的电极反应式为___________________________________________________, 该电池在放电过程中,电解质溶液的pH将________(填“增大”、“减小”或“不变”)。
(4)化合物C2A4(g) 是一种高效清洁的火箭燃料,0.25 mol C2A4完全燃烧的生成物是一种气态单质和一种气态化合物,它们对环境无污染,同时放出热量133.5 kJ的热量。则该反应的热化学方程式为(用具体物质化学式表示)____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B.草酸二乙酯可用于苯巴比妥等药物的中间体,实验室以草酸(HOOC—COOH)和乙醇为原料制备草酸二乙酯的实验步骤如下:

步骤1:在上图所示装置中,加入无水草酸45g,无水乙醇81g,苯200mL,浓硫酸10mL,搅拌下加热6870℃回流共沸脱水。
步骤2:待水基本蒸完后,分离出乙醇和苯。
步骤3:所得混合液冷却后依次用水、饱和碳酸氢钠溶液洗涤,再用无水硫酸钠干燥。
步骤4:常压蒸馏,收集182-184℃的馏分,得草酸二乙酯57g。
(1)步骤1中发生反应的化学方程式是 ,反应过程中冷凝水应从 (填“a”或“b”)端进入。
(2)步骤2操作为 。
(3)步骤3用饱和碳酸氢钠溶液洗涤的目的是 。
(4)步骤4除抽气减压装置外所用玻璃仪器有蒸馏烧瓶、冷凝管、接液管、锥形瓶和 。
(5)本实验中,草酸二乙酯的产率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.钠和钾的合金可用于快中子反应堆作热交换剂
B.实验室常将钠保存在煤油或四氯化碳中
C.小苏打是培制糕点所用的发酵粉的主要成分之一
D.热的纯碱溶液可以去除物品表面的油污
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种短周期元素,原子序数D>C>B>A,且B、C、D同周期,A、D同主族,B原子的最外层只有一个电子,C的原子结构示意图如图,D在同周期元素中原子半径最小,据此填空:
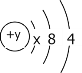
(1)C元素的名称为____,其气态氢化物的化学式为___。
(2)D在周期表的___周期,___族。
(3)A、B、C、D四种元素的原子半径由大到小的顺序为(用化学式填写)___
(4)B的最高价氧化物的水化物的化学式为__
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向蔗糖中加入浓硫酸,搅拌得黑色海绵状固体,并放出刺激性气味气体 | 浓硫酸仅体现吸水性和脱水性 |
B | 向蓝色石蕊试纸上滴加新制氯水,试纸边缘呈红色,中间为白色 | 氯水既有酸性又有还原性 |
C | 卤代烃Y与NaOH溶液共热后,加入足量稀硝酸,再滴加AgNO3溶液,产生白色沉淀 | 卤代烃Y中含有氯原子 |
D | 取5 mL 0.1 mol·L-1KI溶液,加入1 mL 0.1 mol·L-1FeCl3溶液,萃取分液后,向水层滴入KSCN溶液,溶液变成血红色 | Fe3+与I-所发生的反应为可逆反应 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com