
【题目】磷能形成多种含氧酸。
(1)次磷酸(H3PO2)是一种精细化工产品,向10 mL H3PO2溶液中加入10 mL等物质的量浓度的NaOH溶液后,所得的溶液中只有H2PO2-、OH-两种阴离子。
① 写出H3PO2溶液与足量NaOH 溶液反应后形成的正盐的化学式:_______,该正盐溶液中各离子浓度由大到小的顺序为____________。
② 若25℃时,K (H3PO2) = 1×10-2,则0.01 mol · L-1的H3PO2溶液的pH =________。
(2)亚磷酸(H3PO3)是二元中强酸,25℃时亚磷酸的电离常数为K1= 1×10-2、K2=2.6×10-7。
① 试从电离平衡移动的角度解释K1、K2数据的差异_______________。
② NaH2PO3溶液显______性(填“酸”“碱”或“中”)。
(3) 25 ℃时,HF的电离常数为K = 3.6×10-4; H3PO4的电离常数为K1=7.5×10-3,K2=6.2×10-8,K3=4.4×10-13。足量NaF溶液和H3PO4溶液反应的离子方程式为_________。
(4)相同温度下,等物质的量浓度的上述三种磷的含氧酸中。c(H+)由大到小的顺序为_____(用酸的分子式表示)。
【答案】 NaH2PO2 c(Na+)>c(H2PO2-)>c(OH-)>c(H+) 2 H3PO3第一步电离出的H+对第二步电离起到抑制作用 酸 F- +H3PO4 =HF+H2PO4- H3PO3 >H3PO2 >H3PO4
【解析】试题分析:10 mL H3PO2溶液中加入10 mL等物质的量浓度的NaOH溶液后生成NaH2PO2,所得的溶液中只有H2PO2-、OH-两种阴离子,说明H2PO2-不能电离,H3PO2是一元酸;②根据![]() 计算0.01 mol · L-1的H3PO2溶液的pH;(2)①H3PO3第一步电离出的H+对第二步电离起到抑制作用;② H2PO3-电离平衡常数是K=2.6×10-7,H2PO3-水解平衡常数是
计算0.01 mol · L-1的H3PO2溶液的pH;(2)①H3PO3第一步电离出的H+对第二步电离起到抑制作用;② H2PO3-电离平衡常数是K=2.6×10-7,H2PO3-水解平衡常数是![]() ;(3)HF的电离常数为K = 3.6×10-4小于H3PO4的电离常数为K1=7.5×10-3,大于H3PO4的第二步电离常数K2=6.2×10-8,所以足量NaF溶液和H3PO4溶液反应生成HF和NaH2PO4;(4)H3PO4的第一步电离常数为K1=7.5×10-3;亚磷酸是二元酸,第一步电离常数为K1= 1×10-2;次磷酸是一元酸,电离平衡常数是K (H3PO2) = 1×10-2,所以酸性亚磷酸>次磷酸>磷酸;
;(3)HF的电离常数为K = 3.6×10-4小于H3PO4的电离常数为K1=7.5×10-3,大于H3PO4的第二步电离常数K2=6.2×10-8,所以足量NaF溶液和H3PO4溶液反应生成HF和NaH2PO4;(4)H3PO4的第一步电离常数为K1=7.5×10-3;亚磷酸是二元酸,第一步电离常数为K1= 1×10-2;次磷酸是一元酸,电离平衡常数是K (H3PO2) = 1×10-2,所以酸性亚磷酸>次磷酸>磷酸;
解析:①H3PO2是一元酸,H3PO2溶液与足量NaOH 溶液反应后形成的正盐的化学式:NaH2PO2,NaH2PO2是强碱弱酸盐,溶液中各离子浓度由大到小的顺序为c(Na+)>c(H2PO2-)>c(OH-)>c(H+);②![]() ,c(H+)=1×10-2 ,所以0.01 mol · L-1的H3PO2溶液的pH =2;(2)①H3PO3第一步电离出的H+对第二步电离起到抑制作用,所以K1>K2;② H2PO3-电离平衡常数是K=2.6×10-7,H2PO3-水解平衡常数是
,c(H+)=1×10-2 ,所以0.01 mol · L-1的H3PO2溶液的pH =2;(2)①H3PO3第一步电离出的H+对第二步电离起到抑制作用,所以K1>K2;② H2PO3-电离平衡常数是K=2.6×10-7,H2PO3-水解平衡常数是![]() ,电离大于水解,所以溶液出酸性;(3)HF的电离常数为K = 3.6×10-4小于H3PO4的第一步电离常数为K1=7.5×10-3,大于H3PO4的第二步电离常数K2=6.2×10-8,所以足量NaF溶液和H3PO4溶液反应生成HF和NaH2PO4,离子方程式是F- +H3PO4 =HF+H2PO4- ;(4)H3PO4的第一步电离常数为K1=7.5×10-3;亚磷酸是二元酸,第一步电离常数为K1= 1×10-2;次磷酸的电离平衡常数是K (H3PO2) = 1×10-2,所以酸性亚磷酸>次磷酸>磷酸;所以相同温度下,等物质的量浓度的三种磷的含氧酸中,c(H+)由大到小的顺序为H3PO3 >H3PO2 >H3PO4。
,电离大于水解,所以溶液出酸性;(3)HF的电离常数为K = 3.6×10-4小于H3PO4的第一步电离常数为K1=7.5×10-3,大于H3PO4的第二步电离常数K2=6.2×10-8,所以足量NaF溶液和H3PO4溶液反应生成HF和NaH2PO4,离子方程式是F- +H3PO4 =HF+H2PO4- ;(4)H3PO4的第一步电离常数为K1=7.5×10-3;亚磷酸是二元酸,第一步电离常数为K1= 1×10-2;次磷酸的电离平衡常数是K (H3PO2) = 1×10-2,所以酸性亚磷酸>次磷酸>磷酸;所以相同温度下,等物质的量浓度的三种磷的含氧酸中,c(H+)由大到小的顺序为H3PO3 >H3PO2 >H3PO4。


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】计算题(写出计算过程)
在标准状态下,有体积为4.48L的氯化氢,溶于水得到1L溶液(为盐酸)。请计算:
(1)该盐酸中HCl的物质的量是多少?
_________________
(2)Cl-物质的量是多少?溶液H+物质的量浓度是多少?
_________________
(3)若该盐酸密度为ρ g/cm3,则溶质的质量分数为多少?(用含ρ式子表示)
_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质分类正确的是( )
酸 | 碱 | 盐 | 氧化物 | |
A | 硫酸 | 纯碱 | 硫酸钙 | 氧化铁 |
B | 盐酸 | 烧碱 | 纯碱 | 氧化钙 |
C | 碳酸 | 硫酸钙 | 碳酸钠 | 干冰 |
D | 干冰 | 苛性钠 | 食盐 | 石灰石 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关蛋白质溶液实验过程属于物理变化是 ( )
A. 向蛋白质溶液中逐滴加入饱和硫酸铜溶液
B. 将蛋白质溶液加热蒸干
C. 将蛋白质溶液和95%的乙醇溶液混合
D. 用聚光手电筒照射蛋白质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组拟制备氯气并验证其一系列性质,实验装置如图所示(省略夹持装置)。已知:硫代硫酸钠(Na2S2O3)溶液在工业上可作为脱氯剂
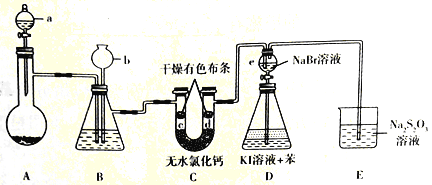
回答下列问题:
(1)仪器a的名称是______,其中盛有浓盐酸,烧瓶A 中盛有的固体试剂是_____(填化学式)。
(2)装置B中盛有饱和NaCl溶液,装置B的作用是________。
a.除去C12中的杂质HCl b.干燥
c.提供后续水蒸气 d.观察装置是否堵塞
(3)c处有色布条褪色,而d处不褪色,这说明__________。
(4)实验结束后,打开e 的活塞,使其中的溶液流人到锥形瓶D中,摇匀锥形瓶,静置后可观察到______________________。
(5)装置E中发生反应的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,己知Co、Fe均为中等活泼金属)的工艺流程如图所示:

问答下列问题:
(l)(NH4)2C2O4中C元素的化合价为________。
(2)合金废料加入盐酸浸取,该盐酸不能换为硝酸,原因是____________。
残渣M的主要成分是一种金属单质,该金属为_______________,
(3)“浸出液”中先后加入的两种试剂涉及氨水、H2O2溶液,应先加入____________,加入氨水发生反应的离+方程式为____________________。
(4)溶液A中的金属阳离子是_________,加入(NH4)2C2O4溶液的目的是__________ 。
(5)“操作1”的名称是_________,草酸钴高温焙烧生成Co2O3,实验室中高温焙烧使用的仪器是_____(填字)。
a.蒸发皿 b.表面皿 c.烧杯 d.坩埚
(6)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表。“操作2”中,蒸发浓缩后必须趁热过滤,其目的是_________________,90℃时Ksp(Li2CO3)的值为___________。
温度/℃ | 10 | 30 | 60 | 90 |
浓度/mol·L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖和淀粉的混合物中氢的质量分数为6.5%,则混合物中氧的质量分数为 ( )
A. 13.0% B. 39.0% C. 45.5% D. 52.0%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某学校实验室买回的硫酸试剂标签的部分内容。判断下列说法正确的是( )

A. 该硫酸的浓度为9.2 mol·L-1
B. 配制480 mL 4.6 mol·L-1的稀硫酸需该H2SO4125mL
C. 该硫酸与等体积水混合质量分数变为49%
D. 取该硫酸100 mL,则浓度变为原来的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对工业废气物进行脱硫(SO2)处理并加以利用,不仅可防止大气污染,还能实现一定经济效益。回答下列问题:
(1)热化学碘硫循环脱硫,涉及以下三个反应:
bunsen反应:SO2(g)+I2(g)+2H2O(l)═2HI (g)+H2SO4(l) △H
硫酸分解反应:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(l) △H=+462kJ·mol-1
碘化氢分解反应:2HI(g)=H2(g)+I2(g)△H=+10kJ·mol-1
已知氢气的燃烧热为286kJ·mol-1,则bunsen反应的△H=_________kJ·mol-1。
(2)在活性炭催化下,SO2与Cl2发生反应:SO2(g)+Cl2(g)![]() SO2Cl2(g)△H<0。在定温定压条件下,容器体积为10L的容器中加入等物质的量的SO2和Cl2,充分混合(二者物质的量均为nmol)后,达到平衡后容器体积为8L。
SO2Cl2(g)△H<0。在定温定压条件下,容器体积为10L的容器中加入等物质的量的SO2和Cl2,充分混合(二者物质的量均为nmol)后,达到平衡后容器体积为8L。
①SO2Cl2能与水发生非氧化还原反应,生成两种酸,则这两种酸的化学式为_________。
②下列事实中,不能作为判断硫元素和氯元素非金属性强弱的依据是_________(填字母)。
A.硫化氢的分解温度为300℃左右,氯化氢1500℃才分解
B.氢硫酸(H2S的水溶液)是一种弱酸,盐酸是强酸
C.将氯气通入氢硫酸中,溶液中产生黄色浑浊
D.高氯酸在无机含氧酸中酸性最强
③该温度下,SO2的平衡转化率α1=_________,反应的平衡常数K=_________(列式并计算)。
④下列措施中不能进一步提高氯气的平衡转化率的是_________。
A.平衡后将容器的体积压缩为4L B.增大二氧化硫的浓度
C.升高温度 D.将SO2Cl2(g)液化分离
⑤若向该容器中初始投入SO2和Cl2的物质的量均为0.5nmol,则达到平衡时SO2的平衡转化率:α2_________填“>”“<”或“=”)α1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com