
����Ŀ��ij��ȤС�����Ʊ���������֤��һϵ�����ʣ�ʵ��װ����ͼ��ʾ��ʡ�Լг�װ�ã�����֪����������ƣ�Na2S2O3����Һ�ڹ�ҵ�Ͽ���Ϊ���ȼ�
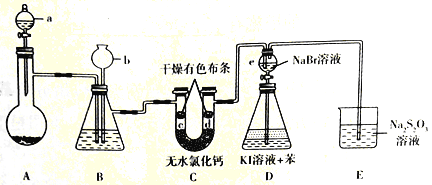
�ش��������⣺
��1������a��������______������ʢ��Ũ���ᣬ��ƿA ��ʢ�еĹ����Լ���_____���ѧʽ����
��2��װ��B��ʢ�б���NaCl��Һ��װ��B��������________��
a����ȥC12�е�����HCl b������
c���ṩ����ˮ���� d���۲�װ���Ƿ����
��3��c����ɫ������ɫ����d������ɫ����˵��__________��
��4��ʵ�������e �Ļ�����ʹ���е���Һ���˵���ƿD�У�ҡ����ƿ�����ú�ɹ۲쵽______________________��
��5��װ��E�з�����Ӧ�����ӷ���ʽΪ____________��
���𰸡� ��Һ©�� KMnO4������KClO3���Ⱥ����Լ�Ҳ�ɣ� acd Cl2��Ư�����ã�HC1O��Ư������ �ϲ���ҺΪ�Ϻ�ɫ S2O32- +4C12+5H2O=2SO42- +8C1- +10H+
�������������������1����������a�������Լ��������������Ʒ������װ��A���������ȡ��������ѡ���ڳ����������Ȼ��������������2�����ɵ������л���HCl��װ��B�������г�ȥ�����е��Ȼ��⣬�ṩ����ˮ������������ȫƿ����3����ʪ����������Ư���ԣ�������������߱�Ư���ԣ�������Ư�����õ��Ǵ������4��������ȡ��ˮ�е��嵥�ʣ������ܶȱ�ˮС����5��Na2S2O3������+2�ۣ�����������SO42-�����ݵ�ʧ�����غ��ԭ���غ���д���ӷ���ʽ��
��������1������a�Ǵ��в���������©����Ϊ��Һ©��������ʢ��Ũ���ᣬ��ƿA ���ڳ����������Ȼ�����ȡ��������ѡ��KMnO4����KClO3���ȣ�����2�����������ڱ���ʳ��ˮ����HCl��������ˮ�����ñ���ʳ��ˮ��ȥ�������������Ȼ������壬����ͨ��C�У��ɹ۲쵽c��������ɫ��d������ɫ��װ��B�ṩ����ˮ��������������ʱB�е�ѹǿ����B�г���©����Һ���������γ�ˮ�����ɹ۲�װ���Ƿ����������acd���ϣ���3����װ��c��ͨ��������d������ɫ��������ɫ����Ϊ������������߱�Ư���ԣ�c������ɫ������ɫ����˵������������ҺB�������ˮ����ʪ����������Ư���ԣ�������Ư�����õ���������ˮ��Ӧ���ɵĴ����ᣬ����c����ɫ������ɫ����d������ɫ����˵��Cl2��Ư�����ã�HC1O��Ư�����ã���4��ʵ�������e �Ļ�����ʹ���е���Һ���˵���ƿD�У���ˮ�м��뱽��ʳȺ췢����ȡ�������ܶȱ�ˮС���ϲ���ҺΪ�Ϻ�ɫ����5��Na2S2O3������+2�ۣ�����������SO42-����װ��E����Ӧ�����ӷ�Ӧ����ʽ��S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�õ��жϣ�������ȷ����( )

A����ߵ�װ���ǵ��أ��ұߵ�װ����ԭ���
B����װ����ͭΪ������пΪ����
C����ͭƬ�������仯Ϊ12.8 gʱ��a�������ĵ�O2�ڱ�״���µ����Ϊ2.24 L
D��װ���еĵ��������ǣ�a��Cu������CuSO4��Һ��Zn��b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W��QΪԭ���������������ǰ������Ԫ�أ�X����δ�ɶԵ�������2����������Ԫ�ؾ����γɶ�Ԫ�����Y�ǵؿ��к������Ľ���Ԫ�أ�Z���Ŵ����ʵ����Ԫ��֮һ��W�ڲ��������������������9����Q��̬ԭ�Ӽ۲�����Ų��гɶԵ�������δ�ɶԵ�������ͬ���ݴ˻ش��������⣺
��1��Q�Ļ�̬ԭ�ӵļ۲�����Ų�ʽΪ____________________��
��2���縺��������_________________����һ�����ܽ���Y��Z֮���ͬ����Ԫ����__________ (��Ԫ�ط��ţ���
��3��Y��W���Ȼ����۵�ߵ���_________(�ѧʽ)��ԭ����____________________________����Z�ĵͼ��Ȼ��ﻥΪ�ȵ������������_____________��
��4������������������˷����ã���ṹ��ʽ��ͼ�������£���������ˮ�е��ܽ��Ϊ2g��������ˮ��������C6H4��OH����COONa���ݿ�ʹ���ܽ��������ԭ�������_____________________�������е�ԭ�ӵ��ӻ�������_______________��
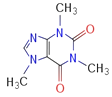
��5����֪WX���ܶ�Ϊ3.25g/cm3����Ԫ�����߳�481pm����
ȷ���õ�Ԫ�����к���______��WX������__________�����ṹ(��д���ġ�������)�������о���W�����X��________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������£������йص������Һ��������ȷ���� ( )
A. ��Na2CO3��Һ��ͨ��CO2����ҺΪ���ԣ���![]()
B. pH��ͬ�İ�ˮ��Ba(OH)2��Һ�У�2c(NH4+)= c( Ba2+)
C. ��Ũ�ȵ�KHSO3��Һ��KOH��Һ�������ϣ�c(OH-)-c(H+)=c(HSO3-)+c(H2SO3)
D. ��Mg(OH)2��Һ�м�������NH4Cl��ĩ![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������γɶ��ֺ����ᡣ
��1�������ᣨH3PO2����һ�־�ϸ������Ʒ����10 mL H3PO2��Һ�м���10 mL�����ʵ���Ũ�ȵ�NaOH��Һ�����õ���Һ��ֻ��H2PO2-��OH-���������ӡ�
�� д��H3PO2��Һ������NaOH ��Һ��Ӧ���γɵ����εĻ�ѧʽ��_______����������Һ�и�����Ũ���ɴ�С��˳��Ϊ____________��
�� ��25��ʱ��K (H3PO2) = 1��10-2����0.01 mol �� L-1��H3PO2��Һ��pH =________��
��2�������ᣨH3PO3���Ƕ�Ԫ��ǿ�ᣬ25��ʱ������ĵ��볣��ΪK1= 1��10-2��K2=2.6��10-7��
�� �Դӵ���ƽ���ƶ��ĽǶȽ���K1��K2���ݵIJ���_______________��
�� NaH2PO3��Һ��______�ԣ���������������������������
��3�� 25 ��ʱ��HF�ĵ��볣��ΪK = 3.6��10-4�� H3PO4�ĵ��볣��ΪK1=7.5��10-3��K2=6.2��10-8��K3��4.4��10-13������NaF��Һ��H3PO4��Һ��Ӧ�����ӷ���ʽΪ_________��
��4����ͬ�¶��£������ʵ���Ũ�ȵ����������ĺ������С�c(H+)�ɴ�С��˳��Ϊ_____������ķ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����㻯����A��һ�ֻ�������ԭ�ϣ����Դ�ú��ʯ���еõ���A��B��C��D��E��ת����ϵ������ʾ��
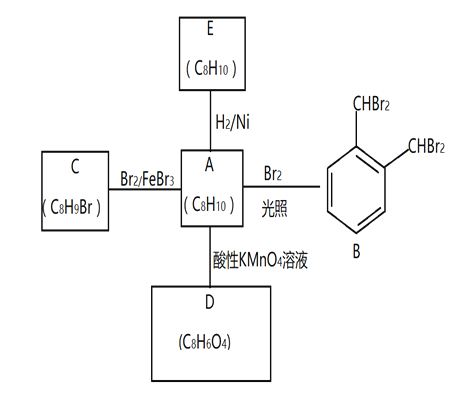
�ش��������⣺
��1��A�Ļ�ѧ������___________
��2��A��B �ķ�Ӧ������______________���ڸ÷�Ӧ�ĸ������У���B��Ϊͬ���칹��ĸ�����Ľṹ��ʽΪ______________________
��3��C�й���������_____________��A������KMnO4��Һ��Ӧ�ɵõ�D��д��D�й���������_______________________________
��4��A��E�Ļ�ѧ����ʽΪ____________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����Ƴ�����ĤH2Sȼ�ϵ�أ�ʵ��������H2S������Դ�����������õ�����������ĤH2Sȼ�ϵ�صĽṹʾ��ͼ����ͼ��ʾ������˵������ȷ����

A. �缫aΪ��صĸ���
B. �缫b�Ϸ����ĵ缫��ӦΪ��O2 +4H+ + 4e��=== 2H2O
C. ��·��ÿ����4 mol���ӣ�����������44.8 LH2S
D. ÿ17 g H2S���뷴Ӧ����1 mol H+������Ĥ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽ������ˮ�ⷴӦ������Һ�����Ե��� ( )
A. HCO3- + H2O ![]() H3O+ + CO32- B. Fe3+ + 3H2O
H3O+ + CO32- B. Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+
Fe(OH)3 + 3H+
C. HS- + H2O ![]() H2S + OH- D. NH4+ + OH-
H2S + OH- D. NH4+ + OH- ![]() NH3��+ H2O
NH3��+ H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com