
����Ŀ����ѧ����Ƴ�����ĤH2Sȼ�ϵ�أ�ʵ��������H2S������Դ�����������õ�����������ĤH2Sȼ�ϵ�صĽṹʾ��ͼ����ͼ��ʾ������˵������ȷ����

A. �缫aΪ��صĸ���
B. �缫b�Ϸ����ĵ缫��ӦΪ��O2 +4H+ + 4e��=== 2H2O
C. ��·��ÿ����4 mol���ӣ�����������44.8 LH2S
D. ÿ17 g H2S���뷴Ӧ����1 mol H+������Ĥ����������
���𰸡�C
��������A������ͼʾ���缫a��H2Sʧȥ���ӱ�������S2���缫aΪ������A����ȷ��B���缫b��O2�����õ��ӵĻ�ԭ��Ӧ���缫��ӦʽΪO2+4H++4e-=2H2O��B����ȷ��C��H2S�ڸ��������ģ������缫��ӦʽΪ2H2S-4e-=S2+4H+����·������4mol���ӣ���������2molH2S��H2S�����¶Ⱥ�ѹǿδ֪������������H2S�������C�����D��n��H2S��=![]() =0.5mol���������������缫��Ӧʽ��ÿ17gH2S���뷴Ӧ��1molH+������Ĥ������������D����ȷ����ѡC��
=0.5mol���������������缫��Ӧʽ��ÿ17gH2S���뷴Ӧ��1molH+������Ĥ������������D����ȷ����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ�¶��£�ˮ��Һ��c(H��)��c(OH��)�Ĺ�ϵ��ͼ��ʾ�������й�˵������ȷ����(����)
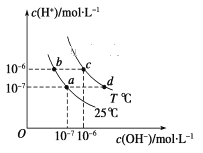
A. ����a�㵽c�㣬�ɲ�����ˮ�м�����ķ���
B. b���Ӧ�Ĵ�������ˮ�����c(H��)��10��6 mol��L��1
C. c���Ӧ��Һ��Kw����d���Ӧ��Һ��Kw
D. T ��ʱ��0.05 mol��L��1��Ba(OH)2��Һ��pH��11
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС�����Ʊ���������֤��һϵ�����ʣ�ʵ��װ����ͼ��ʾ��ʡ�Լг�װ�ã�����֪����������ƣ�Na2S2O3����Һ�ڹ�ҵ�Ͽ���Ϊ���ȼ�
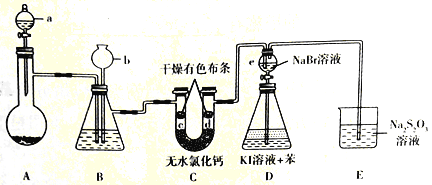
�ش��������⣺
��1������a��������______������ʢ��Ũ���ᣬ��ƿA ��ʢ�еĹ����Լ���_____���ѧʽ����
��2��װ��B��ʢ�б���NaCl��Һ��װ��B��������________��
a����ȥC12�е�����HCl b������
c���ṩ����ˮ���� d���۲�װ���Ƿ����
��3��c����ɫ������ɫ����d������ɫ����˵��__________��
��4��ʵ�������e �Ļ�����ʹ���е���Һ���˵���ƿD�У�ҡ����ƿ�����ú�ɹ۲쵽______________________��
��5��װ��E�з�����Ӧ�����ӷ���ʽΪ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǻ͵��۵Ļ�����������������Ϊ6.5������������������������Ϊ ( )
A. 13.0�� B. 39.0�� C. 45.5�� D. 52.0��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�ǰ�߸պ��Ǻ�����������
A. 2 molˮ��Ħ��������1 molˮ��Ħ������
B. 200 mL 1 mol��L��1�Ȼ�����Һ��c(Cl��)��100 mL 2 mol��L��1�Ȼ�����Һ��c(Cl��)
C. ��״���£�22.4 Lһ����̼����ԭ������16 g������������ԭ����
D. 2 mol��L��1H2SO4��Һ�е�H��������1 mol��L��1HCl��Һ�е�H������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijѧУʵ������ص������Լ���ǩ�IJ������ݡ��ж�����˵����ȷ����( )

A. �������Ũ��Ϊ9.2 mol��L��1
B. ����480 mL 4.6 mol��L��1��ϡ�������H2SO4125mL
C. ������������ˮ�������������Ϊ49%
D. ȡ������100 mL����Ũ�ȱ�Ϊԭ����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)���ڷ�Ӧ2CO��O2=2CO2���ڱ�״���£�4.48 Lһ����̼������������������Ӧ�����ɵĶ�����̼���Ӹ�����__________________��
(2)����һ��Ȫˮ��Ʒ��1.0 L����Ȫˮ����4.8��10-2 g Mg2+����ô����Ȫˮ��Mg2+�����ʵ���Ũ����_______________����1.0 mol Mg2+������Ȫˮ�������_______________����
(3)���mg������a��ԭ�ӹ��ɣ���2mg�����к��еķ�����Ϊ_____________(�ú�a�Ĵ���ʽ��ʾ)��
(4)0.2mol�ĵ���Ax��1.2molB2��ȫ��Ӧ������0.8mol��AB3������Ax�Ļ�ѧʽ��_____________��
(5)����δ֪Ũ�ȵ�����25mL���ܸ�20mLijŨ�ȵ�����������Һ��ȫ��Ӧ��������0.1g̼�����25mL���������ã�ʣ�����������������������Һ4mL�����к͡������������ʵ���Ũ��Ϊ______________������������Һ�����ʵ���Ũ��Ϊ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.ԭ������������Ϊ2��Ԫ��һ���������ڱ��ĵ�IIA��
B.H2O��H2S�ȶ�����ΪH2O���Ӽ������
C.���ӻ������п��ܺ��й��ۼ�
D.��Ϊ��������Ա������ᣨH2Sˮ��Һ��ǿ�����Էǽ����ԣ�Cl��S
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������нϸߵľ��ü�ֵ����ҵ�ϲ���һ����������������ˮʹ�����ŷŲ���������ij��Ʒ�ˮ�е�����Ҫ��NiR2�������ʽ���ڣ���ˮ��Һ�д�������ƽ�⣺NiR2 (aq) ![]() Ni2+(aq) +2R-(aq) ��R-Ϊ�л������壬K=1.6��10-14��
Ni2+(aq) +2R-(aq) ��R-Ϊ�л������壬K=1.6��10-14��
��1����ͳ�ġ�����������������ˮ�м���Na2S��ʹ���е�NiR2����NiS����������������
�ٸ÷�Ӧ�����ӷ���ʽΪ_________��
��NiS�������ɵ�ͬʱ��������Ni(OH)2�������ɣ������ӷ���ʽ����Ni(OH)2���ɵ�ԭ����_________��_________��
��2������������������Ļ����ʲ��ߣ��������ˮ�е����������Դ�ꡣ��������-��ѧ���������ɴﵽԤ��Ч�����÷�����ת��ΪNi(OH)2��������������������������£�
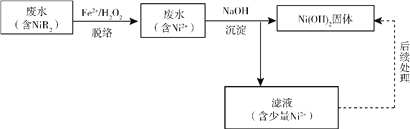
�����硱��ָ��Ԫ���������NiR2ת���������Ni2+�������У�R�����м���OH���ǻ����ɻ�����Ӧ����������Ni2+��ϵġ�R���л������ɻ���������OHҲ����H2O2������Ӧ����Ӧ�ķ���ʽ���£�
Fe2+ + H2O2 ![]() Fe3+ + OH�� +��OH ��������i
Fe3+ + OH�� +��OH ��������i
R�� + ��OH ![]() OH��+ ��R ��������ii
OH��+ ��R ��������ii
H2O2 +2��OH ![]() O2�� + 2H2O ��������iii
O2�� + 2H2O ��������iii
ʵ���á����硱������H2O2�ļ���������Һ����ȥ���ʵ�Ӱ������ͼ��ʾ��
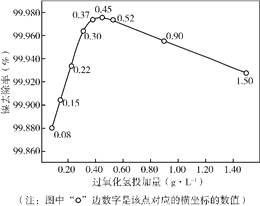
�ٴ�ƽ���ƶ��ĽǶȽ��ͼ���Fe2+��H2O2�ܹ�ʵ�֡����硱��ԭ����_________��
�ڷ���ͼ�����ߣ����ƶϹ����������Ѽ�����Ϊ_________ g��L-1�����ڻ�������ֵ����ˮ����Ч�����½���ԭ����_________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com