
����Ŀ��ŨH2SO4 �ܶ�1.84g/mL�����ʵ���Ũ��Ϊ18.4mol/L����������Ϊ98%��ȡ10mLŨH2SO4��a mLˮ��ϵ����ʵ���Ũ��ΪC mol/L����������Ϊb%�����������ȷ���ǣ� ��
��1����C=9.2��a��10 b��49%
��2����C=9.2��a��10 b��49%
��3����b=49��a=18.4 C��9.2
��4����b=49��a=18.4 C��9.2��
A����1����3�� B����1����4�� C����2����3�� D����2����4��
���𰸡�A
��������
�����������C=9.2������ϡ�Ͷ��ɣ���֪ϡ�ͺ���Һ�����Ϊ10mL��![]() =20mL�������Ũ��Խ���ܶ�Խ��ϡ�ͺ���Һ������С��ԭŨ����������2����ϡ����������������䣬��ϡ�ͺ������������������49%��ϡ����������������������䣬��10mL��1.84g/mL��98g%����10mL��1.84g/mL+amL��1g/mL����49%�����a��18.4����b=49��ϡ����������������������䣬��10mL��1.84g/mL��98g%=��10mL��1.84g/mL+amL��1g/mL����49%�����a=18.4����ϡ�ͺ���ܶ�Ϊdg/mL����d��1.84��ϡ��������ʵ���Ũ��C=
=20mL�������Ũ��Խ���ܶ�Խ��ϡ�ͺ���Һ������С��ԭŨ����������2����ϡ����������������䣬��ϡ�ͺ������������������49%��ϡ����������������������䣬��10mL��1.84g/mL��98g%����10mL��1.84g/mL+amL��1g/mL����49%�����a��18.4����b=49��ϡ����������������������䣬��10mL��1.84g/mL��98g%=��10mL��1.84g/mL+amL��1g/mL����49%�����a=18.4����ϡ�ͺ���ܶ�Ϊdg/mL����d��1.84��ϡ��������ʵ���Ũ��C=![]() mol/L��9.2mol/L����A��ȷ��
mol/L��9.2mol/L����A��ȷ��


 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(NaClO2)����Ư��֯���ά��ֽ�������ж���ά����С���ص㡣������Һ�п�����ClO2��HClO2��ClO2-��Cl- �ȣ�����HClO2��ClO2������Ư�����á���֪POH =-lgc(OH-)�����ⶨ25��ʱ����ֺ�����POH�仯�����ͼ��ʾ(Cl-û�л���)�����¶��£����з����������( )
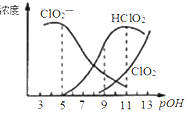
A�����������ڼ��������½��ȶ�
B��PH=7ʱ����Һ�к�������Ũ�ȴ�С��c(ClO2��)��c(HClO2)��c (ClO2)
C��HClO2�ĵ���ƽ�ⳣ������ֵKa=10-6
D��ͬŨ�ȵ�HClO2��Һ��NaClO2��Һ�������ϣ�������Һ����2c(HClO2)+c(H+)=2c(ClO2��) + c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮMgBr2������������ʵ���Ҳ���þм��Һ��Ϊԭ���Ʊ���ˮMgBr2��װ����ͼ1����Ҫ�������£�
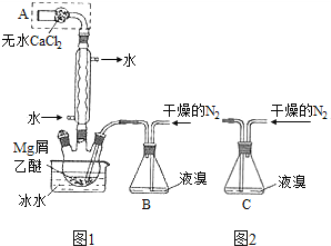
����1 ����ƿ��װ��10 gþм��150 mL��ˮ���ѣ�װ��B�м���15 mLҺ�塣
����2 ����ͨ�����ĵ�����ֱ������ȫ��������ƿ�С�
����3 ��Ӧ��Ϻ�ָ������£����ˣ���Һת������һ�������ƿ�У���ȴ��0�����������壬�ٹ��˵������Ѻ��廯þ��Ʒ��
����4 �������ñ��ܽ��Ʒ����ȴ��0�����������壬���ˣ�ϴ�ӵ������Ѻ��廯þ��������160 ���ֽ����ˮMgBr2��Ʒ��
��֪����Mg��Br2��Ӧ���ҷ��ȣ�MgBr2����ǿ��ˮ�ԡ�
��MgBr2+3C2H5OC2H5![]() MgBr2��3C2H5OC2H5
MgBr2��3C2H5OC2H5
��ش�
��1������A��������____________��ʵ���в����ø�������������N2��ԭ����___________��
��2���罫װ��B��Ϊװ��C(ͼ2)�����ܻᵼ�µĺ����___________��
��3������3�У���һ�ι��˳�ȥ��������___________��
��4���йز���4��˵������ȷ����___________��
A������95%���Ҵ����汽�ܽ��Ʒ
B��ϴ�Ӿ����ѡ��0���ı�
C��������160������ҪĿ���dz�ȥ��
D���ò����Ŀ���dz�ȥ���ѺͿ��ܲ�������
��5��Ϊ�ⶨ��Ʒ�Ĵ��ȣ�����EDTA(��дΪY4-)����Һ�ζ�����Ӧ�����ӷ���ʽ��
Mg2++Y4-=MgY2-
���ζ�ǰ��ϴ�ζ��ܵIJ���������__________��
���ⶨǰ���ȳ�ȡ0.2500g��ˮMgBr2��Ʒ���ܽ����0.0500 mol��L-1��EDTA����Һ�ζ����յ㣬����EDTA����Һ26.50 mL��������ˮMgBr2��Ʒ�Ĵ�����__________________(������������ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȩ��һ�ֻ���ԭ�ϡ�ijʵ��С����������װ�úϳ�����ȩ�������ķ�Ӧ���£�
CH3CH2CH2CH2OH![]() CH3CH2CH2CHO
CH3CH2CH2CHO
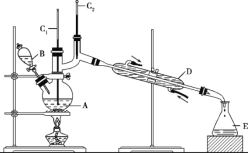
��Ӧ��Ͳ������������б����£�
�е�/��c | �ܶ�/(g��cm-3) | ˮ���ܽ��� | |
������ | 11.72 | 0.8109 | �� |
����ȩ | 75.7 | 0.8017 | �� |
ʵ�鲽�����£�
��6.0gNa2Cr2O7����100mL�ձ��У���30mLˮ�ܽ⣬�ٻ�������5mLŨ���ᣬ��������ҺС��ת����B�С���A�м���4.0g�������ͼ�����ʯ�����ȡ�������������ʱ����ʼ�μ�B����Һ���μӹ����б��ַ�Ӧ�¶�Ϊ90 ~ 95��C����E���ռ�90��C���µ���֡�
������ﵹ���Һ©���У���ȥˮ�㣬�л������������ռ�75 ~ 77��C��֣�����2.0g��
�ش��������⣺
��1��ʵ���У��ܷ�Na2Cr2O7��Һ�ӵ�Ũ�����У�˵������_______________________��
��2�������ʯ��������_____________�������Ⱥ���δ�ӷ�ʯ��Ӧ��ȡ����ȷ������__________________��
��3������װ��ͼ�У�B������������_________________��D������������___________________��
��4����Һ©��ʹ��ǰ������еIJ�����_____________(����ȷ�𰸱��)��
A����ʪ B������ C����© D���궨
��5��������ȩ�ֲ�Ʒ���ڷ�Һ©���з�ˮʱ��ˮ��____________��(����������������)
��6����Ӧ�¶�Ӧ������90~95��C����ԭ����__________________________��
��7����ʵ���У�����ȩ�IJ���Ϊ___________%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC4H9Cl��ͬ���칹�干��(�����������칹���� ��
A��3�� B��4�� C��5�� D��6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£�1���ˮ�ܽ�672���������������Һ�ܶ�Ϊ0.9g��cm��3�����ְ�ˮ�����ʵ���Ũ�Ⱥ����ʵ����������ֱ�Ϊ( ��
A��17.9mol��L��1 34.7% B��20.4mol��L��1 33.8%
C��17.9mol��L��1 33.8% D��20.4mol��L��1 34.7%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�����ۼס��ҡ���������������װ�õ��й��÷������в��������ǣ� ��
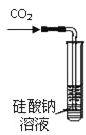
A����װ�ã�������֤��̼�ķǽ����Աȹ�ǿ

B����װ�ã���Ƥ�ܵ���������ʹˮ˳������

C����װ�ã���ͼʾ�ķ������ܼ���װ�õ�������

D����װ�ã��ȴӢٿڽ�������������̼���ٴӢڿڽ��������ռ�NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����200mL MgCl2��AlCl3�Ļ����Һ�У�c(Mg2+)=0.2mol/L��c(Cl)=1.3mol/L����Ҫʹ���е�Mg2+ȫ��ת��Ϊ���������������������Ҫ4mol/L��NaOH��Һ�����Ϊ( )
A��120mL B��80mL C��40mL D��20mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�У�A��B��C��D��E�ǵ��ʣ�G��H��I��F��B��C��D��E�ֱ��A�γɵĶ�Ԫ�����

��֪���ٷ�Ӧ![]() �ܷų��������ȣ��÷�Ӧ��Ӧ��������ĺ��ӣ�
�ܷų��������ȣ��÷�Ӧ��Ӧ��������ĺ��ӣ�
��I��һ�ֳ������������壬����![]() ���Է�����Ӧ��2E��I 2F��D��F�е�EԪ�ص���������Ϊ60%.�ش����⣺
���Է�����Ӧ��2E��I 2F��D��F�е�EԪ�ص���������Ϊ60%.�ش����⣺
��1�����з�Ӧ�Ļ�ѧ����ʽΪ_____________________��
��2���������ĵ���ʽΪ________________,���Ŀռ乹����_________��
��3��1.6g G �������ᣬ�õ�����Һ��ͭ����ȫ��Ӧ����������ͭ�۵�����Ϊ g��
��4��C�����NaOH��Һ��Ӧ�����ӷ���ʽΪ_____________����Ӧ����Һ������������Ӧ�����ӷ���ʽ��__________________;
��5��ʵ������һ�����I���ڵ��Լ��ͷ�������___________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com