
| A、FeSO4可用于防止食品氧化变质,延长食品的保质期 |
| B、向FeSO4中加入NaOH溶液,观察到有灰白色的沉淀生成,灰白色的沉淀迅速变成灰绿色,最后变成红褐色 |
| C、向Fe2(SO4)3溶液中加入足量铁粉,充分反应后滴加KSCN溶液,溶液马上变成血红色 |
| D、铁在氧气中燃烧,生成黑色的Fe3O4 |


科目:高中化学 来源: 题型:
| C(OH-) |
| C(H+) |
| A、该一元碱(AOH)溶液的pH=13 |
| B、该溶液中水电离出的C(OH-)=10-3 mol?L-1 |
| C、将pH=1的盐酸溶液V1 L与0.1 mol?L-1 AOH溶液V2 L混合,若混合溶液pH=7,则V1=V2 |
| D、将pH=1的盐酸溶液V1L与0.1 mol?L-1 AOH溶液V2 L混合,若混合溶液pH>7,则溶液中离子浓度由大到小的顺序可能为C(A+)>C(Cl-)>C(OH-)>C(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在电解池中,与电源正极相连的电极是阴极 |
| B、在电解池中,物质在阴极发生氧化反应 |
| C、在原电池中,物质在负极发生氧化反应 |
| D、在原电池中,电子在正极流向负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇和乙酸能发生酯化反应,只要一种反应物过量酯化反应就能进行彻底 |
| B、乙醇、乙酸和乙酸乙酯三者的混合液可用分液的方法将三者分离 |
| C、煤的气化和煤的干馏都发生了化学变化,而石油的分馏属于物理变化 |
| D、苯不能使酸性高锰酸钾溶液褪色,因此苯不能发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a=2,b=6 |
| B、a=4,b=18 |
| C、a=6,b=16 |
| D、a=8,b=18 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤⑥ | B、①②④⑤ |
| C、①②③④ | D、只有①③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用N2浓度的减少表示的平均反应速率为0.2 mol?L-1?s-1 |
| B、2 s时N2的转化率为40% |
| C、2 s时混合气体中n(N2)?n(H2)?n(NH3)=3:9:4 |
| D、2 s 时NH3的浓度为0.4 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
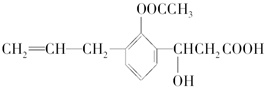
| A、①②③④⑥ | B、②④⑥ |
| C、②④⑤⑥ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO为氧化产物,H2为还原产物 |
| B、CaCN2中含有非极性键 |
| C、HCN既是氧化剂又是还原剂 |
| D、每消耗10g CaCO3生成2.24L CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com