
【题目】M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M基态原子L层中p轨道电子数是s轨道电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满。请回答下列问题:
(1)R基态原子的电子排布式是_____,X和Y中电负性较大的是__(填元素符号)。
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是___________。
(3)X与M形成的XM3分子的空间构型是__________。
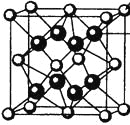
(4)M和R所形成的一种离子化合物R2M晶体的晶胞如图所示,则图中黑球代表的离子是_________(填离子符号)。
(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的化学方程式是____________。
【答案】1s22s22p63s1或[Ne]3s1 Cl H2S分子间不存在氢键,H2O分子间存在氢键 平面三角形 Na+ K2Cr2O7+3H2O2+ 4H2SO4=K2SO4+Cr2(SO4)3+3O2↑+7H2O
【解析】
M元素的2p电子数是2s的2倍,故价电子排布应为2s22p4,M为氧元素。R的原子序数比氧大,又是短周期金属,故只能是第三周期。第三周期最活泼的金属是钠。X与M的化合物,引起酸雨,只有可能是二氧化硫或氮氧化物。但是X的原子序数比氧大,故X只能是硫元素。Y的原子序数比X大,又是短周期元素,只能是氯元素。Z的最高价含氧酸的钾盐是橙色,这是重铬酸盐的典型颜色。题目中关于4s、3d轨道半充满的描述,也能推出Z是铬元素(3d54s1)。
(1)钠元素的基态电子排布为1s22s22p63s1,同周期元素从左到右电负性增大,Cl的电负性比S大。
(2)H2O之间有氢键,而H2S之间没有氢键。分子间氢键会导致化合物熔沸点升高。
(3)对于SO3分子,价电子对数为3,孤电子对数为![]() ,所以分子应该是平面三角形。
,所以分子应该是平面三角形。
(4)R2M为Na2O。晶胞中黑球全部在晶胞内部,故有8个,白球有![]() 个,二者比例为2:1。故黑球为Na+。
个,二者比例为2:1。故黑球为Na+。
(5)水的化学性质稳定,不会与重铬酸钾反应,被氧化的M的氢化物只能是H2O2,氧化产物是O2。根据题目,还原产物中Cr为+3价,反应又在稀硫酸中进行,故还原产物为Cr2(SO4)3。根据元素守恒,另两个产物是K2SO4和H2O。该反应的化学方程式是K2Cr2O7+3H2O2+ 4H2SO4 =K2SO4+Cr2(SO4)3+3O2↑+7H2O。


科目:高中化学 来源: 题型:
【题目】实验室需要0.1 mol·L-1 NaOH溶液490mL。根据溶液的配制情况回答下列问题。
(1)配制上述溶液需要的玻璃仪器有烧杯、玻璃棒、量筒、__________、__________。
(2)配制时,正确的操作顺序是(用字母表示,每个操作只用一次)__________。
A.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶液
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
(3)实验两次用到玻璃棒,其作用分别是:先用于__________、后用于__________。
(4)报据计算用托盘天平称取NaOH固体的质量为__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
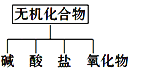
【题目】(1)无机化合物可根据其组成和性质进行分类:
ⅰ、下图所示的物质分类方法名称是________。
ⅱ、以Na、K、H、O、C、S中任意两种或三种元素组成合适的物质,分别填在下表②③⑥的后面。
物质类别 | 酸 | 碱 | 盐 | 氧化物 |
化学式 | ①HCl ② __ | ③ __ ④ Ba(OH)2 | ⑤ Na2CO3 ⑥ ___ | ⑦ CO2 ⑧ H2O |
ⅲ、 写出⑦通入到过量的④溶液中的离子方程式:_________。
ⅳ、 实验室检验气态⑧的方法是___________。
(2)某无色透明溶液,跟金属铝反应放出H2,判断下列离子:Mg2+、Ba2+、Cu2+、H+、Ag+、SO42-、SO32-、OH-、HCO3-、NO3-,哪种离子能大量存在于此溶液中。
ⅰ、 生成Al3+时,原无色透明溶液能够大量存在的离子有_______。
ⅱ、生成AlO2-时,原无色透明溶液能够大量存在的离子有_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V mL Al2(SO4)3溶液中含有Al3+ a g,取0.5V mL溶液稀释到8V mL,则稀释后溶液中SO42-的物质的量浓度是
A. ![]() mol/L B.
mol/L B. ![]() mol/L C.
mol/L C. ![]() mol/L D.
mol/L D. ![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
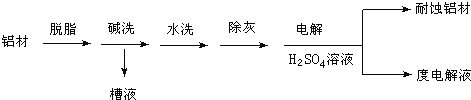
碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是______(用离子方程式表示)。为将碱洗槽液中的铝元素以沉淀形式回收,最好向槽液中加入下列试剂中的____。
a.NH3 b.CO2 c.NaOH d.HNO3
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是________。
(3)利用下图装置,可以模拟铁的电化学防护。
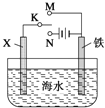
若X为碳棒,为减缓铁的腐蚀,开关K应置于______处。
若X为锌,开关K置于M处,该电化学防护法称为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 石油分馏、硝基苯的制备和乙烯的制取中温度计的位置都不相同
B. 向苯溴代实验后的溶液中加水,可观察到溶液分三层为有苯层、水层和溴苯层
C. 卤代烃中卤原子的检验,可以向卤代烃水解后的产物中直接滴加![]() 溶液
溶液
D. 乙醇与浓硫酸反应所制得的气体通入到溴水中,若溴水褪色即可证明有乙烯产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,在三个容积均为1L的恒容密闭容器中仅发生反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,达到平衡时,下列说法不正确的是
2SO3(g) ΔH<0,达到平衡时,下列说法不正确的是
容器 编号 | 容器类型 | 起始物质的量 / mol | 平衡时SO3的物质的量 / mol | ||
SO2 | O2 | SO3 | |||
I | 恒温恒容 | 2 | 1 | 0 | 1.8 |
II | 恒温恒压 | 2 | 1 | 0 | a |
III | 绝热恒容 | 0 | 0 | 2 | b |
A. 容器I中SO2的转化率小于容器II中SO2的转化率
B. 容器II的平衡常数大于容器III中的平衡常数
C. 平衡时SO3的物质的量:a>1.8、b>1.8
D. 若起始时向容器I中充入0.10 mol SO2(g)、0.20mol O2(g)和2.0 mol SO3(g),则此时v正<v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是
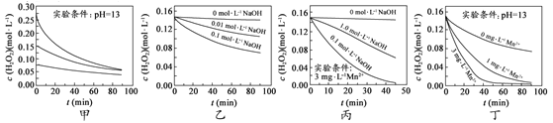
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com