
【题目】四种短周期主族元素![]() 和W的原子序数依次增大,X和Y的单质化合生成气体A,A分子中的电子数与氖原子相同,X和W的单质化合生成气体B,常温下
和W的原子序数依次增大,X和Y的单质化合生成气体A,A分子中的电子数与氖原子相同,X和W的单质化合生成气体B,常温下![]() 的B溶液的
的B溶液的![]() ,气体A和气体B相遇产生白烟,X与Z可按原子个数比1∶1形成化合物C。下列说法正确的是( )
,气体A和气体B相遇产生白烟,X与Z可按原子个数比1∶1形成化合物C。下列说法正确的是( )
A.化合物C可能为离子化合物
B.Z离子的半径比Y离子的大
C.Y的非金属性很强,其单质非常活泼
D.氧化物的水化物的酸性:Y比W强
【答案】A
【解析】
四种短周期主族元素X、Y、Z和W,原子序数依次增大,X和W的单质化合生成气体B,常温下0.1mol/L的B溶液的pH=1,则B为强酸性气体,为HCl,则X是H、W是Cl元素;气体A和气体B相遇产生白烟,白烟为氯化铵,则A是氨气;X和Y的单质化合生成气体A,A分子中的电子数与氖原子相同,所以Y是N元素;X与Z可按原子个数比1: 1形成化合物C,且Z原子序数大于N而小于Cl元素,则Z为O、F或Na元素,C可能是H2O2、HF或NaH。
A.根据上述分析可知:化合物C可能是H2O2、HF或NaH。 HF是共价化合物而NaH是离子化合物 故A正确;
B. 根据上述分析可知:Y为N元素、Z为O或F或Na元素,电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径: Y>Z,故B错误;
C. 根据上述分析可知:Y为N元素,Y的非金属性很强,但是因为氮气分子中存在氮氮三键导致其性质较稳定而不活泼,故C错误;
D. 根据上述分析可知:W是Cl元素,Y为N元素,非金属性W>Y,则最高价氧化物的水合物酸性高氯酸大于硝酸,故D错误;
故选 A。


科目:高中化学 来源: 题型:
【题目】标明下列反应电子转移情况,并根据要求回答问题。
(1)3NO2+H2O=2HNO3+NO_______
(2)氧化剂____________还原剂____________氧化产物____________还原产物__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解结晶水合物CuCl·2H2O制备CuCl,并进行相关探究。
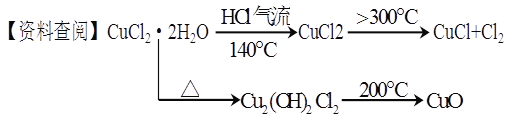
【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)仪器X的名称是 。
(2)实验操作的先后顺序是![]()
![]() (填操作的编号)。
(填操作的编号)。
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是 。
(4)装置D中发生的氧化还原反应的离子方程式是 。
【探究反思】
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是 。
②若杂质是CuO,则产生的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置,在仪器①②③中分别依次加入下列各选项中所对应的试剂进行实验,能达到实验目的的是

A. 浓盐酸、浓硫酸、浓硫酸,制取干燥的氯化氢气体
B. 浓盐酸、二氧化锰、饱和食盐水,制取纯浄的氯气
C. 稀硫酸、溶液X、澄清石灰水,检验溶液X中是否含有CO32—
D. 浓盐酸、碳酸钙、水玻璃,验证盐酸、碳酸、硅酸的酸性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.将铁粉加入![]() 、
、![]() 混合溶液中,充分反应后剩余的固体中必有铁
混合溶液中,充分反应后剩余的固体中必有铁
B.将![]() 和
和![]() 混合气体分别通入
混合气体分别通入![]() 溶液、
溶液、![]() 溶液中,最终都有沉淀生成
溶液中,最终都有沉淀生成
C.检验某酸性溶液中![]() 和
和![]() ,选用试剂及顺序是过量
,选用试剂及顺序是过量![]() 溶液、
溶液、![]() 溶液
溶液
D.用加热分解的方法可将![]() 固体和Ca(OH)2固体的混合物分离
固体和Ca(OH)2固体的混合物分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得结论正确的是
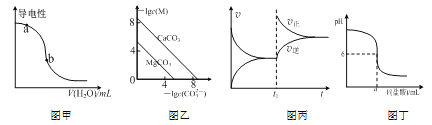
A.图甲表示一定温度下,CH3COOH稀溶液加水时溶液的导电性变化,则pH(a)>pH(b)
B.图乙表示一定温度下,MCO3(M:Mg2+、Ca2+)的沉淀溶解平衡曲线,则Ksp(MgCO3)<Ksp(CaCO3)
C.图丙表示一定温度下,可逆反应N2(g)+3H2(g) ![]() 2NH3(g)正逆反应速率随时间变化的曲线,t1时改变的条件可能是分离出NH3
2NH3(g)正逆反应速率随时间变化的曲线,t1时改变的条件可能是分离出NH3
D.图丁表示常温下将0.1 mol·L-1盐酸溶液滴加到a mL0.1 mol·L-1BOH溶液中,所得溶液pH随所加入盐酸溶液体积的变化图,则BOH为弱碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用方铅矿精矿(主要为![]() )和软锰矿(主要为
)和软锰矿(主要为![]() ,还有少量
,还有少量![]() 、
、![]() 等杂质)制备
等杂质)制备![]() 和
和![]() 的工艺流程如图:
的工艺流程如图:
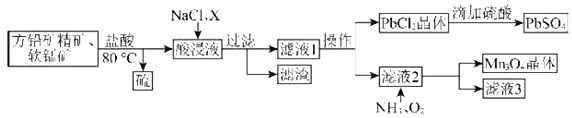
已知:①![]() 。
。
②![]() 。
。
(1)80℃用盐酸处理两种矿石,为加快酸浸速率,还可采用的方法是____________(任写一种)。
(2)向酸浸液中加入饱和食盐水的目的是_____________;加入物质X可用于调节酸浸液的![]() 值,物质X可以是___________(填字母)。
值,物质X可以是___________(填字母)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(3)滤渣中含有两种金属杂质形成的化合物,其成分为___________(写化学式)。
(4)向滤液2中通入![]() 和
和![]() 发生反应,写出总反应的离子方程式:________________。
发生反应,写出总反应的离子方程式:________________。
(5)用![]() 为原料可以获得金属锰,合适的冶炼方法为____________(填字母)。
为原料可以获得金属锰,合适的冶炼方法为____________(填字母)。
A.热还原法 B.电解法 C.热分解法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚砜(SOCl2)是一种液态化合物,沸点为77℃,在农药、制药行业中用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生。实验室合成原理:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示,(已知SCl2的沸点为50℃),回答以下问题:
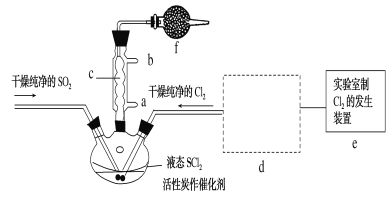
(1)下列四种制备SO2的方案中最佳选择是__。
方案 | A | B | C | D |
发生装置 |
|
|
|
|
所选试剂 | 70%H2SO4+K2SO3 | 18.4mol/LH2SO4+Cu | 4mol/LHNO3+Na2SO3 | NaHSO3固体 |
(2)以MnO2和浓盐酸为原料制备Cl2的离子方程式为__。
(3)仪器f的作用是__。
(4)d的虚线框内隐含两个装置,按气流方向顺序这两个装置的药品分别是__。
(5)实验结束后,将三颈烧瓶混合物中产品分离出来的方法是__。
(6)若用SOCl2作FeCl3·6H2O的脱水剂,设计实验证明脱水时发生了氧化还原反应。取少量FeCl3·6H2O于试管中,加入过量SOCl2,振荡,往试管中加水溶解,滴加__或__溶液,证明脱水过程发生了氧化还原反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物J是一种重要的医药中间体,其合成路线如图:
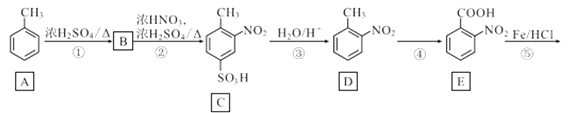
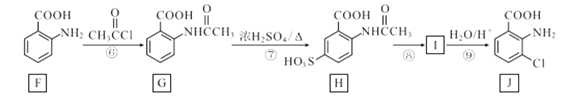
回答下列问题:
(1)G中官能团的名称是__;③的反应类型是__。
(2)通过反应②和反应⑧推知引入—SO3H的作用是__。
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。写出F与足量氢气反应生成产物的结构简式,并用星号(*)标出其中的手性碳__。
(4)写出⑨的反应方程式__。
(5)写出D的苯环上有三个不相同且互不相邻的取代基的同分异构体结构简式_。
(6)写出以对硝基甲苯为主要原料(无机试剂任选),经最少步骤制备含肽键聚合物的合成路线__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com