
����Ŀ����һ��������þ���Ͻ�Ͷ��100mLһ��Ũ�ȵ������У��Ͻ���ȫ�ܽ⣮��������Һ�еμ�Ũ��Ϊ5mol/L��NaOH��Һ�����ɵij����������NaOH��Һ�������ϵ��ͼ���������������λ��mL��������������λ��g�� 
��
��1������NaOH��Һ0����20mL�����з�Ӧ�����ӷ���ʽΪ��������Al��OH��3������Ϊg��
��2���Ͻ���Mg������Ϊ������HCl�����ʵ���Ũ��Ϊmol/L��
���𰸡�
��1��H++OH��=H2O��7.8
��2��4.8g��8
���������⣺��1����ͼ��֪���ӿ�ʼ������NaOH��Һ20mL��û�г������ɣ�˵��ԭ��Һ�������ܽ�Mg��Al��������ʣ�࣬��ʱ�����ķ�ӦΪ��HCl+NaOH=NaCl+H2O����Ӧ���ӷ���ʽΪ��H++OH��=H2O�������μ�NaOH��Һ��������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3 �� ��ҺΪ�Ȼ�����Һ���ټ����μ�NaOH��Һ�������������������Ʒ�Ӧ����ƫ��������ˮ��������ӦAl��OH��3+NaOH=NaAlO2+2H2O������n[Al��OH��3]=��0.18L��0.16L����5mol/L=0.1mol����m[Al��OH��3]=0.1mol��78g/mol=7.8g�����Դ��ǣ�H++OH��=H2O��7.8g����2����ͼ��֪���Ӽ���20m����������ҺL��ʼ������������������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3 �� �ý�������������140mL�����������غ��֪3n[Al��OH��3]+2n[Mg��OH��2]=n��NaOH��=��0.16L��0.02L����5mol/L=0.7mol����3��0.1mol+2n[Mg��OH��2]=0.7mol�����n[Mg��OH��2]=0.2mol����Ԫ���غ��֪n��Mg��=n[Mg��OH��2]=0.2mol������Mg������Ϊ0.2mol��24g/mol=4.8g�����������ʱ����ҺΪ�Ȼ�����Һ��������Ԫ���غ��ʱ��Һ��n��NaCl��=n��NaOH��=0.16L��5mol/L=0.8mol��������Ԫ���غ�n��HCl��=0.8mol������������ʵ���Ũ��Ϊ ![]() =8mol/L�� ���Դ��ǣ�4.8��8��
=8mol/L�� ���Դ��ǣ�4.8��8��


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��A����Է�������Ϊ28������ʹ������Ȼ�̼��Һ��ɫ��F�߷��ӻ������������ת����ϵ�� 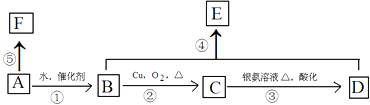
��Ҫ����գ�
��1��д��C�����������ŵ����� �� ָ���ܵķ�Ӧ���� ��
��2����Bת��ΪA�����跴Ӧ����Ϊ�� ��
��3��д��B��F�ṹ��ʽ��B��F ��
��4��д����Ӧ�۶�Ӧ�Ļ�ѧ����ʽ�� ��
��5��д����Ӧ�ܶ�Ӧ�Ļ�ѧ����ʽ�� ��
��6��E��ͬ���칹���ж��֣���������NaHCO3��Ӧ��ͬ���칹�干���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������й�ij�ֵ���ø��ʵ�飬������ʽ����������ͼ��ʾ�����ݽ���жϣ�������ȷ���� �� ��
�Թܱ�� | �Թܢ� | �Թܢ� | �Թܢ� |
pH | 8 | 8 | 7 |
�¶� | 60�� | 40�� | 40�� |
����ø | 1mL | 1mL | 1mL |
���� | 1mL | 1mL | 1mL |

A���������ǵ���ø���Ƽ�
B�����ֵ���ø������35min����ʧȥ����
C�����ֵ���ø�����Ի����е��������ʱ��ڼ����еĿ�
D�����ֵ���ø���ʺ���40��Ļ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ҫ�Ļ����л�����ԭ��֮һ�������ñ���ͬʱʹ�����������Լ�����ʵ������ת������ش��������⣺ 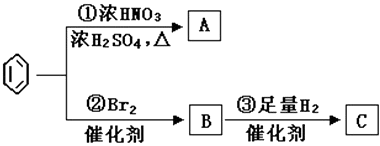
��1��C�Ľṹ��ʽΪ��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ����Ӧ�٣�����Ӧ�ڣ���
��3��������Ӧ�١����У����ڼӳɷ�Ӧ����������ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�����������������ȷ���ǣ� ��
A.��״���£�11.2L SO3����������Ϊ0.5 NA
B.1L 1mol/L���Ȼ�����Һ�У�����������ΪNA
C.64g����������ԭ����Ϊ3NA
D.�ڷ�Ӧ�У�1molþת��ΪMg2+��ʧȥ�ĵ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ֵ����������е�������������Ϊ7��16�������ֵ���������Ļ�ѧʽ��
A. NO B. NO2 C. N2O D. N2O5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼΪ������Ԫ�ء������P�����������̡���ʽ;��֮�����ϵ����ط�����ȷ����( )

A. ��35S��ǵ�������������ϸ����һ��ʱ���ס��ҡ����ж��ܼ�������
B. ��Ȼ����������״�Ķ�����ֻ�����ڼ����ʵĶ�������ɵ�
C. ���Ѽ��ڼ������������࣬��������������������
D. ͼ�����������̼����Է�ʽ����ȫ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ�����ӵ���������ֵ������˵����ȷ���ǣ� ��
A.7.2 g CaO2�����������Ӻ�����������Ϊ0.3 NA
B.0.1 mol/L NH4Cl��Һ��Cl��������ĿΪ0.1 NA
C.��Ӧ3H2��g��+N2��g��2NH3��g����H=��92 kJ/mol�ų�����9.2 kJʱ��ת�Ƶ���0.6 NA
D.0.1 mol H2O2�����к����Թ��ۼ���ĿΪ0.3 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ�������ж���ȷ���ǣ� ��
A.4.48LH2��O2�Ļ������������������Ϊ0.2NA
B.��״���£�1.8g��H2O�к��еĵ�����Ϊ0.1NA
C.53.5 g�Ȼ�茶����к���NH ![]() ����ĿΪNA
����ĿΪNA
D.��״���£�22.4 L���������е�ԭ����Ϊ2NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com