
【题目】苯是最重要的基本有机化工原料之一,现利用苯,同时使用其他部分试剂,可实现如下转化:请回答下列问题: 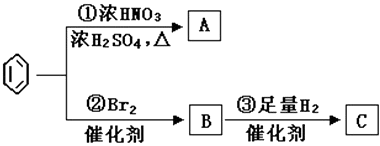
(1)C的结构简式为;
(2)写出下列反应的化学方程式:反应①:;反应②:;
(3)上述反应①~③中,属于加成反应的是(填序号).
科目:高中化学 来源: 题型:
【题目】某研究小组利用含硫酸铜的工业废液制备硫酸铵,流程如下: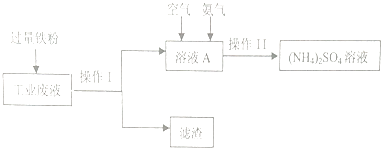
(1)操作Ⅰ的名称为 , 滤渣的成分为 .
(2)工业废液中加入过量铁粉所发生反应的离子方程式为 .
(3)操作Ⅱ得到的(NH4)2SO4溶液进行蒸发浓缩,需要的仪器除了酒精灯、铁架台、蒸发皿外,还需要 .
(4)如图溶液A中发生反应的离子方程式为4Fe2++O2+8NH3+10H2O=8NH4++4Fe(OH)3↓该反应是否为氧化还原反应(填“是”或“否”).
(5)检验(NH4)2SO4溶液中含有SO ![]() 的方法为 .
的方法为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列判断正确的是
A. 常温常压下,18gH2O中含氢原子数为NA
B. 标准状况下,5.6L四氯化碳中含有的氯原子数为NA
C. 常温下,1mol·L-1NaClO溶液中含有的钠离子数为NA
D. 标准状况下,14gCO和N2的混和气体中含有的原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H1N1病毒是一种没有超常抵抗力的病毒.研究证明,许多常用消毒药物如漂粉精、漂白粉、高锰酸钾等,可以将H1N1病毒杀灭.
(1)工业上制取漂白粉的反应方程式为 .
(2)将漂白粉溶于适量水中,呈白色浊状物,静置沉降.取少许上层清液,滴加碳酸钠溶液出现白色沉淀,写出其中一个化学方程式 . 另取少许上层清液,滴加适量的(填化学式)即可检验Cl﹣的存在,发生反应的化学方程式为 .
(3)漂白粉在空气中长期放置,会失效,用化学方程式解释其原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有AgCl(s)的饱和AgCl溶液中加水,下列叙述正确的是( )
A.AgCl的溶解度增大
B.AgCl的溶解度、Ksp均不变
C.Ksp(AgCl)增大
D.AgCl的溶解度、Ksp均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是同学们经常使用的某品牌修正液包装标签.小明仔细阅读后,结合自己的生活经验和所学知识得出了修正液的某些性质,小明的推测中不合理的是( ) 
A.修正液是一种胶体,均一、稳定
B.修正液中含有有毒的化学物质
C.修正液的成分对纸张不具腐蚀性
D.修正液的溶剂易挥发、易燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g) 
求:
(1)加入NaOH溶液0﹣﹣20mL过程中反应的离子方程式为;沉淀中Al(OH)3的质量为g.
(2)合金中Mg的质量为;所用HCl的物质的量浓度为mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是叶绿素分子(左)和血红蛋白分子(右)的局部结构简图,说法不正确的是

A. 合成叶绿素和血红蛋白分别需要镁和铁
B. 植物体缺镁会影响光合作用
C. 人体缺铁会影响血红蛋白对氧的运输
D. Mg和Fe分别存在于植物和动物细胞中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:
C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)
已知燃烧1kg该化合物释放出热量3.8×104kJ,油酸甘油酯的燃烧热为( )
A.3.8×104kJmol﹣1
B.﹣3.8×104kJmol﹣1
C.3.4×104kJmol﹣1
D.﹣3.4×104kJmol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com