
【题目】某研究小组利用含硫酸铜的工业废液制备硫酸铵,流程如下: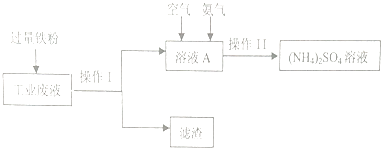
(1)操作Ⅰ的名称为 , 滤渣的成分为 .
(2)工业废液中加入过量铁粉所发生反应的离子方程式为 .
(3)操作Ⅱ得到的(NH4)2SO4溶液进行蒸发浓缩,需要的仪器除了酒精灯、铁架台、蒸发皿外,还需要 .
(4)如图溶液A中发生反应的离子方程式为4Fe2++O2+8NH3+10H2O=8NH4++4Fe(OH)3↓该反应是否为氧化还原反应(填“是”或“否”).
(5)检验(NH4)2SO4溶液中含有SO ![]() 的方法为 .
的方法为 .
【答案】
(1)过滤;Fe、Cu
(2)Fe+Cu2+=Fe2++Cu
(3)玻璃杯
(4)是
(5)取溶液少许于试管中,先加入足量稀盐酸,再加入氯化钡溶液,产生白色沉淀,则证明有SO ![]() 存在
存在
【解析】解:实验目的是利用含硫酸铜的工业废液制备硫酸铵,根据流程可知,向废液中加入过量铁粉,将硫酸铜转化成硫酸亚铁,过滤后得到滤液A硫酸亚铁溶液,向硫酸亚铁溶液中通入空气和氨气,发生反应:4Fe2++O2+8NH3+10H2O=8NH ![]() +4Fe(OH)3↓,将亚铁离子转化成氢氧化铁除去,从而得到硫酸铵,最后通过蒸发浓缩,得到硫酸铵溶液,(1)操作Ⅰ是将固体Fe、Cu与溶液分离,该操作方法为过滤;过滤得到的滤渣为Fe、Cu,滤液为硫酸亚铁溶液,所以答案是:过滤; Fe、Cu;(2)工业废液中加入过量铁粉,铜离子与铁发生置换反应生成亚铁离子和铜,所发生反应的离子方程式为:Fe+Cu2+=Fe2++Cu, 所以答案是:Fe+Cu2+=Fe2++Cu;(3)操作Ⅱ得到的(NH4)2SO4溶液进行蒸发浓缩,需要的仪器除了酒精灯、铁架台、蒸发皿外,还需要用玻璃杯搅拌,所以答案是:玻璃棒;(4)如图溶液A中发生反应的离子方程式为4Fe2++O2+8NH3+10H2O=8NH4++4Fe(OH)3↓,该反应中亚铁离子被氧化成铁离子,氧气从0价变为﹣2价,存在化合价变化,所以该反应是氧化还原反应,所以答案是:是;(5)验(NH4)2SO4溶液中含有SO42﹣ , 可用稀盐酸和氯化钡溶液检验,操作方法为:取溶液少许于试管中,先加入足量稀盐酸,再加入氯化钡溶液,产生白色沉淀,则证明有SO42﹣存在,所以答案是:取溶液少许于试管中,先加入足量稀盐酸,再加入氯化钡溶液,产生白色沉淀,则证明有SO42﹣存在.
+4Fe(OH)3↓,将亚铁离子转化成氢氧化铁除去,从而得到硫酸铵,最后通过蒸发浓缩,得到硫酸铵溶液,(1)操作Ⅰ是将固体Fe、Cu与溶液分离,该操作方法为过滤;过滤得到的滤渣为Fe、Cu,滤液为硫酸亚铁溶液,所以答案是:过滤; Fe、Cu;(2)工业废液中加入过量铁粉,铜离子与铁发生置换反应生成亚铁离子和铜,所发生反应的离子方程式为:Fe+Cu2+=Fe2++Cu, 所以答案是:Fe+Cu2+=Fe2++Cu;(3)操作Ⅱ得到的(NH4)2SO4溶液进行蒸发浓缩,需要的仪器除了酒精灯、铁架台、蒸发皿外,还需要用玻璃杯搅拌,所以答案是:玻璃棒;(4)如图溶液A中发生反应的离子方程式为4Fe2++O2+8NH3+10H2O=8NH4++4Fe(OH)3↓,该反应中亚铁离子被氧化成铁离子,氧气从0价变为﹣2价,存在化合价变化,所以该反应是氧化还原反应,所以答案是:是;(5)验(NH4)2SO4溶液中含有SO42﹣ , 可用稀盐酸和氯化钡溶液检验,操作方法为:取溶液少许于试管中,先加入足量稀盐酸,再加入氯化钡溶液,产生白色沉淀,则证明有SO42﹣存在,所以答案是:取溶液少许于试管中,先加入足量稀盐酸,再加入氯化钡溶液,产生白色沉淀,则证明有SO42﹣存在.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】硫单质及其化合物在工农业生产中有着重要的应用,请回答下列问题: 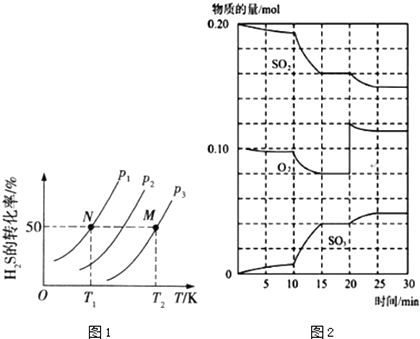
(1)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下: ①CaSO4(s)+CO(g)CaO(s)+SO2(g)+CO2(g)△=+210.5kJmol﹣1
② ![]() CaSO4(s)+CO(g)
CaSO4(s)+CO(g) ![]() CaS(s)+CO2(g)△=﹣47.3kJmol﹣1
CaS(s)+CO2(g)△=﹣47.3kJmol﹣1
反应:CaO(s)+3CO(g)+SO2(g)CaS(s)+3CO2(g)△H=kJmol﹣1
平衡常数K的表达式为 .
(2)图1为密闭容器中H2S气体分解生产H2和S2(g)的平衡转化率与温度、压强的关系. 图1中压强P1、P2、P3的大小顺序为 , 理由是 , 该反应平衡常数的大小关系为K(T1)K(T2)(“>”“=”或“<”),理由是
(3)在一定条件下,二氧化硫和氧气发生反应:2SO2(g)+O2(g)2SO3△H<0 ①600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图2,反应处于平衡状态的时间段所示
②据图2判断,反应进行至20min时,曲线发生变化的原因是(用文字表达):10min到15min的曲线变化的原因可能是(填写编号)
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加SO2的物质的量
(4)烟气中SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=(用含硫微粒浓度的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,在体积为VL的密闭容器中发生反应:mA+nBpC.t秒末,A减少了1mol,B减少了1.25mol,C增加了0.5mol.则m:n:p应为( )
A.4:5:2
B.2:5:4
C.1:3:2
D.3:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下: 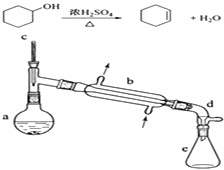
可能用到的有关数据如下:
相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸.b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置a的名称是 .
(2)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并;在本实验分离过程中,产物应该从分液漏斗的(填“上口倒出”或“下口放出”).
(4)分离提纯过程中加入无水氯化钙的目的是 .
(5)在环己烯粗产物蒸馏过程中,可能用到的仪器有 ABE (填正确答案标号).
A圆底烧瓶 B温度计 C漏斗 D玻璃棒 E接收器
(6)本实验所得到的环己烯产率是 . (保留两位有效数字)
(注:产率= ![]() ×100%)
×100%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是
A. 肯定有SO2和NO B. 肯定没有Cl2和NO2 ,可能有O2
C. 可能有Cl2和O2 D. 肯定只有NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A的相对分子质量为28,可以使溴的四氯化碳溶液褪色,F高分子化合物,它有如下转化关系: 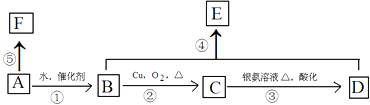
按要求填空:
(1)写出C中所含官能团的名称 , 指出④的反应类型 .
(2)若B转化为A,所需反应条件为: .
(3)写出B和F结构简式:B;F .
(4)写出反应③对应的化学方程式: .
(5)写出反应④对应的化学方程式: .
(6)E的同分异构体有多种,其中能与NaHCO3反应的同分异构体共有种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni﹣Cd)可充电电池在现代生活中有广泛应用.电解质溶液为KOH溶液,电池反应为:Cd+2NiO(OH)+2H2O ![]() Cd(OH)2+2Ni(OH)2 , 下列有关镍镉电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2 , 下列有关镍镉电池的说法正确的是( )
A.充电过程是化学能转化为电能的过程
B.充电时阳极反应为Cd(OH)2+2e﹣═Cd+2OH﹣
C.放电时电池内部OH﹣向正极移动
D.充电时与直流电源正极相连的电极上发生Ni(OH)2转化为NiO(OH)的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯是最重要的基本有机化工原料之一,现利用苯,同时使用其他部分试剂,可实现如下转化:请回答下列问题: 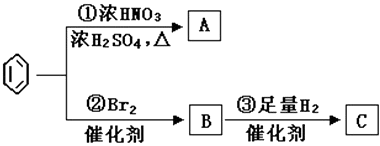
(1)C的结构简式为;
(2)写出下列反应的化学方程式:反应①:;反应②:;
(3)上述反应①~③中,属于加成反应的是(填序号).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com